
題目列表(包括答案和解析)
|
溫度為T時,向2.0 L恒容密閉容器中充入1.0 mol PCl5,反應PCl5(g)
以下對反應過程的分析和判斷正確的是 | |
A. |
反應在前50 s的平均速率為v(PCl3)=0.0032 mol·L-1·s-1 |
B. |
保持其他條件不變,若升高溫度,平衡時,c(PCl3)=0.11 mol·L-1,則反應為放熱反應 |
C. |
相同溫度下,若起始時向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,則達平衡前v(正)>v(逆) |
D. |
相同溫度下,若起始時向容器中充入2.0 mol PCl3、2.0 mol Cl2,則達平衡時,PCl3的轉化率大于80% |
| 3 |
| 4 |
| 3 |
| 4 |
| 3 |
| 4 |
| 3 |
| 4 |
I.科學家一直致力于“人工固氮”的方法研究。目前合成氨的技術原理為氮氣和氫氣在高溫高壓催化劑條件下生成氨氣,一定條件下,向一個2L的密閉容器中充入2molN2和6molH2,反應達平衡時生成NH3的濃度為0.5mol/L,并放出QkJ熱量,該反應的熱化學方程式可表示為______。
II.已知:N2O4(g)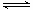 2NO2(g)
△H=+57.20kJ/mol。
2NO2(g)
△H=+57.20kJ/mol。
在1000C時,將0.100molN2O4氣體充入lL恒容抽空的密閉容器中,每隔一定時間對該容器內的物質濃度進行分析得到下表數據:
|
時間(s) |
0 |
20 |
40 |
60 |
80 |
|
c(N2O4)/mol |
0.100 |
c1 |
0.050 |
c3 |
c4 |
|
c(NO2)/mol |
0.000 |
0.060 |
c2 |
0.120 |
0.120 |
(1)該反應的平衡常數表達式為______;從表中數據分析:c1 ______c2、c3______c4(選填“>”、“<”或“=”)。
(2)在右圖中畫出并標明此反應中N2O4和NO2的濃度隨時間變化的曲線。
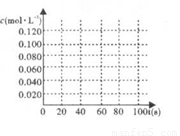
(3)在上述條件下,從反應開始至達到化學平衡時,四氧化二氮的平均反應速率為______。
(4)若起始時充入NO2氣體0.200mol,則達到平衡時NO2 氣體的轉化率為______;其它條件不變時,下列措施能提高NO2轉化率的是______ (填字母)。
A.減小NO2的濃度 B.降低溫度 C.增加NO2的濃度
D.升高溫度 E.再充入一定量的He
(5)向容積相同、溫度分別為T1和T1的兩個密閉容器中分別充入等量NO2,發生反應:2NO2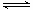 N2O4(g) (g) △H=-57.20kJ/mol。恒溫恒容下反應相同時間后,分別測得體系中NO2的百分含量分別為a1和a2。巳知T1<T2,則a1____a2
(選擇A、B、C、D填空)。
N2O4(g) (g) △H=-57.20kJ/mol。恒溫恒容下反應相同時間后,分別測得體系中NO2的百分含量分別為a1和a2。巳知T1<T2,則a1____a2
(選擇A、B、C、D填空)。
A.大于 B.小于 C.等于 D.以上都有可能
I.科學家一直致力于“人工固氮”的方法研究。目前合成氨的技術原理為氮氣和氫氣在高溫高壓催化劑條件下生成氨氣,一定條件下,向一個2L的密閉容器中充入2molN2和6molH2,反應達平衡時生成NH3的濃度為0.5mol/L,并放出QkJ熱量,該反應的熱化學方程式可表示為______。
II.已知:N2O4(g) 2NO2(g) △H=+57.20kJ/mol。
2NO2(g) △H=+57.20kJ/mol。
在1000C時,將0.100molN2O4氣體充入lL恒容抽空的密閉容器中,每隔一定時間對該容器內的物質濃度進行分析得到下表數據:
| 時間(s) | 0 | 20 | 40 | 60 | 80 |
| c(N2O4)/mol | 0.100 | c1 | 0.050 | c3 | c4 |
| c(NO2)/mol | 0.000 | 0.060 | c2 | 0.120 | 0.120 |

 N2O4(g)(g) △H=-57.20kJ/mol。恒溫恒容下反應相同時間后,分別測得體系中NO2的百分含量分別為a1和a2。巳知T1<T2,則a1____a2(選擇A、B、C、D填空)。
N2O4(g)(g) △H=-57.20kJ/mol。恒溫恒容下反應相同時間后,分別測得體系中NO2的百分含量分別為a1和a2。巳知T1<T2,則a1____a2(選擇A、B、C、D填空)。研究人員通過對北京地區PM2.5的化學組成研究發現,汽車尾氣和燃煤污染分別 占4%、l8%
I.(1)用于凈化汽車尾氣的反應為:2NO(g)+2CO(g) 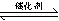 2CO2(g)+N2(g),已知該反應在570K時的平衡常數為1×1059,但反應速率極慢。下列說法正確的是:
2CO2(g)+N2(g),已知該反應在570K時的平衡常數為1×1059,但反應速率極慢。下列說法正確的是:
| A.裝有尾氣凈化裝置的汽車排出的氣體中不再含有NO或CO |
| B.提高尾氣凈化效率的最佳途徑是使用高效催化劑 |
| C.增大壓強,上述平衡右移,故實際操作中可通過增壓的方式提高其凈化效率 |
| D.提高尾氣凈化效率的常用方法是升高溫度 |
 N2(g)+CO2(g)
N2(g)+CO2(g)  H=akJ·mol-1,向某密閉容器加入一定量的活性炭和NO,恒溫(T1℃)條件下反應,反應進行到不同時間測得各物質的濃度如下:
H=akJ·mol-1,向某密閉容器加入一定量的活性炭和NO,恒溫(T1℃)條件下反應,反應進行到不同時間測得各物質的濃度如下:| 濃度/mol·L-1 時間/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.050 | 0.025 | 0.025 |
| 30 | 0.050 | 0.025 | 0.025 |
| 40 | 0.036 | 0.032 | 0.010 |
| 50 | 0.036 | 0.032 | 0.010 |
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com