
題目列表(包括答案和解析)
(15分)硝酸是一種重要的化工原料,工業(yè)上生產(chǎn)硝酸的主要過(guò)程如下。
(1)以N2和H2為原料合成氨氣。反應(yīng)N2(g)+3H2(g)2NH3(g)△H<0
①下列措施可以提高H2的轉(zhuǎn)化率是(填選項(xiàng)序號(hào)) 。
a.選擇適當(dāng)?shù)拇呋瘎?nbsp; b.增大壓強(qiáng)
c.及時(shí)分離生成的NH3 d.升高溫度
②一定溫度下,在密閉容器中充入1molN2和3molH2發(fā)生反應(yīng)。若容器容積恒定,達(dá)到平衡狀態(tài)時(shí),氣體的總物質(zhì)的量是原來(lái)的![]() ,則N2的轉(zhuǎn)化率a1= ;
,則N2的轉(zhuǎn)化率a1= ;
若容器壓強(qiáng)恒定,達(dá)到平衡狀態(tài)時(shí),N2的轉(zhuǎn)化率為a2,則a2 a1(填“>”、“<”或“=”)。
(2)以氨氣、空氣為主要原料制硝酸。
①NH3被氧氣催化氧化生成NO的反應(yīng)的化學(xué)方程式是 。
②在容積恒定的密閉容器中進(jìn)行反應(yīng)2NO(g)+O2(g)2NO2(g):△H>0
該反應(yīng)的反應(yīng)速率(v)隨時(shí)間(t)變化的關(guān)系如右圖所示。若t2、t4時(shí)刻只改變一個(gè)條件,下列說(shuō)法正確的是(填選項(xiàng)序號(hào)) 。
a.在t1~t2時(shí),可依據(jù)容器內(nèi)氣體的壓強(qiáng)保持不變判斷反應(yīng)已達(dá)到平衡狀態(tài);
b.在t2時(shí),采取的措施可以是升高溫度;
c.在t3~t4時(shí),可依據(jù)容器內(nèi)氣體的密度保持不變判斷反應(yīng)已達(dá)到平衡狀態(tài);
d.在t5時(shí),容器內(nèi)NO2的體積分?jǐn)?shù)是整個(gè)過(guò)程中的最大值。(3)硝酸廠常用如下2種方法處理尾氣。
①催化還原法:催化劑存在時(shí)用H2將NO2還原為N2。
已知:2H2(g)+O2(g)=2H2O(g): △H=-483.6kJ/mol
N2(g)+2O2(g)=2NO2(g): △H=+67.7kJ/mol
則H2還原NO2生成水蒸氣反應(yīng)的熱化學(xué)方程式是 。
②堿液吸收法:用Na2CO3溶液吸收NO2生成CO2。
若每9.2gNO2和Na2CO3溶液反應(yīng)時(shí)轉(zhuǎn)移電子數(shù)為0.1mol,則反應(yīng)的離子方程式是 。
(14分)硝酸是一種重要的化工原料,工業(yè)上生產(chǎn)硝酸的主要過(guò)程如下:
(1)以N2和H2為原料合成氨氣。反應(yīng)N2(g)+3H2(g)2NH3(g) △H<0
①下列措施可以提高H2的轉(zhuǎn)化率是(填選項(xiàng)序號(hào)) 。
a.選擇適當(dāng)?shù)拇呋瘎?nbsp; b.增大壓強(qiáng)
c.及時(shí)分離生成的NH3 d.升高溫度
②一定溫度下,在密閉容器中充入1molN2和3molH2發(fā)生反應(yīng)。若容器容積恒定,達(dá)到平衡狀態(tài)時(shí),氣體的總物質(zhì)的理是原來(lái)的,則N2的轉(zhuǎn)化率a1= ;
若容器壓強(qiáng)恒定,達(dá)到平衡狀態(tài)時(shí),N2的轉(zhuǎn)化率為a2,則a2 a1(填“>”、“<”或“=”)。
(2)以氨氣、空氣為主要原料制硝酸。
①NH3被氧氣催化氧化生成NO的反應(yīng)的化學(xué)方程式是 。
②在容積恒定的密閉容器中進(jìn)行反應(yīng)2NO(g)+O2(g)2NO2(g)△H>0
該反應(yīng)的反應(yīng)速率(v)隨時(shí)間(t)變化的關(guān)系如右圖所示。若t2、t4時(shí)刻只改變一個(gè)條件,下列說(shuō)法正確的是(填選項(xiàng)序號(hào)) 。
a.在t1~t2時(shí),可依據(jù)容器內(nèi)氣體的壓強(qiáng)保持不變判斷反應(yīng)已達(dá)到平衡狀態(tài)
b.在t2時(shí),采取的措施可以是升高溫度
c.在t3~ t4時(shí),可依據(jù)容器內(nèi)氣體的密度保持不變判斷反應(yīng)已達(dá)到平衡狀態(tài)
d.在t5時(shí),容器內(nèi)NO2的體積分?jǐn)?shù)是整個(gè)過(guò)程中的最大值
(3)硝酸廠常用如下2種方法處理尾氣。
①催化還原法:催化劑存在時(shí)用H2將NO2還原為N2。
已知:2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol
N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ/mol
則H2還原NO2生成水蒸氣反應(yīng)的熱化學(xué)方程式是 。
②堿液吸收法:用Na2CO3溶液吸收NO2生成CO2。
若每9.2gNO2和Na2FCO3溶液反應(yīng)時(shí)轉(zhuǎn)移電子數(shù)為0.1mol,則反應(yīng)的離子方程式是 。
(14分)硝酸 是一種重要的化工原料,工業(yè)上生產(chǎn)硝酸的主要過(guò)程如下:
是一種重要的化工原料,工業(yè)上生產(chǎn)硝酸的主要過(guò)程如下:
(1)以N2和H2為原料合成氨氣。反應(yīng)N2(g)+3H2(g) 2NH3(g) △H<0
2NH3(g) △H<0
①下列措施可以提高H2的轉(zhuǎn)化率是(填選項(xiàng)序號(hào)) 。
a.選擇適當(dāng)?shù)拇呋瘎?nbsp; b.增大壓強(qiáng)
c.及時(shí)分離生成的NH3 d.升高溫度
②一定溫度下,在密閉容器中充入1molN2和3molH2發(fā)生反應(yīng)。若容器容積恒定,達(dá)到平衡狀態(tài)時(shí),氣體的總物質(zhì)的理是原來(lái)的 ,則N2的轉(zhuǎn)化率a1= ;
,則N2的轉(zhuǎn)化率a1= ;
若容器壓強(qiáng)恒定,達(dá)到平衡狀態(tài)時(shí),N2的轉(zhuǎn)化率為a2,則a2 a1(填“>”、“<”或“=”)。
(2)以氨氣、空氣為主要原料制硝酸。
①NH3被氧氣催化氧化生成NO的反應(yīng)的化學(xué)方程式是 。
②在容積恒定的密閉容器中進(jìn)行反應(yīng)2NO(g)+O2(g) 2NO2(g)△H>0
2NO2(g)△H>0
該反應(yīng)的反應(yīng)速率(v)隨時(shí)間(t)變化的關(guān)系如右圖所示。若t2、t4時(shí)刻只改變一個(gè)條件,下列說(shuō)法正確的是(填選項(xiàng)序號(hào)) 。
a.在t1~t2時(shí),可依據(jù)容器內(nèi)氣體的壓強(qiáng)保持不變判斷反應(yīng)已達(dá)到平衡狀態(tài)
b.在t2時(shí),采取的措施可以是升高溫度
c.在t3~ t4時(shí),可依據(jù)容器內(nèi)氣體的密度保持不變判斷反應(yīng)已達(dá)到平衡狀態(tài)
d.在t5時(shí),容器內(nèi)NO2的體積分?jǐn)?shù)是整個(gè)過(guò)程中的最大值
(3)硝酸廠常用如下2種方法處理尾氣。
①催化還原法:催化劑存在時(shí)用H 2將NO2還原為N2。
2將NO2還原為N2。
已知:2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol
N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ/mol
則H2還原NO2生成水蒸氣反應(yīng)的熱化學(xué)方程式是 。
②堿液吸收法:用Na2CO3溶液吸收NO2生成CO2。
若每9.2gNO2和Na2FCO3溶液反應(yīng)時(shí)轉(zhuǎn)移電子數(shù)為0.1mol,則反應(yīng)的離子方程式是 。
(15分)硝酸是一種重要的化工原料,工業(yè)上生產(chǎn)硝酸的主要過(guò)程如下。
(1)以N2和H2為原料合成氨氣。反應(yīng)N2(g)+3H2(g) 2NH3(g)△H<0
2NH3(g)△H<0
①下列措施可以提高H2的轉(zhuǎn)化率是(填選項(xiàng)序號(hào)) 。
a.選擇適當(dāng)?shù)拇呋瘎?nbsp; b.增大壓強(qiáng)
c.及時(shí)分離生成的NH3 d.升高溫度
②一定溫度下,在密閉容器中充入1molN2和3molH2發(fā)生反應(yīng)。若容器容積恒定,達(dá)到平衡狀態(tài)時(shí),氣體的總物質(zhì)的量是原來(lái)的 ,則N2的轉(zhuǎn)化率a1=
;
,則N2的轉(zhuǎn)化率a1=
;
若容器壓強(qiáng)恒定,達(dá)到平衡狀態(tài)時(shí),N2的轉(zhuǎn)化率為a2,則a2 a1(填“>”、“<”或“=”)。
(2)以氨氣、空氣為主要原料制硝酸。
①NH3被氧氣催化氧化生成NO的反應(yīng)的化學(xué)方程式是 。
②在容積恒定的密閉容器中進(jìn)行反應(yīng)2NO(g)+O2(g) 2NO2(g):△H>0
2NO2(g):△H>0
該反應(yīng)的反應(yīng)速率(v)隨時(shí)間(t)變化的關(guān)系如右圖所示。若t2、t4時(shí)刻只改變一個(gè)條件,下列說(shuō)法正確的是(填選項(xiàng)序號(hào)) 。

a.在t1~t2時(shí),可依據(jù)容器內(nèi)氣體的壓強(qiáng)保持不變判斷反應(yīng)已達(dá)到平衡狀態(tài);
b.在t2時(shí),采取的措施可以是升高溫度;
c.在t3~t4時(shí),可依據(jù)容器內(nèi)氣體的密度保持不變判斷反應(yīng)已達(dá)到平衡狀態(tài);
d.在t5時(shí),容器內(nèi)NO2的體積分?jǐn)?shù)是整個(gè)過(guò)程中的最大值。(3)硝酸廠常用如下2種方法處理尾氣。
①催化還原法:催化劑存在時(shí)用H2將NO2還原為N2。
已知:2H2(g)+O2(g)=2H2O(g): △H=-483.6kJ/mol
N2(g)+2O2(g)=2NO2(g): △H=+67.7kJ/mol
則H2還原NO2生成水蒸氣反應(yīng)的熱化學(xué)方程式是 。
②堿液吸收法:用Na2CO3溶液吸收NO2生成CO2。
若每9.2gNO2和Na2CO3溶液反應(yīng)時(shí)轉(zhuǎn)移電子數(shù)為0.1mol,則反應(yīng)的離子方程式是 。
(14分)硝酸是一種重要的化工原料,工業(yè)上生產(chǎn)硝酸的主要過(guò)程如下:
(1)以N2和H2為原料合成氨氣。反應(yīng)N2(g)+3H2(g)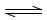 2NH3(g) △H<0
2NH3(g) △H<0
①下列措施可以提高H2的轉(zhuǎn)化率是(填選項(xiàng)序號(hào)) 。
a.選擇適當(dāng)?shù)拇呋瘎?nbsp; b.增大壓強(qiáng)
c.及時(shí)分離生成的NH3 d.升高溫度
②一定溫度下,在密閉容器中充入1molN2和3molH2發(fā)生反應(yīng)。若容器容積恒定,達(dá)到平衡狀態(tài)時(shí),氣體的總物質(zhì)的理是原來(lái)的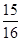 ,則N2的轉(zhuǎn)化率a1= ;
,則N2的轉(zhuǎn)化率a1= ;
若容器壓強(qiáng)恒定,達(dá)到平衡狀態(tài)時(shí),N2的轉(zhuǎn)化率為a2,則a2 a1(填“>”、“<”或“=”)。
(2)以氨氣、空氣為主要原料制硝酸。
①NH3被氧氣催化氧化生成NO的反應(yīng)的化學(xué)方程式是 。
②在容積恒定的密閉容器中進(jìn)行反應(yīng)2NO(g)+O2(g)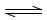 2NO2(g)△H>0
2NO2(g)△H>0
該反應(yīng)的反應(yīng)速率(v)隨時(shí)間(t)變化的關(guān)系如右圖所示。若t2、t4時(shí)刻只改變一個(gè)條件,下列說(shuō)法正確的是(填選項(xiàng)序號(hào)) 。
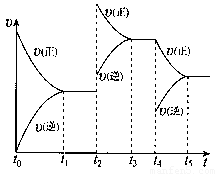
a.在t1~t2時(shí),可依據(jù)容器內(nèi)氣體的壓強(qiáng)保持不變判斷反應(yīng)已達(dá)到平衡狀態(tài)
b.在t2時(shí),采取的措施可以是升高溫度
c.在t3~ t4時(shí),可依據(jù)容器內(nèi)氣體的密度保持不變判斷反應(yīng)已達(dá)到平衡狀態(tài)
d.在t5時(shí),容器內(nèi)NO2的體積分?jǐn)?shù)是整個(gè)過(guò)程中的最大值
(3)硝酸廠常用如下2種方法處理尾氣。
①催化還原法:催化劑存在時(shí)用H2將NO2還原為N2。
已知:2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol
N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ/mol
則H2還原NO2生成水蒸氣反應(yīng)的熱化學(xué)方程式是 。
②堿液吸收法:用Na2CO3溶液吸收NO2生成CO2。
若每9.2gNO2和Na2FCO3溶液反應(yīng)時(shí)轉(zhuǎn)移電子數(shù)為0.1mol,則反應(yīng)的離子方程式是 。
百度致信 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無(wú)主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com