
題目列表(包括答案和解析)
 A、【供選學《化學與生活》考生作答】
A、【供選學《化學與生活》考生作答】| 溫度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
 “白鐵皮”具有較強的耐腐蝕性,是生產中常用的金屬材料之一.鍍鋅層猶如鐵皮的保護層,這層膜的厚度及均勻度也成了判斷鍍層質量的重要指標.某研究性學習小組為了測定鍍鋅鐵皮的厚度,設計了下面的實驗方案:
“白鐵皮”具有較強的耐腐蝕性,是生產中常用的金屬材料之一.鍍鋅層猶如鐵皮的保護層,這層膜的厚度及均勻度也成了判斷鍍層質量的重要指標.某研究性學習小組為了測定鍍鋅鐵皮的厚度,設計了下面的實驗方案:
| ||
| 2S×7.14 |
| ||
| 2S×7.14 |
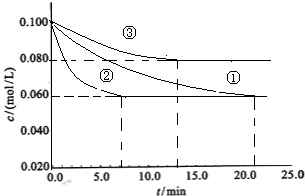
| c2(NH3)平衡 |
| c(N2)平衡c3(H2)平衡 |
| c2(NH3)平衡 |
| c(N2)平衡c3(H2)平衡 |
“白鐵皮”具有較強的耐腐蝕性,是生產中常用的金屬材料之一。鍍鋅層猶如鐵皮的保護層,這層膜的厚度及均勻度也成了判斷鍍層質量的重要指標。某研究性學習小組為了測定鍍鋅鐵皮的厚度,設計了下面的實 驗方案:
驗方案:
方案一:取三塊鍍鋅鐵皮(A、B、C,截自同一塊鍍鋅鐵皮),將鍍鋅鐵皮A放入燒杯中,加入40mL 6mol·L—1鹽酸,反應時用玻璃棒小心翻動鍍鋅鐵皮,待鋅鍍層反應完全時,立即將未反應的鐵皮取出,洗滌、小心烘干、稱量。將B、C重復上面的實驗。
(1)鋅鍍層完全反應的標志是 。
(2)如何檢驗鐵片已經洗凈
。
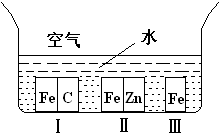
方案二:已知鋅與強堿溶液反應的離子方程式為:Zn+2OH—+2H2O=[Zn(OH)4]2—+H2↑。某同學按右圖裝置設計了測定鍍鋅鐵皮鍍層厚度的實驗方案,將單側面積為S cm2、質量為mg的鍍鋅鐵皮放入6mol·L—1 NaOH溶液中。回答下列問題:
(3)裝置中導管a的作用是 。
(4)檢查氣密性,將藥品和水裝入各儀器中,連接好裝置后,需進行的操作還有:
①記錄C的液面位置;②待B中不再有氣體產生并恢復至室溫;③由A向B中滴加足量NaOH溶液;④上下移動C,使干燥管和C中液面相平。
上述操作的順序是 (填序號)。
(5)實驗前后堿式滴定管中液面讀數分別為V1 mL、V2 mL(已知Zn的密度為7.14g/cm3,實驗條件的氣體摩爾體積為Vm L / mol)。則鍍鋅鐵皮的鍍層厚度為 cm。(寫出數學表達式)
(16分)氨氣是一種重要的基礎化工原料,用途廣泛。
(1)在微電子工業中,氨水可作刻蝕劑H2O2的清除劑,產物不污染環境。該反應的化學方程式為2NH3 + 3H2O2= +6H2O
(2)工業中常用以下反應合成氨:N2+3H2 2NH3 △H<0。某實驗室在三個不同條件的密閉容器中,分別加入N2和H2,濃度均為c(N2) =" 0.100mol/L," c(H2) = 0.300mol/L,進行反應時, N2的濃度隨時間的變化如圖①、②、③曲線所示。
2NH3 △H<0。某實驗室在三個不同條件的密閉容器中,分別加入N2和H2,濃度均為c(N2) =" 0.100mol/L," c(H2) = 0.300mol/L,進行反應時, N2的濃度隨時間的變化如圖①、②、③曲線所示。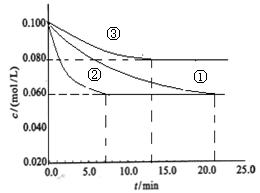
該反應平衡常數的數學表達式為 ;實驗②平衡時H2的轉化率為_____ 。
(3)據圖所示,②、③兩裝置中各有一個條件與①不同。請指出,并說明判斷的理由。
②條件:_______ 理由: ________
③條件:_______ 理由: ________
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com