
題目列表(包括答案和解析)
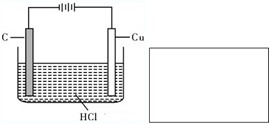 鹽酸、硫酸和硝酸是中學常見的三種酸.
鹽酸、硫酸和硝酸是中學常見的三種酸.
| ||
| ||

| ||
| H | + 4 |
| O | 2- 4 |
| O | - 3 |
| O | - 3 |

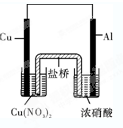
(1)寫出A、B兩試管中的實驗現象:
A__________________________________、__________________________________(兩種即可);B__________________________________。
(2)充分反應后,發現銅和硫酸都有剩余。在不補充濃硫酸的前提下,若使剩余銅片溶解,可再加入物質的化學式為____________________。
(3)測定剩余硫酸的物質的量時,先測銅與濃硫酸反應產生SO2的量,再計算余酸的物質的量。他認為測定SO2的量的方法有多種,下列方案中不可行的是( )
A.將A產生的氣體干燥后緩緩通過預先稱量的盛有堿石灰的干燥管,結束反應后再次稱量
B.將A產生的氣體緩緩通入稀硫酸酸化的KMnO4溶液,加足量BaCl2溶液,過濾、洗滌、干燥、稱量沉淀
C.將A產生的氣體緩緩通入足量用HNO3酸化的Ba(NO3)2溶液,充分反應過濾、洗滌、干燥、稱量沉淀
D.用排飽和NaHSO3溶液的方法測出干燥后裝置A產生SO2氣體的體積(已折算成標準狀況)
(4)向反應后的溶液中加入足量的氧化銅,使剩余的硫酸轉化為硫酸銅,過濾后將濾液加熱濃縮,冷卻制得硫酸銅晶體(CuSO4·xH2O),用加熱法測定該晶體里結晶水x的值。其中一次實驗的數據為:
坩堝質量 | 坩堝與晶體總質量 | 加熱后坩堝與固體總質量 |
11.7 | G | 11.7 |
根據數據計算,判斷x的實測值比理論值(x=5)_________(填“偏大”或“偏小”),實驗中產生誤差的原因可能是_________(填字母編號)。
A.硫酸銅晶體中含有不揮發雜質
B.加熱失水后露置在空氣中冷卻
C.加熱時有晶體飛濺出去
D.硫酸銅晶體(CuSO4·xH2O)在稱量前晶體的表面吸收了水分
| ||
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com