
題目列表(包括答案和解析)
| 通電 |
| 一定條件 |
| c4(NH3)?c3(O2) |
| c2(N2)?c6(H2O) |
| c4(NH3)?c3(O2) |
| c2(N2)?c6(H2O) |

已知理想氣體各參數(shù)p(壓強(qiáng))、V(體積)、T(溫度)、n(物質(zhì)的量)滿足理想氣體狀態(tài)方程pV=nRT。某學(xué)校課外活動小組粗略測定理想氣體狀態(tài)方程中氣體常數(shù)R的值,下面是測定實驗的分析報告,請?zhí)顚懹嘘P(guān)空白:
(一)測定原理:在理想氣體狀態(tài)方程pV=nRT中,氣體常數(shù)R=pV/nT的數(shù)值可以通過實驗來確定。本實驗通過金屬鎂置換出鹽酸中的氫來測定R的值。其反應(yīng)為:
Mg+2HCl=MgCl2+H2↑
如果稱取一定質(zhì)量的鎂與過量的鹽酸反應(yīng),則在一定溫度和壓力下,可以通過測出反應(yīng)放出氫氣的體積。實驗室的溫度和壓力可以分別由溫度計和氣壓計測得。氫氣物質(zhì)的量可以通過反應(yīng)中鎂的質(zhì)量來求得。將以上所得各項數(shù)據(jù)代入R= pV /nT式中,即可算出R值。
 (二)實驗用品及試劑:①儀器:托盤天平、測定氣體常數(shù)的裝置(如上圖所示);②試劑:6mol·L-1HCl、鎂條若干。
(二)實驗用品及試劑:①儀器:托盤天平、測定氣體常數(shù)的裝置(如上圖所示);②試劑:6mol·L-1HCl、鎂條若干。
(三)實驗內(nèi)容:
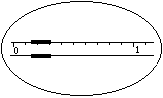
1.在托盤天平上稱出鎂條的質(zhì)量(稱量鎂條天平的游碼示數(shù)如右圖所示,未用砝碼,單位為g);
2.按上圖搭好儀器。取下試管,移動量氣管B,使量氣管A中的水面略低于零刻度線,然后將量氣管B固定。
3.在試管中加入15mL 6 mol·L-1HCl,不要使鹽酸沾濕試管的上半部。將已稱重的鎂沾少許水,貼在試管上部不與鹽酸接觸。
4.檢查儀器是否漏氣,方法如下:(方法要求簡單有效)
。
 5.如果裝置不漏氣,調(diào)整量氣管B的位置,使量氣管A內(nèi)水面與量氣管B 內(nèi)水面在同一水平面上(要求“在同一水平面上”的原因是 ;實現(xiàn)“在同一水平面上”的操作是 ),然后準(zhǔn)確讀出量氣管A內(nèi)水面凹面最低點的讀數(shù)V1(如右圖所示)。
5.如果裝置不漏氣,調(diào)整量氣管B的位置,使量氣管A內(nèi)水面與量氣管B 內(nèi)水面在同一水平面上(要求“在同一水平面上”的原因是 ;實現(xiàn)“在同一水平面上”的操作是 ),然后準(zhǔn)確讀出量氣管A內(nèi)水面凹面最低點的讀數(shù)V1(如右圖所示)。
6.輕輕搖動試管,使鎂條落入鹽酸中,鎂條與鹽酸反應(yīng)放出氫氣。此時量氣管A內(nèi)水面即開始下降。為了不使量氣管A內(nèi)氣壓增大而造成漏氣,在量氣管A內(nèi)水面下降的同時,慢慢 (上或下)移量氣管B,使兩管內(nèi)的水面基本保持水平。反應(yīng)停止后,待試管冷卻至室溫(約10分鐘),移動量氣管B,使兩管內(nèi)的水面相平,讀出反應(yīng)后量氣管A內(nèi)的精確讀數(shù)V2(如右圖所示)。
7.記錄實驗時的室溫t和大氣壓P。(已知室溫為27℃,大氣壓為100kPa)
(四)數(shù)據(jù)記錄與處理(在橫線上填寫適當(dāng)內(nèi)容):
| 鎂條的質(zhì)量 | w= |
| g |
| 氫氣的物質(zhì)的量 | n= |
| mol |
| 反應(yīng)前量氣管A內(nèi)讀數(shù) | V1= |
| ml |
| 反應(yīng)后量氣管A內(nèi)讀數(shù) | V2= |
| ml |
| 氫氣的體積 | V |
| ml |
| 室溫 | T |
| K |
| 大氣壓 | P |
| Pa |
氣體常數(shù)R的值(計算過程和結(jié)果):
(五)問題與討論:①在讀取量氣管內(nèi)氣體體積V1時,眼睛仰視讀數(shù),結(jié)果造成R的測定值 (偏高、偏低或無影響);②若沒等反應(yīng)試管冷卻到室溫就量取液面的高度,結(jié)果造成R的測定值 (偏高、偏低或無影響)。
人工固氮是指將氮元素由游離態(tài)轉(zhuǎn)化為化合態(tài)的過程。
I.最近一些科學(xué)家研究采用高質(zhì)子導(dǎo)電性的SCY陶瓷(能傳遞H+)實驗氮的固定一電解法合成氨,大大提高了氮氣和氫氣的轉(zhuǎn)化率。總反應(yīng)式為:N2(g)+3H2(g)  2NH3(g),則在電解法合成氨的過程中,應(yīng)將H2不斷地通入_________極(填“陰”或“陽”) ;向另一電極通入N2,該電極的反應(yīng)式為__________________________。
2NH3(g),則在電解法合成氨的過程中,應(yīng)將H2不斷地通入_________極(填“陰”或“陽”) ;向另一電極通入N2,該電極的反應(yīng)式為__________________________。
II.據(jù)報道,在一定條件下,N2在摻有少量氧化鐵的二氧化鈦催化劑表面能與水發(fā)生反應(yīng),主要產(chǎn)物為NH3,相應(yīng)的反應(yīng)方程式為:2N2(g)+6H2O(g) 4NH3(g)+3O2(g) △H=Q。
4NH3(g)+3O2(g) △H=Q。
(1)上述反應(yīng)的平衡常數(shù)表達(dá)式為_______________。
(2)取五份等體積N2和H2O的混合氣體(物質(zhì)的量之比均為1:3),分別加入體積相同的恒容密閉容器中,在溫度不相同的情況下發(fā)生反應(yīng),反應(yīng)相同時間后,測得氮氣的體積分?jǐn)?shù) 與反應(yīng)溫度T的關(guān)系曲線如圖所示,則上述反應(yīng)的Q________0(填“>”、“<”或“=”)。
與反應(yīng)溫度T的關(guān)系曲線如圖所示,則上述反應(yīng)的Q________0(填“>”、“<”或“=”)。

(3)若上述反應(yīng)在有催化劑的情況下發(fā)生,則下圖所示的a、b、c、d四條曲線中,能表示反應(yīng)體系能量變化的是_______(選填字母代號),圖中△H的絕對值為1530kJ·mol-1。

III.目前工業(yè)合成氨的原理是:N2(g)+3H2(g)  2NH3(g) △H=-93.0kJ/mol。
2NH3(g) △H=-93.0kJ/mol。
回答下列問題:
(1)結(jié)合II中的數(shù)據(jù),則O2(g)+2H2(g)=2H2O(g)的△H=______________。
(2)在一定溫度下,將1molN2和3mol H2混合置于體積不變的密閉容器中發(fā)生反應(yīng),達(dá)到平衡狀態(tài)時,測得氣體總物質(zhì)的量為2.8mol。
①達(dá)平衡時,H2的轉(zhuǎn)化率α1=______________。
②在相同條件下,若起始時只將NH3置于該容器中,達(dá)到平衡狀態(tài)時NH3的轉(zhuǎn)化率為α2,當(dāng)α1+α2=1時,則起始時NH3的物質(zhì)的量n(NH3)=_____________mol。
 2NH3(g)
2NH3(g)
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com