
題目列表(包括答案和解析)
(10分)
I.(4分)某溫度下的溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L。x與y的關系如圖所示:

(1)該溫度下,中性溶液的pH= 。
(2)該溫度下0.01 mol/L NaOH溶液的pH= 。
II. (6分)某研究小組在實驗室探究氨基甲酸銨(NH2COONH4)分解反應平衡常數和水解反應速率的測定。
(1)將一定量純凈的氨基甲酸銨置于特制的密閉真空容器中(假設容器體積不變,固體試樣體積忽略不計),在恒定溫度下使其達到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)。實驗測得不同溫度下的平衡數據列于下表:
2NH3(g)+CO2(g)。實驗測得不同溫度下的平衡數據列于下表:
|
溫度(℃) |
15.0 |
20.0 |
25.0 |
30.0 |
35.0 |
|
平衡總壓強(kPa) |
5.7 |
8.3 |
12.0 |
17.1 |
24.0 |
|
平衡氣體總濃度 (×10-3mol/L) |
2.4 |
3.4 |
4.8 |
6.8 |
9.4 |
①可以判斷該分解反應已經達到化學平衡的是 (填字母)。
A.2v(NH3)=v(CO2) B.密閉容器中總壓強不變
C.密閉容器中混合氣體的密度不變 D.密閉容器中氨氣的體積分數不變
②根據表中數據,計算25.0℃時的分解平衡常數為 。
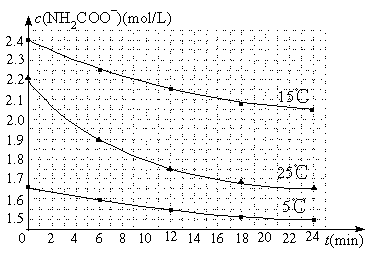
(2)已知:NH2COONH4+2H2O NH4HCO3+NH3·H2O。該研究小組分別用三份不同初始濃度的氨基甲酸銨溶液測定水解反應速率,得到c(NH2COO-)隨時間變化趨勢如圖所示。
NH4HCO3+NH3·H2O。該研究小組分別用三份不同初始濃度的氨基甲酸銨溶液測定水解反應速率,得到c(NH2COO-)隨時間變化趨勢如圖所示。

③計算25℃時,0~6min氨基甲酸銨水解反應的平均速率為 。
④根據圖中信息,如何說明水解反應的平均速率隨溫度升高而增大:
。
 I.(4分)某溫度下的溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L。x與y的關系如圖所示:
I.(4分)某溫度下的溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L。x與y的關系如圖所示:
(1)該溫度下,中性溶液的pH= 。
(2)該溫度下0.01 mol/L NaOH溶液的pH= 。
II. (6分)某研究小組在實驗室探究氨基甲酸銨(NH2COONH4)分解反應平衡常數和水解反應速率的測定。
(1)將一定量純凈的氨基甲酸銨置于特制的密閉真空容器中(假設容器體積不變,固體試樣體積忽略不計),在恒定溫度下使其達到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g)。實驗測得不同溫度下的平衡數據列于下表:
2NH3(g)+CO2(g)。實驗測得不同溫度下的平衡數據列于下表:
| 溫度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡總壓強(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡氣體總濃度 (×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
①可以判斷該分解反應已經達到化學平衡的是 (填字母)。
A.2v(NH3)=v(CO2) B.密閉容器中總壓強不變
C.密閉容器中混合氣體的密度不變 D.密閉容器中氨氣的體積分數不變
②根據表中數據,計算25.0℃時的分解平衡常數為 。
(2)已知:NH2COONH4+2H2O![]() NH4HCO3+NH3·H2O。該研究小組分別用三份不同初始濃度的氨基甲酸銨溶液測定水解反應速率,得到c(NH2COO-)隨時間變化趨勢如圖所示。
NH4HCO3+NH3·H2O。該研究小組分別用三份不同初始濃度的氨基甲酸銨溶液測定水解反應速率,得到c(NH2COO-)隨時間變化趨勢如圖所示。
③計算25℃時,0~6min氨基甲酸銨水解反應的平均速率為 。
④根據圖中信息,如何說明水解反應的平均速率隨溫度升高而增大:
。
(16分)某研究小組取足量形狀、質量均相同的鋁片,分別與濃度均為6 mol?L-1的等體積的鹽酸、氫氧化鈉溶液充分反應后,取出剩余的鋁片洗凈、干燥、稱量。
(1)上述反應剩余鋁片的質量,前者________后者(填“大于”或“小于”或“等于”)。
(2)觀察鋁片與鹽酸反應后的溶液較渾濁,且試管底部有少量黑色固體。
查資料已知:
①鋁與鹽酸反應,因反應過快而變成粉末分散到溶液中,形成黑色固體
②電解法冶煉鋁所用的原料氧化鋁是從鋁土礦中提取的,氧化鋁中往往還含有微量的氧化鐵和二氧化硅雜質。寫出在電解池中生成的鋁與雜質二氧化硅反應的化學方程式: ________。
(3)為探究(2)中黑色固體的成分,提出合理假設。
假設1:黑色固體是Al和Fe
假設2:黑色固體是Al和Si
假設3:黑色固體是Al和_______________
(4)設計實驗方案,基于假設3進行實驗,驗證黑色固體含有Al之外的其它成分。
限選實驗試劑:蒸餾水、6mol·L-1H2SO4溶液、6mol·L-1NaOH溶液、6mol·L-1氨水、0.01mol·L-1KMnO4溶液、新制氯水、20%KSCN溶液。
| 實驗步驟 | 預期實驗現象和結論 |
| 步驟1:將反應所得濁液過濾、洗滌,取少量固體于試管中,加入足量的6mol·L-1 H2SO4溶液,充分振蕩,靜置。 | ___________________________________, 證明黑色固體含有Si |
| 步驟2: | |

(16分)某研究小組取足量形狀、質量均相同的鋁片,分別與濃度均為6 mol•L-1的等體積的鹽酸、氫氧化鈉溶液充分反應后,取出剩余的鋁片洗凈、干燥、稱量。
(1)上述反應剩余鋁片的質量,前者________后者(填“大于”或“小于”或“等于”)。
(2)觀察鋁片與鹽酸反應后的溶液較渾濁,且試管底部有少量黑色固體。
查資料已知:
①鋁與鹽酸反應,因反應過快而變成粉末分散到溶液中,形成黑色固體
②電解法冶煉鋁所用的原料氧化鋁是從鋁土礦中提取的,氧化鋁中往往還含有微量的氧化鐵和二氧化硅雜質。寫出在電解池中生成的鋁與雜質二氧化硅反應的化學方程式: ________。
(3)為探究(2)中黑色固體的成分,提出合理假設。
假設1:黑色固體是Al和Fe
假設2:黑色固體是Al和Si
假設3:黑色固體是Al和_______________
(4)設計實驗方案,基于假設3進行實驗,驗證黑色固體含有Al之外的其它成分。
限選實驗試劑:蒸餾水、6mol·L-1H2SO4溶液、6mol·L-1NaOH溶液、6mol·L-1氨水、0.01mol·L-1KMnO4溶液、新制氯水、20%KSCN溶液。
|
實驗步驟 |
預期實驗現象和結論 |
|
步驟1:將反應所得濁液過濾、洗滌,取少量固體于試管中,加入足量的6mol·L-1 H2SO4溶液,充分振蕩,靜置。 |
___________________________________, 證明黑色固體含有Si |
|
步驟2:
|
|
(5)已知硅與NaOH溶液反應與鋁相似。取m1g黑色固體加足量NaOH溶液充分溶解,
濾去不溶物(不考慮可溶物的損失),配成250mL溶液,取出25.00mL溶液,按下列操作進行實驗:

在上述操作中,需要用到的玻璃定量儀器有________________________________;
計算黑色固體中Al的質量分數為__________________(相對原子質量:Al-27 Fe-56 H-1 O-16)。
(9分)某興趣小組探究SO2氣體還原Fe3+、I2,他們使用的藥品和裝置如下圖所示: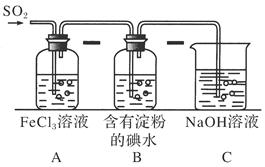
(1)SO2氣體還原Fe3+的產物是________、________(填離子符號),參加反應的SO2和Fe3+的物質的量之比是____。
(2)下列實驗方案適用于在實驗室制取所需SO2的是________(填序號)。
A.Na2SO3溶液與HNO3 B.Na2SO3固體與濃硫酸
C.固體硫在純氧中燃燒 D.銅與熱濃H2SO4
(3)裝置C的作用是____________________________________________________。
(4)若要從A中所得溶液提取晶體,必須進行的實驗操作步驟:蒸發、冷卻結晶、________、自然干燥,在這一系列操作中沒有用到的儀器有________(填序號)。
A.蒸發皿 B.石棉網 C.漏斗 D.燒杯 E.玻璃棒 F.坩堝
(5)在上述裝置中通入過量的SO2,為了驗證A中SO2與Fe3+發生了氧化還原反應,他們取A中的溶液,分成三份,并設計了如下實驗:
方案①:往第一份試液中加入KMnO4溶液,紫紅色褪去
方案②:往第二份試液中加入KSCN溶液,不變紅,再加入新制的氯水,溶液變紅
方案③:往第三份試液中加入用稀鹽酸酸化的BaCl2,產生白色沉淀。
上述方案不合理的是________,原因是____________________________________。
(6)能表明I-的還原性弱于SO2的現象是____________________________________。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com