
題目列表(包括答案和解析)
- 3 |
- 3 |
| ||
| 106(d-b) |
| 44a |
| 106(d-b) |
| 44a |
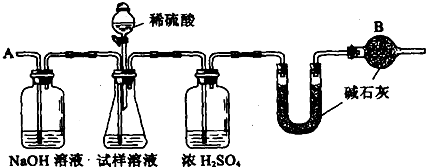
實驗室測定含碘廢液中I-的含量以及碘的回收過程如下:
Ⅰ.含碘廢液中I-含量的測定
用移液管量取25.00 mL廢液于250 mL錐形瓶中,分別加入5 mL 2 mol·L-1 H2SO4和10 mL 20% NH4Fe(SO4)2·12H2O溶液,搖勻。小火加熱蒸發至碘完全升華,取下錐形瓶冷卻后,加入10 mL 2 mol·L-1H2SO4,加入幾滴二苯胺磺酸鈉(用作指示劑),用0.0250 mol·L-1標準K2Cr2O7溶液進行滴定至終點。重復3次,數據記錄如下表:
(已知反應:①2Fe3++2I-=2Fe2++I2 ②6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O)
| 次數 | 1 | 2 | 3 |
| 滴定體積(mL) | 19.60 | 19.65 | 19.55 |
A. A、B、C、D、E、F為原子序數依次增大的短周期主族元素。 A、F原子的最外層電子數均等于其周期序數,F原子的電子層數是A的3倍;B原子核外電子分處3個不同能級,且每個能級上排布的電子數相同;A與C形成的最簡單分子為三角錐形;D原子p軌道上成對電子數等于未成對電子數;E原子核外每個原子軌道上的電子都已成對,E電負性小于F。
⑴寫出B的基態原子的核外電子排布式 。
⑵A、C形成的最簡單分子極易溶于水,其主要原因是 ;與該最簡單分子互為等電子體的陽離子為 。
⑶比較E、F的第一電離能:E F(選填“>”或“<”)。
⑷BD2在高溫高壓下所形成的晶胞如右圖所示。該晶體的類型屬于 (選填“分子”、“原子”、“離子”或“金屬”)晶體,該晶體中B原子的雜化形式為 。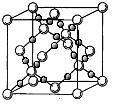
⑸光譜證實單質F與強堿性溶液反應有[F(OH)4]—生成,則[F(OH)4]—中存在 。
a.共價鍵 b.非極性鍵 c.配位鍵 d.σ鍵 e.π鍵
B.某研究性學習小組對過量炭粉與氧化鐵反應的氣體產物成分進行研究。
⑴提出假設 ①該反應的氣體產物是CO2。
②該反應的氣體產物是CO。
③該反應的氣體產物是 。
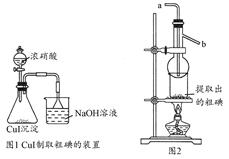
⑵設計方案 如圖所示,將一定量的氧化鐵在隔絕空氣的條件下與過量炭粉完全反應,測定參加反應的碳元素與氧元素的質量比。
⑶查閱資料
氮氣不與碳、氧化鐵發生反應。實驗室可以用氯化銨飽和溶液和亞硝酸鈉(NaNO2)飽和溶液混合加熱反應制得氮氣。
請寫出該反應的離子方程式: 。
⑷實驗步驟
①按上圖連接裝置,并檢查裝置的氣密性,稱取3.20g氧化鐵、2.00g碳粉混合均勻,放入48.48g的硬質玻璃管中;
②加熱前,先通一段時間純凈干燥的氮氣;
③停止通入N2后,夾緊彈簧夾,加熱一段時間,澄清石灰水(足量)變渾濁;
④待反應結束,再緩緩通入一段時間的氮氣。冷卻至室溫,稱得硬質玻璃管和固體總質量為52.24g;
⑤過濾出石灰水中的沉淀,洗滌、烘干后稱得質量為2.00g。
步驟②、④中都分別通入N2,其作用分別為 。
⑸數據處理
試根據實驗數據分析,寫出該實驗中氧化鐵與碳發生反應的化學方程式:
。
⑹實驗優化 學習小組有同學認為應對實驗裝置進一步完善。
①甲同學認為:應將澄清石灰水換成Ba(OH)2溶液,其理由是 。
②從環境保護的角度,請你再提出一個優化方案: 。
A. A、B、C、D、E、F為原子序數依次增大的短周期主族元素。 A、F原子的最外層電子數均等于其周期序數,F原子的電子層數是A的3倍;B原子核外電子分處3個不同能級,且每個能級上排布的電子數相同;A與C形成的最簡單分子為三角錐形;D原子p軌道上成對電子數等于未成對電子數;E原子核外每個原子軌道上的電子都已成對,E電負性小于F。
⑴寫出B的基態原子的核外電子排布式 。
⑵A、C形成的最簡單分子極易溶于水,其主要原因是 ;與該最簡單分子互為等電子體的陽離子為 。
⑶比較E、F的第一電離能:E F(選填“>”或“<”)。
⑷BD2在高溫高壓下所形成的晶胞如右圖所示。該晶體的類型屬于 (選填“分子”、“原子”、“離子”或“金屬”)晶體,該晶體中B原子的雜化形式為 。

⑸光譜證實單質F與強堿性溶液反應有[F(OH)4]—生成,則[F(OH)4]—中存在 。
a.共價鍵 b.非極性鍵 c.配位鍵 d.σ鍵 e.π鍵
B.某研究性學習小組對過量炭粉與氧化鐵反應的氣體產物成分進行研究。
⑴提出假設 ①該反應的氣體產物是CO2。
②該反應的氣體產物是CO。
③該反應的氣體產物是 。
⑵設計方案 如圖所示,將一定量的氧化鐵在隔絕空氣的條件下與過量炭粉完全反應,測定參加反應的碳元素與氧元素的質量比。

⑶查閱資料
氮氣不與碳、氧化鐵發生反應。實驗室可以用氯化銨飽和溶液和亞硝酸鈉(NaNO2)飽和溶液混合加熱反應制得氮氣。
請寫出該反應的離子方程式: 。
⑷實驗步驟
①按上圖連接裝置,并檢查裝置的氣密性,稱取3.20g氧化鐵、2.00g碳粉混合均勻,放入48.48g的硬質玻璃管中;
②加熱前,先通一段時間純凈干燥的氮氣;
③停止通入N2后,夾緊彈簧夾,加熱一段時間,澄清石灰水(足量)變渾濁;
④待反應結束,再緩緩通入一段時間的氮氣。冷卻至室溫,稱得硬質玻璃管和固體總質量為52.24g;
⑤過濾出石灰水中的沉淀,洗滌、烘干后稱得質量為2.00g。
步驟②、④中都分別通入N2,其作用分別為 。
⑸數據處理
試根據實驗數據分析,寫出該實驗中氧化鐵與碳發生反應的化學方程式:
。
⑹實驗優化 學習小組有同學認為應對實驗裝置進一步完善。
①甲同學認為:應將澄清石灰水換成Ba(OH)2溶液,其理由是 。
②從環境保護的角度,請你再提出一個優化方案: 。
下面是某病人體檢結果部分記錄表,請分析回答下列問題:
項目 | 測定值 | 正常范圍 |
紅細胞計數 | 413萬個/立方毫米 | 400—550萬個/立方毫米 |
血紅蛋白 | 0.1毫克/立方毫米 | 0.12—0.16毫克/立方毫米 |
白細胞計數 | 11 300個/立方毫米 | 4 000—10 000個/立方毫米 |
嗜中性粒細胞絕對數 | 8 300個/立方毫米 | 2 000—7 500個/立方毫米 |
嗜酸性粒細胞絕對數 | 700個/立方毫米 | 500—2 000個/立方毫米 |
嗜堿性粒細胞絕對數 | 100個/立方毫米 | <700個/立方毫米 |
淋巴細胞絕對數 | 1 800個/立方毫米 | 800—4 000個/立方毫米 |
單核細胞絕對數 | 400個/立方毫米 | 100—1 000個/立方毫米 |
血壓(收縮壓/舒張壓) | 120/75毫米汞柱 | 90—140/60—90 |
毫米汞柱 | 血糖 | 6.5毫摩爾/升 |
(1)這位病人可能患有的疾病是______________、______________、______________。
(2)血紅蛋白的基本組成單位是______________,參與組成血紅蛋白的金屬元素是______________。
(3)可供這位病人選擇的食品有:米飯、面包、雞蛋、牛肉、豬肝、巧克力、西瓜。
結合這位病人的病情,請你為他提供飲食建議:
這位病人應該多吃的食品有______________、______________等。
這位病人盡量少吃的食品有______________、______________等。
(4)木糖醇是一種理想的蔗糖替代品,適合糖尿病患者食用,原因是( )
A.木糖醇不受酵母菌和細菌作用,能防齲齒 B.木糖醇是多羥基化合物,易溶于水
C.木糖醇具有清涼甜味,沒有蔗糖甜 D.木糖醇被食用后不提高血糖濃度
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com