
題目列表(包括答案和解析)
物質的結構可以用不同的方式來表示,如電子式、結構式等。下列結構圖中,●代表原子序數從1到10的元素的原子實(原子實是原子除去最外層電子后剩余的部分),小黑點代表沒有形成共價鍵的最外層電子,短線代表價鍵。示例: 。
。
請用A、B、C、D代表對應的物質填空:
(1)能與 化合形成離子化合物的物質是_________;該離子化合物中存在的微粒間的作用類型有_________(在“①離子鍵、②極性鍵、③配位鍵、④金屬鍵”中選擇)。
化合形成離子化合物的物質是_________;該離子化合物中存在的微粒間的作用類型有_________(在“①離子鍵、②極性鍵、③配位鍵、④金屬鍵”中選擇)。
(2)在空氣中大量存在且又能形成配位化合物的單質是________。
(3)由極性鍵構成的非極性分子是__________
____________。


| 電離能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 500 | 4600 | 6900 | 9500 |
| B | 740 | 1500 | 7700 | 10500 |
| C | 580 | 1800 | 2700 | 11600 |
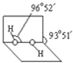 (4)已知過氧化氫分子的空間結構如圖所示,分子中氧原子采取
(4)已知過氧化氫分子的空間結構如圖所示,分子中氧原子采取
【物質結構與性質】
X、Y、Z、W是原子序數依次增大的前四周期元素,已知:
①X元素原子的最外層電子數是次外層的2倍;
②Y元素原子的p軌道上有2個未成對電子;
③Z元素在同一短周期元素中的原子半徑最大;
④W元素原子的最外層電子數與Z相同,其余各電子層均充滿電子。
請回答下列問題:
(1)X、Y、Z三種元素的第一電離能從小到大的順序是 (用元素符號表示,下同);
(2)W元素原子核外電子排布式是 ;
(3)Z元素與氫元素形成的化合物熔點比Y元素的氫化物熔點高,原因是 ;
(4)X的一種氫化物相對分子質量為42,分子中含有σ鍵和π鍵的個數比為8︰1,則該分子中X原子的雜化類型是 和 。
(5)Y的最簡單氫化物可以和W2+形成配位鍵,而X的最簡單氫化物則不行,其原因是 。
(15分)【物質結構與性質】
A、B、C、D為前四周期元素.A元素的原子價電子排布為ns2 np2,B元素原子的最外層鬼子數是其電子層數的3倍,C元素原子的M能層的p能級有3個未成對電子,D元素原子核外的M能層中只有2對成對電子.請回答下列問題:
(1)當n=2時,AB2屬于 分子(填“極性”或“非極性”),分子中有 個δ鍵、 個π鍵. A6H6分子中A原子的雜化軌道類型是 雜化.
(2)當n=3時,A與B形成的晶體屬于 晶體.
(3)若A元素的原子價電子排布為3s23p2,A、C、D三種原子的電負性由大到小的順序是 (用元素符號表示);A、C、D三種元素的第一電離能由大到小的順序是 (用元素符號表示).
(4)已知某紅紫色配合物的組成為CoCl3·5NH3·H2O.該配合物中的中心離子鈷離子
在基態時的核外電子排布式為 .作為配位體之一的NH3分子的空間構型為
(5)金屬鐵的晶體在不同溫度下有兩種堆積方式,晶胞分別如右圖所示,體心立方晶胞和面心立方晶胞中實際含有的Fe原子個數之比為
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com