
題目列表(包括答案和解析)
硫鐵礦又稱黃鐵礦(主要成分FeS2,雜質不含硫元素),是地殼中分布最廣的硫化物。因其淺黃的顏色和明亮的金屬光澤,常被誤認為是黃金,故又稱“愚人金”。
工業上硫鐵礦主要用于接觸法制造硫酸,其反應原理為:
①FeS2與O2高溫下反應生成SO2;
②SO2在催化劑作用下與O2反應生成SO3;
③SO3與H2O反應生成H2SO4.
(1)若1.00噸 SO2與O2的混合氣體中含SO2 0.40噸,在一定條件下發生反應②,有80%的SO2發生轉化,則反應后混合氣體中SO3的質量分數是_________。
(2)現用80噸硫鐵礦制硫酸,最后生產出100噸98%的硫酸。若反應過程中硫元素的損失率為5%,則硫鐵礦中FeS2的質量分數為__________________。
(3)在濃硫酸中繼續溶解SO3后所形成的液體稱發煙硫酸,其濃度通常以游離的SO3含量來表示,如20%的發煙硫酸即表示在硫酸中含有20%的SO3。現有1L含SO330%的發煙硫酸(密度為1.95g/cm3),要把它稀釋成質量分數為95%的濃硫酸,需加水約多少?(寫出計算過程)
(4)已知:850℃~900℃時,硫鐵礦在氧氣中煅燒,可能發生下列反應:
①3FeS2+8O2→Fe3O4+6SO2
②4FeS2+11O2→2Fe2O3+8SO2
為使FeS2煅燒完全生成Fe2O3,工業上使用過量氧氣,當氧氣過量20%時,求所得爐氣中SO2的體積分數。(寫出計算過程)
57.將480 g純凈的FeS2在氧氣中完全反應,若所得固體中n(Fe)∶n(O)=4∶a,此時消耗氧氣b mol,試寫出b與a的關系式_______________________。
硫鐵礦又稱黃鐵礦(主要成分FeS2,雜質不含硫元素),是地殼中分布最廣的硫化物。因其淺黃的顏色和明亮的金屬光澤,常被誤認為是黃金,故又稱“愚人金”。
工業上硫鐵礦主要用于接觸法制造硫酸,其反應原理為:
①FeS2與O2高溫下反應生成SO2;
②SO2在催化劑作用下與O2反應生成SO3;
③SO3與H2O反應生成H2SO4.
(1)若1.00噸 SO2與O2的混合氣體中含SO2 0.40噸,在一定條件下發生反應②,有80%的SO2發生轉化,則反應后混合氣體中SO3的質量分數是_________。
(2)現用80噸硫鐵礦制硫酸,最后生產出100噸98%的硫酸。若反應過程中硫元素的損失率為5%,則硫鐵礦中FeS2的質量分數為__________________。
(3)在濃硫酸中繼續溶解SO3后所形成的液體稱發煙硫酸,其濃度通常以游離的SO3含量來表示,如20%的發煙硫酸即表示在硫酸中含有20%的SO3。現有1L含SO330%的發煙硫酸(密度為1.95g/cm3),要把它稀釋成質量分數為95%的濃硫酸,需加水約多少?(寫出計算過程)
(4)已知:850℃~900℃時,硫鐵礦在氧氣中煅燒,可能發生下列反應:
①3FeS2+8O2→Fe3O4+6SO2
②4FeS2+11O2→2Fe2O3+8SO2
為使FeS2煅燒完全生成Fe2O3,工業上使用過量氧氣,當氧氣過量20%時,求所得爐氣中SO2的體積分數。(寫出計算過程)
57.將480 g純凈的FeS2在氧氣中完全反應,若所得固體中n(Fe)∶n(O)=4∶a,此時消耗氧氣b mol,試寫出b與a的關系式_______________________。
| 元素 | 有關信息 |
| X | 原子半徑為0.074nm,其氫化物的結構模型可表示為: 常溫下是液體 常溫下是液體 |
| Y | 原子半徑為0.102nm,其原子核外電子排布為: |
| Z | 人體中必需微量元素中含量最多,體內缺失會引起貧血 |
| W | 所在主族序數與所在周期序數之差為4 |
(15分)
(1).CO可以和很多過渡金屬形成配合物,如羰基鐵[Fe(CO)5]、羰基鎳[Ni(CO)4]。CO分子中C原子上有一對孤對電子,C、O原子都符合8電子穩定結構,CO的結構式為 ,與CO互為等電子體的離子為 (填化學式)。
(2).人類在使用金屬的歷史進程中,經歷了銅、鐵、鋁之后,第四種將被廣泛應用的金屬被科學家預測是鈦(Ti),它被譽為“未來世紀的金屬”。Ti 元素在元素周期表中的位置是 周期,第 族;其基態原子的價電子層排布為 ;
(3). 在Ti的化合物中,可以呈現+2、+3、+4 三種化合價,其中以+4價的Ti最為穩定。偏鈦酸鋇的熱穩定性好,介電常數高,在小型變壓器、話筒和擴音器中都有應用。偏鈦酸鋇晶體中晶胞的結構示意圖如圖,它的化學式是 ;
(4)已知Ti3+可形成配位數為6的配合物。現有含鈦的兩種顏色的晶體,一種為紫色,另一為綠色,但相關實驗證明,兩種晶體的組成皆為TiCl3·6H2O。為測定這兩種晶體的化學式,設計了如下實驗:
a. 分別取等質量的兩種配合物晶體的樣品配成待測溶液;
b. 分別往待測溶液中滴入AgNO3溶液,均產生白色沉淀;
c. 沉淀完全后分別過濾得兩份沉淀,經洗滌干燥后稱量,發現原綠色晶體的水溶液與AgNO3溶液反應得到的白色沉淀質量為紫色晶體的水溶液反應得到沉淀質量的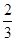 。
。
則綠色晶體配合物的化學式為 ,綠色晶體中含有化學鍵類型是 。
(15分)
(1).CO可以和很多過渡金屬形成配合物,如羰基鐵[Fe(CO)5]、羰基鎳[Ni(CO)4]。CO分子中C原子上有一對孤對電子,C、O原子都符合8電子穩定結構,CO的結構式為 ,與CO互為等電子體的離子為 (填化學式)。
(2).人類在使用金屬的歷史進程中,經歷了銅、鐵、鋁之后,第四種將被廣泛應用的金屬被科學家預測是鈦(Ti),它被譽為“未來世紀的金屬”。Ti 元素在元素周期表中的位置是 周期,第 族;其基態原子的價電子層排布為 ;
(3). 在Ti的化合物中,可以呈現+2、+3、+4 三種化合價,其中以+4價的Ti最為穩定。偏鈦酸鋇的熱穩定性好,介電常數高,在小型變壓器、話筒和擴音器中都有應用。偏鈦酸鋇晶體中晶胞的結構示意圖如圖,它的化學式是 ;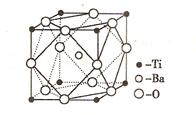
(4)已知Ti3+可形成配位數為6的配合物。現有含鈦的兩種顏色的晶體,一種為紫色,另一為綠色,但相關實驗證明,兩種晶體的組成皆為TiCl3·6H2O。為測定這兩種晶體的化學式,設計了如下實驗:
a. 分別取等質量的兩種配合物晶體的樣品配成待測溶液;
b. 分別往待測溶液中滴入AgNO3溶液,均產生白色沉淀;
c. 沉淀完全后分別過濾得兩份沉淀,經洗滌干燥后稱量,發現原綠色晶體的水溶液與AgNO3溶液反應得到的白色沉淀質量為紫色晶體的水溶液反應得到沉淀質量的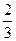 。
。
則綠色晶體配合物的化學式為 ,綠色晶體中含有化學鍵類型是 。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com