
題目列表(包括答案和解析)
(12分)
A.下圖是元素周期表中的前四周期,①~⑨為相應的元素,請從中選擇合適的元素回答問題:
|
| |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ⑨ | |||||||||||||||
(1)根據元素原子的外圍電子排布特征,元素周期表可劃分為五個區域,①元素位于周期表
的 區。
(2)②、⑥兩元素形成的化合物的空間構型為 ,其中心原子的雜化類型為 。
(3)寫出元素⑧基態原子的電子排布式 。
(4)①③兩元素形成的最簡單的化合物與 (寫微粒符號)互為等電子體。
(5)元素⑦與CO可形成的X(CO)5型化合物,該化合物常溫下呈液態,熔點為-20.5℃,沸點為103℃,易溶于非極性溶劑,據此可判斷該化合物晶體屬于___ 晶體(填晶體類型)。
(6)元素⑨的離子的氫氧化物不溶于水,但可溶于氨水中,該離子與NH3間結合的作用力
為 。
(7) 金屬⑦的晶體在不同溫度下有兩種堆積方式,晶胞分 別如右圖所示。 則面心立方晶胞和體心立方晶胞中實際含有的原子個數之比為 。
則面心立方晶胞和體心立方晶胞中實際含有的原子個數之比為 。
B.(12分)乙醇是重要的化工產品和液體燃料,可以利用下列反應制取乙醇
2CO2(g)+6H2(g) ![]() CH3CH2OH(g)+3H2O(g)①,25℃時, K=2.95×1011
CH3CH2OH(g)+3H2O(g)①,25℃時, K=2.95×1011
2CO(g)+4H2(g) ![]() CH3CH2OH(g)+H2O(g)②,25℃時, K=1.71×1022
CH3CH2OH(g)+H2O(g)②,25℃時, K=1.71×1022
(1)寫出反應①的平衡常數表達式K=__________________。
(2)條件相同時,反應①與反應②相比,轉化程度更大的是________。以CO2為原料合成乙醇的優點是 (寫出一條即可)。
 |
根據表中數據分析:
①溫度升高,K值______(填“增大”、“減小”或“不變”)。
②提高氫碳比[ n(H2)/n(CO2)],對生成乙醇 (填“有利”、“不利”)。
 (4)在下圖的坐標中作圖說明壓強變化對反應①的化學平衡的影響。(必須在圖中標明坐標軸所表示的物理量。
(4)在下圖的坐標中作圖說明壓強變化對反應①的化學平衡的影響。(必須在圖中標明坐標軸所表示的物理量。
| A元素的核外電子數和電子層數相等,也是宇宙中最豐富的元素 |
| B元素原子的核外p電子數比s電子數少1 |
| C原子的第一至第四電離能分別是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p軌道全滿或半滿 |
| E元素的主族序數與周期數的差為4 |
| F是前四周期中電負性最小的元素 |
| G在周期表的第八列 |
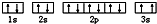 該同學所畫的電子排布圖違背了
該同學所畫的電子排布圖違背了| A元素的核外電子數和電子層數相等,也是宇宙中最豐富的元素 |
| B元素原子的核外p電子數比s電子數少1 |
| C原子的第一至第四電離能分別是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p軌道全滿或半滿 |
| E元素的主族序數與周期數的差為4 |
| F是前四周期中電負性最小的元素 |
| G在周期表的第七列 |


 該同學所畫的電子排布圖違背了
該同學所畫的電子排布圖違背了(15分)現有七種元素,其中A、B、C、D、E為短周期主族元素,F、G為第四周期元素,它們的原子序數依次增大。請根據下列相關信息,回答問題.
| A元素的核外電子數和電子層數相等,也是宇宙中最豐富的元素 |
| B元素原子的核外p電子數比s電子數少1 |
| C原子的第一至第四電離能分別是: I1=738kJ/mol I2 = 1451 kJ/mol I3 = 7733kJ/mol I4 = 10540kJ/mol |
| D原子核外所有p軌道全滿或半滿 |
| E元素的主族序數與周期數的差為4 |
| F是前四周期中電負性最小的元素 |
| G在周期表的第七列 |
⑴已知BA5 為離子化合物,寫出其電子式 .
⑵B基態原子中能量最高的電子,其電子云在空間有 個方向,原子軌道呈 形
⑶某同學根據上述信息,推斷C基態原子的核外電子排布為:
該同學所畫的電子排布圖違背了 .
⑷G位于 族 區,價電子排布式為 .
⑸DE3 中心原子的雜化方式為 ,用價層電子對互斥理論推測其空間構型為 .
⑹檢驗F元素的方法是 ,請用原子結構的知識解釋產生此現象的原因是 .
⑺若某單質晶體中原子的堆積方式如下圖甲所示,其晶胞特征如下圖乙所示,原子之間相互位置關系的平面圖如下圖丙所示。則晶胞中該原子的配位數為 ,該單質晶體中原子的堆積方式為四種基本模式中的 .
(15分)現有七種元素,其中A、B、C、D、E為短周期主族元素,F、G為第四周期元素,它們的原子序數依次增大。請根據下列相關信息,回答問題.
| A元素的核外電子數和電子層數相等,也是宇宙中最豐富的元素 |
| B元素原子的核外p電子數比s電子數少1 |
| C原子的第一至第四電離能分別是: I1=738kJ/mol I2 = 1451 kJ/mol I3 = 7733kJ/mol I4 = 10540kJ/mol |
| D原子核外所有p軌道全滿或半滿 |
| E元素的主族序數與周期數的差為4 |
| F是前四周期中電負性最小的元素 |
| G在周期表的第七列 |
⑴已知BA5 為離子化合物,寫出其電子式 .
⑵B基態原子中能量最高的電子,其電子云在空間有 個方向,原子軌道呈 形
⑶某同學根據上述信息,推斷C基態原子的核外電子排布為:
該同學所畫的電子排布圖違背了 .
⑷G位于 族 區,價電子排布式為 .
⑸DE3 中心原子的雜化方式為 ,用價層電子對互斥理論推測其空間構型為 .
⑹檢驗F元素的方法是 ,請用原子結構的知識解釋產生此現象的原因是 .
⑺若某單質晶體中原子的堆積方式如下圖甲所示,其晶胞特征如下圖乙所示,原子之間相互位置關系的平面圖如下圖丙所示。則晶胞中該原子的配位數為 ,該單質晶體中原子的堆積方式為四種基本模式中的 .
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com