
題目列表(包括答案和解析)
(16分)
㈠、了解一些用藥常識,有利于自我保健。現有下列藥物:碳酸鎂、青霉素、阿司匹林、氫氧化鋁。
①其中屬于解熱鎮痛的藥物是
②青霉素在醫療上的主要作用是
③藥片常用淀粉作為黏合劑,淀粉水解的最終產物是
④OTC表示 (處方藥或非處方藥)
㈡、生活中處處有化學,化學已滲透到我們的“衣、食、住、行”之中。
(1)衣:鑒別真假羊毛衫的方法是先取樣,再 。
(2)食: 合理膳食,保持營養均衡,是青少年學生健康成長的重要保證。
①下列有關維生素和微量元素敘述正確的是 (填字母)
A.人體缺乏維生素A易患壞血病
B.維生素C大量存在于新鮮蔬菜中
C.維生素C屬脂溶性維生素,不易被氧化
D.人體缺碘容易引起甲狀腺腫大
②蛋白質是人體必需的營養物質,它在人體內最終分解為 (填字母)。
A.葡萄糖 B.氨基酸 C.脂肪酸
(3)住:玻璃和鋼鐵是常用的建筑材料:
普通玻璃是由 等物質組成的;
鋼鐵制品不僅可發生化學腐蝕,還能在潮濕的環境中發生 腐蝕。請舉出一種防止鐵制品被腐蝕的方法: 。
(4)行:鋁可用于制造交通工具,鋁制品不易生銹的原因是 ;
橡膠是制造輪胎的重要原料,天然橡膠通過 措施可增大強度和彈性。
㈢、保持潔凈安全的生存環境已成為全人類的共識,人與自然要和諧相處。
①;向煤中加入適量的 ,可以大大減少燃燒產物中SO2的量。
②對汽車加裝尾氣催化凈化裝置,可以使其中的NO、CO相互反應轉化成無毒的氣體,其原理可以用化學方程式表示為 。
| ||
| △ |
| ||
| △ |
| 淀粉酶 |
| 酒化酶 |
 2CH3CHO+2H2O
2CH3CHO+2H2O 2CH3CHO+2H2O
2CH3CHO+2H2O +HO-NO2
+HO-NO2 | 50-60℃ |
| 濃硫酸 |
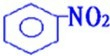 +H2O
+H2O +HO-NO2
+HO-NO2 | 50-60℃ |
| 濃硫酸 |
 +H2O
+H2O

為探究銅與濃硫酸的反應,某興趣小組進行了如下實驗。
【實驗1】銅與濃硫酸反應,實驗裝置如圖所示。
(1)、裝置A中發生反應的化學方程式為:
(2)、熄滅酒精燈后,因為有導管存在,B中的液體不會倒吸,其原因是: 。
拆除裝置前,不打開膠塞,為了使裝置中的殘留氣體完全被吸收,應當采取的操作是: 。
【實驗2】實驗中發現試管內除了產生白色固體外,在銅絲表面還有黑色固體甲生成,甲中可能含有氧化銅、氧化亞銅、硫化銅、硫化亞銅。
查閱資料:
①氧化亞銅在酸性環境下會發生自身氧化還原反應生成Cu2+和銅單質,在空氣中充分煅燒,可以轉化為氧化銅。
②硫化銅和硫化亞銅常溫下都不溶于稀鹽酸,在空氣中充分煅燒,均轉化為氧化銅和二氧化硫。
為了研究甲的成分,該小組同學在收集到足夠量的固體甲后,進行了如下實驗:
(3)、步驟②中檢驗濾渣是否洗滌干凈的實驗方法是: 。
(4)、固體乙在空氣中煅燒時,使用的實驗儀器除了玻璃棒、三腳架、酒精燈外,還必須有:
。
(5)、確定乙是否煅燒完全的操作是: 。
(6)、煅燒過程中一定發生的化學反應方程式為: 。
高氯酸銨(NH4ClO4)是復合火箭推進劑的重要成分,實驗室可通過下列反應制取:
NaClO4(aq)+NH4Cl(aq) NH4ClO4(aq)+NaCl(aq)
(7)、用氨氣和濃鹽酸代替NH4Cl,上述反應不需要外界供熱就能進行,其原因是:
。
(8)、反應得到的混合溶液中NH4ClO4和NaCl的質量分數分別為0.30和0.l5(相關物質的溶解度曲線如下圖)。從混合溶液中獲得較多NH4ClO4晶體的實驗操作依次為(填操作名稱)蒸發濃縮, ,過濾, 、干燥。
為了測定樣品中NH4ClO4的含量,裝置如上圖所示(加熱裝置、儀器固定裝置已略去),實驗步驟如下:

(9)、步驟3中,準確取用24.00 mL H2SO4(aq)的玻璃儀器是 。
(10)、實驗中確保生成的氨被稀硫酸完全吸收的實驗步驟是 (填寫步驟編號)。
(11)、必須重復實驗2~3次,其原因是 。
(12)、如果0.320 g試樣中含NH4ClO4的準確值為0.095g,而實驗測定結果是0.092g 。該實驗
的相對誤差為 。
為探究銅與濃硫酸的反應,某興趣小組進行了如下實驗。
【實驗1】銅與濃硫酸反應,實驗裝置如圖所示。
(1)、裝置A中發生反應的化學方程式為:
(2)、熄滅酒精燈后,因為有導管存在,B中的液體不會倒吸,其原因是: 。
拆除裝置前,不打開膠塞,為了使裝置中的殘留氣體完全被吸收,應當采取的操作是: 。
【實驗2】實驗中發現試管內除了產生白色固體外,在銅絲表面還有黑色固體甲生成,甲中可能含有氧化銅、氧化亞銅、硫化銅、硫化亞銅。
查閱資料:
①氧化亞銅在酸性環境下會發生自身氧化還原反應生成Cu2+和銅單質,在空氣中充分煅燒,可以轉化為氧化銅。
②硫化銅和硫化亞銅常溫下都不溶于稀鹽酸,在空氣中充分煅燒,均轉化為氧化銅和二氧化硫。
為了研究甲的成分,該小組同學在收集到足夠量的固體甲后,進行了如下實驗:
(3)、步驟②中檢驗濾渣是否洗滌干凈的實驗方法是: 。
(4)、固體乙在空氣中煅燒時,使用的實驗儀器除了玻璃棒、三腳架、酒精燈外,還必須有:
。
(5)、確定乙是否煅燒完全的操作是: 。
(6)、煅燒過程中一定發生的化學反應方程式為: 。
高氯酸銨(NH4ClO4)是復合火箭推進劑的重要成分,實驗室可通過下列反應制取:
NaClO4(aq)+NH4Cl(aq) NH4ClO4(aq)+NaCl(aq)
NH4ClO4(aq)+NaCl(aq)
(7)、用氨氣和濃鹽酸代替NH4Cl,上述反應不需要外界供熱就能進行,其原因是:
。
(8)、反應得到的混合溶液中NH4ClO4和NaCl的質量分數分別為0.30和0.l5(相關物質的溶解度曲線如下圖)。從混合溶液中獲得較多NH4ClO4晶體的實驗操作依次為(填操作名稱)蒸發濃縮, ,過濾, 、干燥。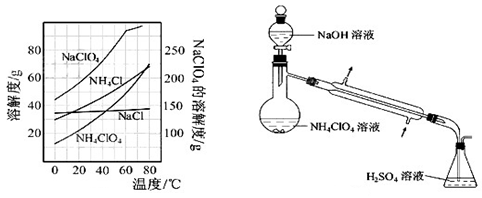
為了測定樣品中NH4ClO4的含量,裝置如上圖所示(加熱裝置、儀器固定裝置已略去),實驗步驟如下:
(9)、步驟3中,準確取用24.00 mL H2SO4(aq)的玻璃儀器是 。
(10)、實驗中確保生成的氨被稀硫酸完全吸收的實驗步驟是 (填寫步驟編號)。
(11)、必須重復實驗2~3次,其原因是 。
(12)、如果0.320 g試樣中含NH4ClO4的準確值為0.095g,而實驗測定結果是0.092g。該實驗
的相對誤差為 。
為探究銅與濃硫酸的反應,某興趣小組進行了如下實驗。
【實驗1】銅與濃硫酸反應,實驗裝置如圖所示。
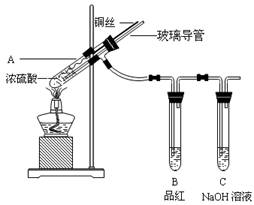
(1)、裝置A中發生反應的化學方程式為:
(2)、熄滅酒精燈后,因為有導管存在,B中的液體不會倒吸,其原因是: 。
拆除裝置前,不打開膠塞,為了使裝置中的殘留氣體完全被吸收,應當采取的操作是: 。
【實驗2】實驗中發現試管內除了產生白色固體外,在銅絲表面還有黑色固體甲生成,甲中可能含有氧化銅、氧化亞銅、硫化銅、硫化亞銅。
查閱資料:
①氧化亞銅在酸性環境下會發生自身氧化還原反應生成Cu2+和銅單質,在空氣中充分煅燒,可以轉化為氧化銅。
②硫化銅和硫化亞銅常溫下都不溶于稀鹽酸,在空氣中充分煅燒,均轉化為氧化銅和二氧化硫。
為了研究甲的成分,該小組同學在收集到足夠量的固體甲后,進行了如下實驗:
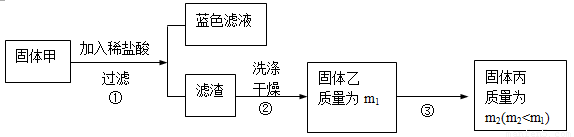
(3)、步驟②中檢驗濾渣是否洗滌干凈的實驗方法是: 。
(4)、固體乙在空氣中煅燒時,使用的實驗儀器除了玻璃棒、三腳架、酒精燈外,還必須有:
。
(5)、確定乙是否煅燒完全的操作是: 。
(6)、煅燒過程中一定發生的化學反應方程式為: 。
高氯酸銨(NH4ClO4)是復合火箭推進劑的重要成分,實驗室可通過下列反應制取:
NaClO4(aq)+NH4Cl(aq)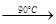 NH4ClO4(aq)+NaCl(aq)
NH4ClO4(aq)+NaCl(aq)
(7)、用氨氣和濃鹽酸代替NH4Cl,上述反應不需要外界供熱就能進行,其原因是:
。
(8)、反應得到的混合溶液中NH4ClO4和NaCl的質量分數分別為0.30和0.l5(相關物質的溶解度曲線如下圖)。從混合溶液中獲得較多NH4ClO4晶體的實驗操作依次為(填操作名稱)蒸發濃縮, ,過濾, 、干燥。
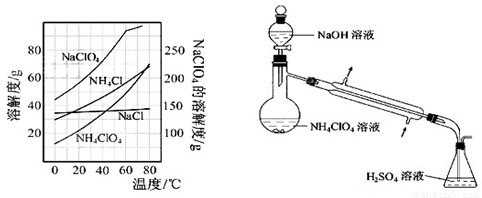
為了測定樣品中NH4ClO4的含量,裝置如上圖所示(加熱裝置、儀器固定裝置已略去),實驗步驟如下:
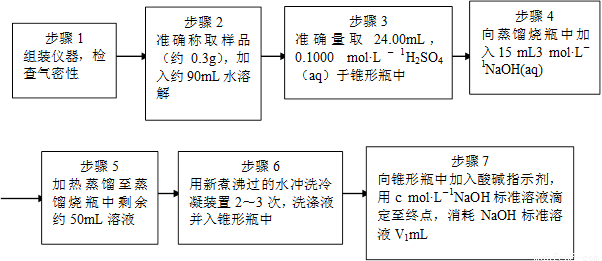
(9)、步驟3中,準確取用24.00 mL H2SO4(aq)的玻璃儀器是 。
(10)、實驗中確保生成的氨被稀硫酸完全吸收的實驗步驟是 (填寫步驟編號)。
(11)、必須重復實驗2~3次,其原因是 。
(12)、如果0.320 g試樣中含NH4ClO4的準確值為0.095g,而實驗測定結果是0.092g 。該實驗
的相對誤差為 。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com