
題目列表(包括答案和解析)
單質硫在KOH的熱溶液中發生岐化反應:3 S + 6 KOH 2 K2S + K2SO3 + 3 H2O
2 K2S + K2SO3 + 3 H2O
若硫過量,進一步生成K2Sx(x ≤ 5)和K2S2O3。將0.08 mol單質硫與含0.06 mol KOH的熱溶液充分反應恰好生成a mol K2Sx和b mol K2S2O3,再加入足量KClO-KOH的混合溶液,硫元素全部轉化為K2SO4,轉移電子n mol。則以下正確的是
A.a = 2b B.x = 2 C.n = 0.48 D.b = 0.02
單質硫在KOH的熱溶液中發生岐化反應:3 S + 6 KOH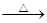 2 K2S + K2SO3 + 3 H2O
2 K2S + K2SO3 + 3 H2O
若硫過量,進一步生成K2Sx(x ≤ 5)和K2S2O3。將0.08 mol單質硫與含0.06 mol KOH的熱溶液充分反應恰好生成a mol K2Sx和b mol K2S2O3,再加入足量KClO-KOH的混合溶液,硫元素全部轉化為K2SO4,轉移電子n mol。則以下正確的是
| A.a = 2b | B.x = 2 | C.n = 0.48 | D.b = 0.02 |
 2 K2S + K2SO3 + 3 H2O
2 K2S + K2SO3 + 3 H2O| A.a = 2b | B.x = 2 | C.n = 0.48 | D.b = 0.02 |
已知Cl-和Ag+反應生成AgCl,每次新生成的AgCl中又有10%見光分解成單質銀和氯氣,氯氣又可在水溶液中岐化成HClO3(為強酸)和HCl。而這樣生成的Cl-又與剩余的Ag+作用生成沉淀,如此循環往復,直至最終。現有含1.1molNaCl的溶液,向其中加入足量AgNO3,求最終能生成多少克難溶物(AgCl和Ag)?若最后溶液體積為1L,求溶液中H+物質的量濃度是多少?
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com