
題目列表(包括答案和解析)
(12分)20 L恒容的密閉容器中,加入3 mol SO3(g)和1 mol氧氣,在某溫度下使其反應,反應至4 min時,氧氣的濃度為0.06mol/L,當反應到8 min時,反應到達平衡。
(1)0 min~4min內生成O2的平均速率:
v(O2)=____________mol/(L·min)。
(2)整個過程中,各物質的濃度與時間關系如下圖所示,則該溫度下的平衡常數K=________________。
(3)若起始時按下表數據投料,相同溫度下達到平衡時,三氧化硫濃度大于0.05 mol/L的是________,此時的平衡常數與(2)小題比較________(填“大于”、“小于”或“等于”)。
|
| A | B | C | D |
| SO3 | 1 mol | 3 mol | 3 mol | 0 mol |
| SO2 | 2 mol | 1.5 mol | 0 mol | 6 mol |
| O2 | 2 mol | 1 mol | 0 mol | 5 mol |
(4)物質的濃度不再改變標志該反應已達平衡,下列還可以說明該反應已達平衡的是________(填序號)。
①體系內壓強不再改變
②容器內氣體的密度不再改變
③混合氣體的平均相對分子質量不再改變
④v正(SO3)=2v逆(O2)
⑤n(SO3)∶n(O2)∶n(SO2)=2∶1∶2
(20分) “酒是陳的香”,就是因為酒在儲存過程中生成了有香味的乙酸乙酯,在實驗室我們也可以用如右圖所示的裝置制取乙酸乙酯。回答下列問題:
(1).寫出制取乙酸乙酯的化學反應方程式
(2).在大試管中配制一定比例的乙醇、乙酸和濃硫酸的混合液的方法是: 。
(3).濃硫酸的作用是:① ;② 。
(4).飽和碳酸鈉溶液的主要作用是 。
(5).裝置中通蒸氣的導管要插在飽和碳酸鈉溶液的液面上,不能插入溶液中,目的是防止 。
(6).若要把制得的乙酸乙酯分離出來,應采用的實驗操作的名稱是 。
(7).做此實驗時,有時還向盛乙酸和乙醇的試管里加入幾塊碎瓷片,其目的是 。
(8).生成乙酸乙酯的反應是可逆反應,反應物不能完全變成生成物,反應一段時間后,就達到了該反應的限度,也即達到化學平衡狀態。下列描述能說明乙醇與乙酸的酯化反應已達到化學平衡狀態的有(填序號) 。
①單位時間里,生成1mol乙酸乙酯,同時生成1mol水
②單位時間里,生成1mol乙酸乙酯,同時生成1mol乙酸
③單位時間里,消耗1mol乙醇,同時消耗1mol乙酸
④正反應的速率與逆反應的速率相等
⑤混合物中各物質的濃度不再變化
⑴20世紀30年代,Eyring和Pzer在碰撞理論的基礎上提出化學反應的過渡態理論:化學反應并不是通過簡單的碰撞就能完成的,而是在反應物到生成物的過程中經過一個高能量的過渡態。如題圖⑴所示是NO2和CO反應生成CO2和NO過程中的能量變化示意圖,說明這個反應是 (填“吸熱”或“放熱”)反應,NO2和CO的總能量 (填“>”、“<”或“=”)CO2和NO的總能量。
⑵某溫度時,在一個2 L的密閉容器中,X、Y、Z三種物質物質的量隨時間的變化曲線如圖⑵所示。根據圖中數據,試填寫下列空白:
①該反應在 min時達到平衡狀態;
②該反應的化學方程式為: ;
⑶一定溫度下,對于反應2A(g) + B(g) 2C(g)在反應過程中C的物質的量n(C)隨著時間變化關系如圖⑶所示,現從t1時間開始對反應體系升高溫度,n(C)的變化如圖qb所示。則:
2C(g)在反應過程中C的物質的量n(C)隨著時間變化關系如圖⑶所示,現從t1時間開始對反應體系升高溫度,n(C)的變化如圖qb所示。則:
①p點時反應的v正 v逆(填“>”、“<”或“=”);
②a,b兩點的正反應速率va vb(填“>”、“<”或“=”)
(12分)20 L恒容的密閉容器中,加入3 mol SO3(g)和1 mol氧氣,在某溫度下使其反應,反應至4 min時,氧氣的濃度為0.06 mol/L,當反應到8 min時,反應到達平衡。
(1)0 min~4 min內生成O2的平均速率:
v(O2)=____________mol/(L·min)。
(2)整個過程中,各物質的濃度與時間關系如下圖所示,則該溫度下的平衡常數K=________________。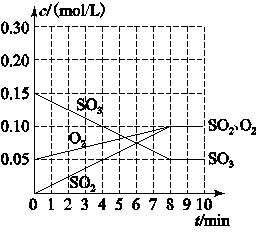
(3)若起始時按下表數據投料,相同溫度下達到平衡時,三氧化硫濃度大于0.05 mol/L的是________,此時的平衡常數與(2)小題比較________(填“大于”、“小于”或“等于”)。
| | A | B | C | D |
| SO3 | 1 mol | 3 mol | 3 mol | 0 mol |
| SO2 | 2 mol | 1.5 mol | 0 mol | 6 mol |
| O2 | 2 mol | 1 mol | 0 mol | 5 mol |
⑴20世紀30年代,Eyring和Pzer在碰撞理論的基礎上提出化學反應的過渡態理論:化學反應并不是通過簡單的碰撞就能完成的,而是在反應物到生成物的過程中經過一個高能量的過渡態。如題圖⑴所示是NO2和CO反應生成CO2和NO過程中的能量變化示意圖,說明這個反應是 (填“吸熱”或“放熱”)反應,NO2和CO的總能量 (填“>”、“<”或“=”)CO2和NO的總能量。

⑵某溫度時,在一個2 L的密閉容器中,X、Y、Z三種物質物質的量隨時間的變化曲線如圖⑵所示。根據圖中數據,試填寫下列空白:
①該反應在 min時達到平衡狀態;
②該反應的化學方程式為: ;
⑶一定溫度下,對于反應2A(g) + B(g) 2C(g)在反應過程中C的物質的量n(C)隨著時間變化關系如圖⑶所示,現從t1時間開始對反應體系升高溫度,n(C)的變化如圖qb所示。則:
2C(g)在反應過程中C的物質的量n(C)隨著時間變化關系如圖⑶所示,現從t1時間開始對反應體系升高溫度,n(C)的變化如圖qb所示。則:
①p點時反應的v正 v逆(填“>”、“<”或“=”);
②a,b兩點的正反應速率va vb(填“>”、“<”或“=”)
一、選擇題(本題包括9小題,每小題3分,共27分。每小題只有一個選項符合題意。)
題號
1
2
3
4
5
6
7
8
9
答案
B
B
A
D
C
C
A
D
B
二、選擇題(本題包括9小題,每小題4分,共36分。每小題有一個或兩個選項符合題意。若正確答案包括兩個選項,只選一個且正確的給2分,但只要選錯一個,該小題就為0分。)
題號
10
11
12
13
14
15
16
17
18
答案
C
C
CD
BD
D
BC
B
BD
AC
三、(本題包括3小題,共34分)
19.(11分)
(1)CO32- + H2O
 HCO3- + OH- (2分)(配平、化學式錯得0分,寫等號扣1分)
HCO3- + OH- (2分)(配平、化學式錯得0分,寫等號扣1分)
(2)不再有氣泡產生(或只有極少量氣泡產生) (1分)
(3)若控制不準確溫度過高Fe2+易被氧化;由于有氫氣生成,明火加熱不安全 (2分)
(兩個方面各占1分)
(4)4Fe2+ + O2 + 4H+ = 4Fe3+ + 2H2O (2分) (化學式錯得0分,配平錯扣1分)
(5)6.6 (2分) (多寫單位g不扣分)
(6)循環使用 (2分)(具體說出如何循環使用同樣得分,意思相近表達欠清晰扣1分)
20.(11分)
(1)2MnO4- + 5H
(化學式錯得0分,配平錯扣1分,漏↑扣1分,扣完為止)
(2)4 (2分)
(3)① 反應開始時:c(KMnO4)= =0.00067 mol?L-1 (1分)
=0.00067 mol?L-1 (1分)
反應時間: =
= =6.7min (1分)
=6.7min (1分)
KMnO4的平均反應速率:
ν(KMnO4)= =
= =1×10-4 mol?L-1?min-1 (1分)
=1×10-4 mol?L-1?min-1 (1分)
(一步完成計算且結果正確得3分,結果錯誤得0分。速率單位錯誤扣1分)
② 否(或:不可行) (1分) 取過量的體積相同、濃度不同的草酸溶液分別同時與體積相同、濃度相同的高錳酸鉀酸性溶液反應。(3分)
(基本思路錯誤得0分,思路正確未強調草酸過量扣1分,未強調體積相同扣1分)
21.(12分)
(1)7 (1分)
實驗操作
預期現象和結論
步驟1:用藥匙取少量白色粉末于試管A底部,點燃酒精燈,充分加熱試管。
(1分)
白色粉末減少,有白煙生成,試管上部有白色固體凝結,說明原白色粉末含有NH4Cl。(2分)
步驟2:用藥匙取少量試管A中的殘留固體于試管B中,滴加適量蒸餾水,振蕩。(1分)
固體溶解得無色溶液。(1分)
步驟3:向試管B中滴加過量的 Ba(NO3)2溶液和1mol?L-1硝酸,充分振蕩后靜置。(2分)
有白色沉淀生成,證明原白色粉末含有 K2SO4。(1分)
步驟4:取試管B中上層清液少量于試管C中,滴加 AgNO3溶液和1mol?L-1硝酸。(2分)
有白色沉淀生成,證明原白色粉末含有NaCl。(1分)
(3)
(NH4Cl的檢驗用NaOH溶液和紅色石蕊試紙同樣得3分;另取樣品溶于水進行K2SO4的檢驗同樣得2分;NaCl的檢驗必須包含有上述4個步驟的操作,共6分(著重號為關鍵點);步驟設計不合理,次序混亂酌情扣分。)
四、(本題包括3小題,共34分)
22.(10分)
(1)①  (1分)
(1分)
② 取形狀大小相同的鎂片和鋁片分別與體積相同、濃度相同的稀鹽酸反應,觀察產生氣泡的快慢 (2分)(操作1分,觀察指標1分。著重號部分缺一處扣1分。用金屬與沸水反應、等濃度鹽溶液堿性比較等合理方法均得分,方案無可行性不給分。)
③ Na2SO3 + SO2 + H2O = 2NaHSO3 (2分)(化學式錯得0分,配平錯扣1分)
有白色膠狀沉淀生成,有無色刺激性氣味氣體產生 (2分)
(各占1分,著重號部分有缺漏合扣1分)
(2)① H2PO4-、HCO3-、HPO42- (2分) ② 強 (1分)
23.(12分)
(1)Ba2+ + SO42- = BaSO4↓ Mg2+ + 2OH- = Mg(OH)2↓
Ca2+ + CO32- = CaCO3↓ Ba2+ + CO32- = BaCO3↓ (4分)
(每個1分。符號錯誤、漏↓得0分)
(2)2NaCl + 2H2O  2NaOH + H2↑+ Cl2↑ (2分)
2NaOH + H2↑+ Cl2↑ (2分)
(化學式錯得0分,配平錯扣1分,漏↑扣1分,漏條件扣1分,扣完為止)
(3)制漂白粉、生產鹽酸、自來水消毒、制高純硅、合成塑料等(任寫2種) (2分)
(寫對1個得1分。答案多于2個的按前2個答案評分。)
(4)蒸發濃縮(1分) 過濾(1分) (多寫冷卻不得分也不扣分)
蒸發過程中溶劑(水)大量減少,Na+濃度顯著增加促進NaCl的沉淀溶解平衡向沉淀方向移動(或:Na+濃度顯著增加抑止了NaCl的溶解) (2分)
(兩個因素各占1分。后者從溶度積角度作答敘述正確也給分。)
24.(12分)
(1)增大 (1分)
(2)向左移 (1分)
 (3)(4分)
(3)(4分)
(各占2分,起點位置、曲線走勢、終點與原曲線的相對高低等只要有一處錯誤則得0分。)
(4)(4分)
0.60(2分)
ν正_>_ν逆(2分)
(5)-787.0 (2分)(不帶負號得0分,有效數字不準確扣1分。)
五、(本題包括1小題,共9分)
 25.(9分)
25.(9分)
(1) (2分)(有錯即得0分)
 |
(2分)(漏系數n扣1分,漏條件不扣分)
 |
(2) (2分)

(3) (2分)
(漏系數2扣1分,不寫條件不扣分)
(4)A、B (2分) (漏選1個扣1分,多選一個也扣1分,扣完為止。)
六、選做題(本題包括2小題,每小題10分。考生只能選做一題)
26.(10分)
 (1)① 碳碳雙鍵、羧基 (2分)(寫對一種得1分,錯別字不給分,多寫一個扣1分)
(1)① 碳碳雙鍵、羧基 (2分)(寫對一種得1分,錯別字不給分,多寫一個扣1分)
② (3分)
(2) (5分)

|