
題目列表(包括答案和解析)
 實驗室用H2O2分解反應(yīng)制取氧氣時,常加入催化劑以加快反應(yīng)速率,某研究性學(xué)習(xí)小組為研究催化劑FeCl3的量對O2生成速率的影響,設(shè)計了如下三組實驗方案(見下表),將表中所給的試劑按一定體積混合后進行反應(yīng).
實驗室用H2O2分解反應(yīng)制取氧氣時,常加入催化劑以加快反應(yīng)速率,某研究性學(xué)習(xí)小組為研究催化劑FeCl3的量對O2生成速率的影響,設(shè)計了如下三組實驗方案(見下表),將表中所給的試劑按一定體積混合后進行反應(yīng).| 實驗編號 試劑 |
A | B | C |
| 10% H2O2/mL | 20.0 | V1 | V2 |
| 2mol/L FeCl3/mL | 0 | 5.0 | 10.0 |
| H2O/mL | V3 | V4 | 0 |
(9分)實驗室用H2O2分解反應(yīng)制取氧氣時,常加入催化劑以加快反應(yīng)速率,某研究性學(xué)習(xí)小組為研究催化劑FeCl3的量對O2生成速率的影響,設(shè)計了如下三組實驗方案(見下表),將表中所給的試劑按一定體積混合后進行反應(yīng)。
| 實驗編號 試劑 | A | B | C |
| 10% H2O2/mL | 20.0 | V1 | V2 |
| 2mol/L FeCl3/ mL | 0 | 5.0 | 10.0 |
| H2O/ mL | V3 | V4 | 0 |

(9分)實驗室用H2O2分解反應(yīng)制取氧氣時,常加入催化劑以加快反應(yīng)速率,某研究性學(xué)習(xí)小組為研究催化劑FeCl3的量對O2生成速率的影響,設(shè)計了如下三組實驗方案(見下表),將表中所給的試劑按一定體積混合后進行反應(yīng)。
| 實驗編號 試劑 | A | B | C |
| 10% H2O2/mL | 20.0 | V1 | V2 |
| 2mol/L FeCl3/ mL | 0 | 5.0 | 10.0 |
| H2O/ mL | V3 | V4 | 0 |
按要求回答下列問題:
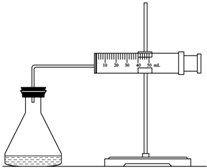
(1)欲用右圖裝置來比較該反應(yīng)的反應(yīng)速率快慢,當(dāng)反應(yīng)物的濃度、用量及其他影響速率的條件確定之后,可以通過測 推(計)算反應(yīng)速率。
(2)為實現(xiàn)實驗?zāi)康模瑒tV1= ,V2= ;
V3= ,V4= 。
(3)根據(jù)你所掌握的知識判斷,在上述實驗中反應(yīng)速率最快的可能是 (填“實驗編號”)
(4)已知Fe3+催化H2O2分解的機理可分兩步反應(yīng)進行,其中第一步反應(yīng)為:2Fe3+ + H2O2 ==2Fe2++ O2↑+ 2H+,則第二步反應(yīng)的離子方程式為:
。
【解析】(1)因為反應(yīng)中生成氧氣,所以可以通過收集相同體積的氣體所需要的時間來進行計算。
(2)為使實驗在相同條件下進行雙氧水的量應(yīng)該相同,且最終溶液的體積要相同,所以V1=20.00ml,V2=20.00ml,V3=10.00ml,V4=5.00ml。
(3)C中催化劑的量最多,所以反應(yīng)速率可能最快。
(4)因為催化劑在反應(yīng)前后是不能變的,所以在第二步中亞鐵離子要重新生成鐵離子,因此正確的反應(yīng)式為2Fe2+ + H2O2 +2H+ == 2Fe3+ + 2H2O。
(9分)實驗室用H2O2分解反應(yīng)制取氧氣時,常加入催化劑以加快反應(yīng)速率,某研究性學(xué)習(xí)小組為研究催化劑FeCl3的量對O2生成速率的影響,設(shè)計了如下三組實驗方案(見下表),將表中所給的試劑按一定體積混合后進行反應(yīng)。
|
實驗編號 試劑 |
A |
B |
C |
|
10% H2O2/mL |
20.0 |
V1 |
V2 |
|
2mol/L FeCl3/ mL |
0 |
5.0 |
10.0 |
|
H2O/ mL |
V3 |
V4 |
0 |
按要求回答下列問題:
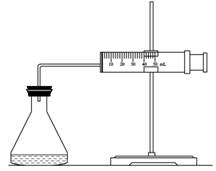
(1)欲用右圖裝置來比較該反應(yīng)的反應(yīng)速率快慢,當(dāng)反應(yīng)物的濃度、用量及其他影響速率的條件確定之后,可以通過測 推(計)算反應(yīng)速率。
(2)為實現(xiàn)實驗?zāi)康模瑒tV1= ,V2= ;
V3= ,V4= 。
(3)根據(jù)你所掌握的知識判斷,在上述實驗中反應(yīng)速率最快的可能是 (填“實驗編號”)
(4)已知Fe3+催化H2O2分解的機理可分兩步反應(yīng)進行,其中第一步反應(yīng)為:2Fe3+ + H2O2 ==2Fe2+ + O2↑+ 2H+,則第二步反應(yīng)的離子方程式為:
。
【解析】(1)因為反應(yīng)中生成氧氣,所以可以通過收集相同體積的氣體所需要的時間來進行計算。
(2)為使實驗在相同條件下進行雙氧水的量應(yīng)該相同,且最終溶液的體積要相同,所以V1=20.00ml,V2=20.00ml,V3=10.00ml,V4=5.00ml。
(3)C中催化劑的量最多,所以反應(yīng)速率可能最快。
(4)因為催化劑在反應(yīng)前后是不能變的,所以在第二步中亞鐵離子要重新生成鐵離子,因此正確的反應(yīng)式為2Fe2+ + H2O2 + 2H+ == 2Fe3+ + 2H2O。
| 實驗編號 試劑 | A | B | C |
| 10% H2O2/mL | 20.0 | V1 | V2 |
| 2mol/L FeCl3/ mL | 0 | 5.0 | 10.0 |
| H2O/ mL | V3 | V4 | 0 |
一、1.B 2.A?
3.解析:v(NH3)∶v(O2)∶v(NO)∶v(H2O)=4∶5∶4∶6。
答案:D?
4.BC 5.B 6.B 7.D 8.BD?
9.解析:由①②組數(shù)據(jù)解得m=1,由②③組數(shù)據(jù)解得n=58個考點名師精講[整理51套]/考點27化學(xué)反應(yīng)速率.files/image056.gif) 。
。
答案:D
二、10.(1)0.013 (2)1.0 催化劑 (3)> >
(4)吸熱 溫度升高時,平衡向右移動?
11.①
12.④>③=②>①?
13.58個考點名師精講[整理51套]/考點27化學(xué)反應(yīng)速率.files/image062.gif)
58個考點名師精講[整理51套]/考點27化學(xué)反應(yīng)速率.files/image064.gif) (
(58個考點名師精講[整理51套]/考點27化學(xué)反應(yīng)速率.files/image066.gif) -x)?mol?L-1?min-1
-x)?mol?L-1?min-1
14.(1)1∶50 根據(jù)勒夏特列原理,通入過量而廉價的氧氣,可提高SO2的轉(zhuǎn)化率
(2)廢氣中每小時排出的SO2的體積為:1
(3)SO2 ~ 2NH3 ~ (NH4)2SO4?
58個考點名師精講[整理51套]/考點27化學(xué)反應(yīng)速率.files/image068.gif) mol?
mol?
58個考點名師精講[整理51套]/考點27化學(xué)反應(yīng)速率.files/image070.gif) mol
mol
58個考點名師精講[整理51套]/考點27化學(xué)反應(yīng)速率.files/image072.gif) mol
mol
故可得(NH4)2SO4:58個考點名師精講[整理51套]/考點27化學(xué)反應(yīng)速率.files/image072.gif) mol×1
mol×1
消耗氨氣:58個考點名師精講[整理51套]/考點27化學(xué)反應(yīng)速率.files/image072.gif) mol×2×1
mol×2×1
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com