
題目列表(包括答案和解析)
1(11分) 按要求填空:
(1) 含有18種元素的周期是第____________周期。
(2) 周期表中最活潑的金屬元素位于第_____________縱行。
(3) 寫出分子具有雙核18電子的物質與水反應的化學方程式
_______________________________________________________________________。
(4) 周期表前20號元素中,某兩種元素的原子序數相差3,周期數相差1,它們形成化合物時原子數之比為1∶2。寫出這些化合物的化學式:(至少寫4種)_______________。
 M、N、X、Y四種主族元素在周期表里的相對位置如圖所示,已知它們的原子序數總和為46.
M、N、X、Y四種主族元素在周期表里的相對位置如圖所示,已知它們的原子序數總和為46.

| ||
| ||
| 質子數 | 16 | 16 | 16 |
| 電子數 | 16 | 17 | 18 |
| 化學式 |
A、B、C、D、E、F六種短周期主族元素,其核電荷數依次增大,已知元素A和C可形成兩種常溫下均為液體的化合物,B原子最外層電子數是最內層電子數的兩倍,A與D、C與F分別處于同一主族且A、D質子數之和是C、F質子數之和的一半,18gE與足量鹽酸反應生成標準狀況下的H222.4L。
請按要求回答:
(1)由A、C、D三種元素形成的化合物X中含有的化學鍵類型為_______。
(2)A、D、F三種元素形成的化合物Y溶液中的微粒濃度之間存在如下關系(請填寫下式中的空白,每空只填一種微粒濃度的符號)。
c(H+)+_______:c(OH―)+ _______。
(3)E、F構成的化合物能與水反應,寫出化學方程式_______。
(4)①寫出單質D與乙醇反應的化學方程式_______。
②A、B、C三種元素可以形成最簡式為A4B2C的有機物,該有機物與足量X水溶液反應得到的兩種產物中含有相同數目的B原子。寫出該反應的化學方程式_____。
(5)A和B組成的化合物M,每個分子中含有18個電子,常溫常壓下,0.5molM完全燃燒放出780kJ的熱量,請寫出表示M完全燃燒的熱化學方程式____。
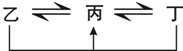 有A、B、C、D、E、F六種前四周期的元素,原子序數依次增大,A、B、C、D、E均為短周期元素,D和F元素對應的單質為日常生活中常見金屬.A原子核內只有一個質子,元素A與B形成的氣態化合物甲具有10e-、空間構型為三角錐形,C元素原子的最外層電子數是其電子層數的3倍,C與E同主族.圖中均含D或F元素的物質均會有圖示轉化關系:
有A、B、C、D、E、F六種前四周期的元素,原子序數依次增大,A、B、C、D、E均為短周期元素,D和F元素對應的單質為日常生活中常見金屬.A原子核內只有一個質子,元素A與B形成的氣態化合物甲具有10e-、空間構型為三角錐形,C元素原子的最外層電子數是其電子層數的3倍,C與E同主族.圖中均含D或F元素的物質均會有圖示轉化關系:(12分)有A、B、C、D、E、F六種前四周期的元素,原子序數依次增大,A、B、C、D、E均為短周期元素,D和F元素對應的單質為日常生活中常見金屬。A原子核內只有一個質子,元素A與B形成的氣態化合物甲具有10e-、空間構型為三角錐形,C元素原子的最外層電子數是其電子層數的3倍,C與E同主族。下圖中均含D或F元素的物質均會有圖示轉化關系:
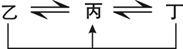
①均含D元素的乙、丙、丁微粒間的轉化全為非氧化還原反應;
②均含F元素的乙(單質)、丙、丁微粒間的轉化全為氧化還原反應。請回答下列問題:
(1)化合物甲的電子式為 。
(2)F元素在周期表中的位置 ;穩定性:A2C A2E(填“大于”“小于” “等于”)。
(3)均含有D元素的乙與丁在溶液中發生反應的離子方程式 。
(4)丙、丁分別是含F元素的簡單陽離子,檢驗含丙、丁兩種離子的混合溶液中的低價離子,可以用酸性KMnO4溶液,其對應的離子方程式為:
(5)已知常溫下化合物FE的Ksp=6×10-18 mol2·L-2,常溫下將1.0×10-5mol·L-1的Na2E溶液與含FSO4溶液按體積比3 :2混合,若有沉淀F E生成,則所需的FSO4的濃度要求 。(忽略混合后溶液的體積變化)。
一、單項選擇題(本題包括12小題,每小題4分,共48分。每小題只有一個選項符合題意)
題號
1
2
3
4
5
6
7
8
9
10
答案
D
B
D
A
B
A
C
B
D
C

 22.(14分)
(1) O、H、S、Cl 硫酸(4分)
22.(14分)
(1) O、H、S、Cl 硫酸(4分)
(2) (3分)
(3) SO2 + 2H2O + Cl2 = 4H++ SO42-+ 2Cl-(3分)
SO2和Cl2按相等物質的量通入品紅溶液(2分)
(4) Fe + S
 FeS,2Fe + 3Cl2
FeS,2Fe + 3Cl2
 2FeCl3(或Cl2 +
H2S = S↓+ 2HCl
2FeCl3(或Cl2 +
H2S = S↓+ 2HCl
或Cl2 + Na2S S↓+ 2NaCl)(2分)
四、實驗題(本大題共2小題,共21分)
23.(5分)
(1)同周期
(2)同主族
Ⅰ
A、F、H
E、D
Ⅱ
d、c、b
g、f
24.(16分) (1) 分液漏斗上口的塞子未打開(或漏斗未與大氣相通或漏斗塞子的凹槽未與頸部的通氣孔對準。(2分)
(2) ④ (2分)
(3) 溶液由紅色褪為無色,SO2 + OH- = HSO3-或SO2 + 2OH-= SO32-+ H2O。 (4分)
(4) 產生白色沉淀,SO2被HNO3氧化產生SO42-,與Ba2+產生白色沉淀。(4分)
(5) ① 關閉K2,在燒杯中用水封住玻璃導管口,用手捂住集氣瓶b,燒杯中導管口有氣泡產生,松手后,導管內有一段液柱保持不降則氣密性好。(2分)
② 打開K1,關閉K2,點燃酒精燈。(2分)
五、計算題(本大題共1個小題,共11分)
25.(1) S H2S Na2S2O3 + H2SO4 = Na2SO4 + SO2 + S↓+ H2O
Na2S + H2SO4 = Na2SO4 + H2S↑ 2H2S+SO2=3S↓+2H2O(各1分)
(2) Na2S2O3 :0.025 mol Na2S:0.075 mol(各3分)
本資料由《七彩教育網》www.7caiedu.cn 提供!
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com