
題目列表(包括答案和解析)
(6分)下列說法正確的是 (填序號)。
①由于碘在酒精中的溶解度大,所以可用酒精將碘水中的碘萃取出來
②水的沸點是100℃,酒精的沸點是78.5℃,用直接蒸餾法能使含水酒精變為無水酒精
③由于膠粒的直徑比離子大,所以淀粉溶液中混有的碘化鉀可用滲析法分離
④分離苯和苯酚的混合液,先加入適量濃溴水,再過濾、分液,即可實現
⑤由于高級脂肪酸鈉鹽在水中的分散質微粒直徑在1nm~100 nm之間,所以可用食鹽使高級脂肪酸納從皂化反應后的混合物中析出
⑥不慎把苯酚溶液沾到皮膚上,應立即用酒精洗滌
⑦用稀溴水滴入苯酚溶液中制備2,4,6-三溴苯酚
⑧實驗室使用體積比為1:3的濃硫酸與乙醇的混合溶液制乙烯時,為防加熱時反應混合液出現暴沸現象,除了要加沸石外,還應注意緩慢加熱讓溫度慢慢升至170℃
17..(18分)某化學小組采用類似制乙酸乙酯的裝置(如右圖),以環己醇制備環己烯:
 已知:
已知:
| 密度 | 熔點 | 沸點 | 溶解性 | |
| 環己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 環己烯 | 0.81 | -103 | 83 | 難溶于水 |
(1)制備粗品
將12.5mL環己醇加入試管A中,再加入1mL濃硫酸,搖勻后放入碎瓷片,緩慢加熱至反應完全,在試管C內得到環己烯粗品。
①A中碎瓷片的作用是 ,
導管B除了導氣外還具有的作用是 。
②試管C置于冰水浴中的目的是 。
 (2)制備精品
(2)制備精品
①環己烯粗品中含有環己醇和少量酸性雜質等。加入飽和
食鹽水,振蕩、靜置、分層,環己烯在 層(填
“上”或“下”),分液后用 (填入編號)洗滌。
A.KMnO4溶液 B.稀H2SO4 C.Na2CO3溶液
②再將環己烯按右圖裝置蒸餾,冷卻水從 口進入。
蒸餾時要加入生石灰,目的是: 。
③收集產品時,控制的溫度應在 左右,實驗制得的環己烯精品質量低于理論產量,可能的原因是 ( )
A.蒸餾時從70℃開始收集產品 B.環己醇實際用量多了
C.制備粗品時環己醇隨產品一起蒸出
(3)以下區分環己烯精品和粗品的方法,合理的是 ( )
A.用酸性高錳酸鉀溶液 B.用金屬鈉 C.測定沸點
18.(12分)有機
物A的結構簡式為![]() ,它可通過不同化學反應分別制得B、C、D和E四種物質。
,它可通過不同化學反應分別制得B、C、D和E四種物質。

請回答下列問題:
(1)指出反應的類型:A→C: 。
(2)在A~E五種物質中,互為同分異構體的是 (填代號)。
(3)寫出由A生成B的化學方程式
。
(4)已知HCHO分子中所有原子都在同一平面內,則在上述分子中所有的原子有可能都在同一平面的物質是 (填序號)。
(5)C能形成高聚物,該高聚物的結構簡式為 。
(6)寫出D與NaOH溶液共熱反應的化學方程式
。
19.(16分)肉
桂酸甲酯( )常用于調制具有草莓、葡萄、櫻桃、香子蘭等香味的食用香精
)常用于調制具有草莓、葡萄、櫻桃、香子蘭等香味的食用香精
⑴肉桂酸甲酯的分子式是 ;
 ⑵下列有關肉桂酸甲酯的敘述中,正確的是 填字母);
⑵下列有關肉桂酸甲酯的敘述中,正確的是 填字母);
A.能與溴的四氯化碳溶液發生加成反應
B.無法使酸性高錳酸鉀溶液褪色
C.在堿性條件下能發生水解反應
D.不可能發生加聚反應
⑶G為肉桂酸甲酯的一種同分異構體,其分子結構模型如右圖所示(圖中球與球之間連線表示單鍵或雙鍵)。則G的結構簡式為 ;
⑷用芳香烴A為原料合成G的路線如下:

①化合物E中的官能團有 (填名稱)。
②F→G的反應類型是 ,該反應的化學方程式為 _ _ 。
③C→D的化學方程式為 _。
④寫出符合下列條件的F的同分異構體的結構簡式 。O%M
ⅰ.分子內含苯環,且苯環上只有一個支鏈;
ⅱ.一定條件下,1mol該物質與足量銀氨溶液充分反應,生成4mol銀單質。
20.(10分)有機物A的蒸汽對同溫同壓下氫氣的相對密度為31,取3.1克A物質在足量氧氣中充分燃燒,只生成2.7克水和標準狀況下CO22.24L,求有機物的分子式;若該有機物0.2mol恰好與9.2克金屬鈉完全反應,請寫出有機物的結構簡式并命名。
室安卡因(G)是一種抗心律失常藥物,可由下列路線合成:

(1)已知A是 的單體,則A中所含官能團的名稱是
。
的單體,則A中所含官能團的名稱是
。
(2)F→G的反應類型是 。
(3)下列關于室安卡因(G)說法不正確的是 (填字母編號)。
a.屬于氨基酸 b.能發生加成反應
c.能使酸性高錳酸鉀溶液退色 d.其苯環上的一氯代物只有兩種
(4)H是C的同系物,其核磁共振氫譜圖中有兩個峰,它的相對分子質量為167,則H的結構簡式為 。
(5)寫出C與足量NaOH醇溶液共熱時反應的化學方程式:
。
室安卡因(G)是一種抗心律失常藥物,可由下列路線合成: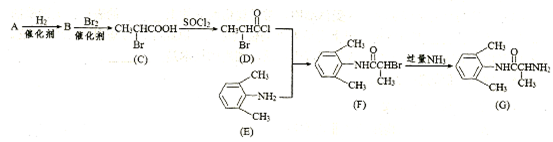
(1)已知A是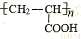 的單體,則A中所含官能團的名稱是 。
的單體,則A中所含官能團的名稱是 。
(2)F→G的反應類型是 。
(3)下列關于室安卡因(G)說法不正確的是 (填字母編號)。
a.屬于氨基酸 b.能發生加成反應
c.能使酸性高錳酸鉀溶液退色 d.其苯環上的一氯代物只有兩種
(4)H是C的同系物,其核磁共振氫譜圖中有兩個峰,它的相對分子質量為167,則H的結構簡式為 。
(5)寫出C與足量NaOH醇溶液共熱時反應的化學方程式:
。
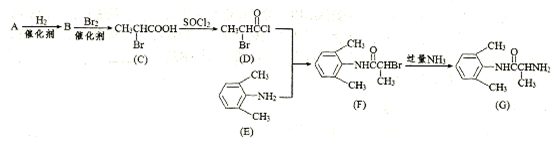
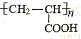 的單體,則A中所含官能團的名稱是 。
的單體,則A中所含官能團的名稱是 。某一容積可變的密閉體系中發生下列反應:N2(g) + 3H2(g) ![]() 2NH3(g) + Q(Q>0),回答下列問題:
2NH3(g) + Q(Q>0),回答下列問題:
(1)對于合成氨工業生產條件的選擇,下列說法正確的是(選填字母序號) ;
A.溫度、壓強越大,越有利于化學平衡的正向移動;
B.鐵觸媒在該溫度時活性大;
C.工業生產受動力、材料、設備等條件的限制;
D.使用催化劑有利于提高反應的轉化率。
(2)下圖是某一時間段中反應速率與反應進程的關系圖:

①處于平衡狀態的時間段是 。
②在t1、t3、t4時刻,體系中分別是何種條件發生了什么樣變化?
t1: ,t3: , t4: 。
③在下列時間段中,氨的百分含量最高的是 (選填代號)。
a.t0~t1 b.t2~t3 c.t3~t4 d.t5~t6
二、選擇題(48分)
13.C 14.ACD 15.AC 16.B 17.A 18.D
三、實驗題(17分)
19、實驗題
 ?)(8分)
?)(8分)
 (5分)
(5分)
連線如圖(連線正確給3分,有任何錯誤不給這3分)
?)(9分)
(1) ② (2分) ③
(2分) ③ (2分) ④斜面傾角(或填h的數值)(2分)
(2分) ④斜面傾角(或填h的數值)(2分)
(2) 不能(3分)
20.
(1)由前三列數據可知物體在斜面上勻加速下滑時的加速度為a1==5m/s2,mg sin a=ma1,可得:a=30°,
(2)由后二列數據可知物體在水平面上勻減速滑行時的加速度大小為a2==2m/s2,mmg=ma2,可得:m=0.2,
(3)由2+5t=1.1+2(0.8-t),解得t=0.1s,即物體在斜面上下滑的時間為0.5s。
21.(18分)(1)設ab上產生的感應電動勢為E,回路中電流為I,ab運動距離s所用的時間為t,則有:E=BLv I= t= Q=I2(4R)t 由上述方程得:v=
(2)設電容器兩極板間的電勢差為U,則有:U=IR
電容器所帶電荷量q=CU 解得q=
22.(1)洛侖茲力不做功,由動能定理得,mgy= mv2
mv2 ……①
……①
得 v=
 ……②
……②
(2)設在最大距離ym處的速率為vm,根據圓周運動有,qvmB-mg=m ……③
……③
且由②知 
 ……④
……④
 由③④及R=2ym得
由③④及R=2ym得  ……⑤
……⑤
(3)小球運動如圖所示,當它運動到最高點時速度最大,設為vm,此時小球在最高點的曲率半徑也為該點到x軸距離的2倍,
由動能定理
(qE-mg)|ym|= ……⑥
……⑥
由圓周運動 qvmB+mg-qE=m ……⑦
……⑦
qE =2mg ……⑧
且由⑥⑦⑧及R=2|ym|解得vm=
28. D ③ 29. A ①
化學參考答案
一、選擇題:(本題包括7小題,每題只有一個選項符合題意,每題6分,共42分)
6
7
8
9
10
11
12
C
B
A
D
C
B
C
二、(本題包括3小題,共35分)
23、(1)H2O2=HO2―+H+
(2)O2+2H2O+4e―→4OH―
(3)0.5mol
(4)2A1+2OH―+6H2O=2[A1(OH)4]―+3H2↑
(5)10―10mol?L―1c(NO3―)>c(NH4+)>c(H+)>c(OH―)
24(共16分,每空2分)
(1)否 硫酸溶質質量分數為23%<60%,其氧化性不突出所以無明顯現象
(2)銅片慢慢溶解,帶支管的試管中溶液漸成藍色小試管中品紅褪色。
化學方程式為:Cu+2H2SO4 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(3)現象是: ①液體呈淺藍色,原因是溶液中含有Cu2+;②有白色固體在試管底部析出,
原因是:98%濃H2SO4有吸水性只剩無水CuSO4。
操作是:帶支管的試管中的溶液冷卻后沿燒杯壁緩緩加入到水中,并不斷用玻璃棒拌。
25.(1)① ,減小 ② 200℃,100
MPa 200℃時反應速率過低,壓強過大對設備要求過高 ③B
(2)2NH3+60H--6e-=N2+6H2O 堿性 NH3在酸性介質中易轉化為NH4+離子
,減小 ② 200℃,100
MPa 200℃時反應速率過低,壓強過大對設備要求過高 ③B
(2)2NH3+60H--6e-=N2+6H2O 堿性 NH3在酸性介質中易轉化為NH4+離子
【物質結構】
⑴第三周期 ⅦA 1s22s22p63s23p4 ⑵2Na+2H2O=2NaOH+H2↑ 大于
⑶大 SiO2是原子晶體或 小 CO2是分子晶體 (合理即給分)
⑷Cl高氯酸的酸性大于硫酸的酸性或氯化氫穩定比硫化氫強(合理即給分)
【有機化學】
(1)C4H6O5 羥基,羥基
|