
題目列表(包括答案和解析)
|
3.6 g CO和H2組成的混合氣體與足量氧氣充分燃燒后,立即將全部燃燒產物通過足量Na2O2固體,固體質量增加 | |
| [ ] | |
A. |
2.1 g |
B. |
3.6 g |
C. |
7.2 g |
D. |
8.4 g |
(1)m g鐵屑與含有n g HNO3的溶液完全反應,若m∶n=1∶2.7,該反應的化學方程式為________.(假設還原產物只生成一種鹽)
(2)含n g HNO3的稀溶液,恰好使5.6g鐵粉完全溶解,若有n/4g HNO3被還原成NO(無其他還原產物)則n值不可能是
[ ]
(3)某條件下鋅和硝酸反應時的物質的量之比為2∶5,此時硝酸的還原產物是________.
|
將7 g某銅、銀合金與足量的a mol/L的HNO3充分反應,完全溶解后放出的氣體與標準狀況下的氧氣0.56 L混合,通入水中恰好完全被吸收,則此合金中銅的質量是 | |
| [ ] | |
A. |
1.6 g |
B. |
2.4 g |
C. |
3.2 g |
D. |
4.8 g |
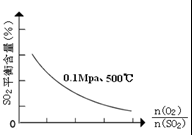 (1)在一定條件下,在一容積可變的密閉容器中,將SO2和O2混合發生反應:
(1)在一定條件下,在一容積可變的密閉容器中,將SO2和O2混合發生反應:| 催化劑 |
| △ |
| 時間min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| n(SO2) | 2.00 | 1.92 | 1.84 | 1.76 | 1.76 | 1.64 | 1.52 | 1.40 | 1.40 | 1.40 |
| n(O2) | 1.00 | 0.96 | 0.92 | 0.88 | 0.88 | 0.82 | 0.76 | 0.70 | 0.70 | 0.70 |
| n(SO3) | 0 | 0.08 | 0.16 | 0.24 | 0.24 | 0.36 | 0.48 | 0.60 | 0.60 | 0.60 |
| n(O2) |
| n(SO2) |
| n(O2) |
| n(sO2) |
(14分)I. A~J分別表示中學化學中常見的一種物質,它們之間相互關系如下圖所示(部分反應物、生成物沒有列出),且已知G為主族元素的固態氧化物,A、B、C、D、E、 F六種物質中均含同一種元素。請填寫下列空白:
(1)A、B、C、D、E、F六種物質中含有的同一種元素在周期表中位置 ,
(2)寫出反應④的離子方程式 。
(3)若向氣體K的水溶液中加入鹽酸,使其恰好完全反應,所得溶液的
pH 7 (填“>”、“<”或“=”),用離子方程式表示其原因: 。
II.電浮選凝聚法是工業上采用的一種污水處理方法:保持污水的pH在5.0~6.0之間,通過電解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉積下來,具有凈化水的作用。陰極產生的氣泡把污水中懸浮物帶到水面形成浮渣層,刮去(或撇掉)浮渣層,即起到了浮選凈化的作用。某科研小組用電浮選凝聚法處理污水,設計裝置如圖所示:
(1)電解池陽極的電極反應分別是
① ; ②。
(2)熔融鹽燃料電池是以熔融碳酸鹽為電解質,以CH4為燃料,空氣為氧化劑,稀土金屬材料為電極。已知負極的電極反應是。
①正極的電極反應是 。
②為了使該燃料電池長時間穩定運行,電池的電解質組成應保持穩定。為此電池工作時必須有部分A物質參加循環。則A物質的化學式是 。
(3)實驗過程中,若在陰極產生了44.8 L(標準狀況)氣體,則熔融鹽燃料電池消耗CH4(標準狀況) L。
一、單項選擇題(本題包括8小題,每小題3分,共24分。每小題只有一個選項符合題意)
1.A 2.C 3.B 4.D 5.C 6.D 7.C 8.B
二、不定項選擇題(本題包括6小題,每小題4分,共24分。每小題有一個或兩個選項符合題意。若正確答案只包括一個選項,多選時,該題為0分;若正確答案包括兩個選項,只選一個且正確的給2分,選兩個且都正確的給4分,但只要選錯一個,該小題就為0分。)
9.AC 10.BD 11.B 12.AB 13.D 14.B
三、非選擇題(共7小題,72分)
15.⑴ CaCO3+2H+=Ca2++H2O+CO2↑ 除去碳酸鈣等不溶性雜質
⑵ 檢驗HCO3―離子 另取一份濾液,加入NaOH溶液,觀察有無沉淀產生
⑶ 同時將濾液和飽和氯水滴在有色布條上,比較有色布條褪色的快慢
(每空2分,共10分)
16.⑴NaOH溶液和稀硫酸 ⑵在隔絕空氣的條件下,蒸發濃縮、冷卻結晶 將濾渣F在空氣中灼燒 ⑶由濾液A制得氯化鋁溶液不合理,所得氯化鋁溶液中含有大量NaCl雜質 向濾液A中通入足量的CO2生成Al(OH)3沉淀,過濾,向Al(OH)3沉淀中加入鹽酸至沉淀溶解
(每空2分,共10分)
17.⑴CuSO4 ⑵燒杯中有硫酸,黑色固體不溶于硫酸 ⑶①CuS+8HNO3=CuSO4+8NO2↑+4H2O ②所得溶液為藍色,加BaCl2溶液后有白色沉淀生成 ③將黑色固體在空氣中灼燒,比較反應前后固體的質量
(每空2分,共10分)
18.⑴保護臭氧層
⑵①2KHCO3 K2CO3+CO2↑+H2O
K2CO3+CO2↑+H2O
②CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH=-49.47kJ/mol
CH3OH(g)+H2O(g) ΔH=-49.47kJ/mol
⑶Ba(OH)2(或NaOH溶液和BaCl2溶液) 實驗時的溫度、壓強,沉淀的質量
(每空2分,共10分)
19.⑴Na+[ ]2-Na+ ⑵白色物質迅速變為灰綠色,最終變為紅褐色
]2-Na+ ⑵白色物質迅速變為灰綠色,最終變為紅褐色
⑶3Fe+4H2O Fe3O4+4H2↑ 在鋁熱劑上加少量KClO3,插上鎂條并將其點燃 ⑷2Al+2OH-+2H2O=2AlO2-+3H2↑
Fe3O4+4H2↑ 在鋁熱劑上加少量KClO3,插上鎂條并將其點燃 ⑷2Al+2OH-+2H2O=2AlO2-+3H2↑
(每空2分,共10分)
20.⑴CH3CHBrCH3 ⑵②④⑤⑦
⑶ +
+ +2H2O
+2H2O
⑷ +2NaOH
+2NaOH +H2O+NaBr
+H2O+NaBr
⑸HOCH2CH2CH2CHO CH3CH(OH)CH2CHO CH3CH2CH(OH)CHO
(CH3)
(第⑸小題4分,其余每空2分,共12分)
21.⑴參加反應的硝酸的物質的量為(13.5mol/L-1mol/L)×0.080 mol/L=1 mol
被還原的硝酸的物質的量即生成氣體的物質的量: =0.3 mol
=0.3 mol
則未被還原的硝酸的物質的量為1mol-0.3mol=0.7 mol
即生成物AgNO3、Cu(NO3)2中含NO3-0.7 mol
設合金中銀的質量為x,則: ×1+
×1+ ×2=0.7 mol
×2=0.7 mol
解得:x= =0.36(36%)
=0.36(36%)
(4分)
⑵若生成的0.3 mol氣體全部是NO2,則應轉移電子0.3 mol
若生成的0.3 mol氣體全部是NO,則應轉移電子0.9 mol
而合金溶于硝酸時轉移電子數為: ×1+
×1+ ×2=0.7 mol
×2=0.7 mol
所以生成的氣體中既有NO2,又有NO
根據3n(NO)+n(NO2)=0.7 mol n(NO)+n(NO2)=0.3 mol
算出n(NO)=0.2 mol,n(NO2)=0.1 mol
即V(NO)=
(6分)
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com