
題目列表(包括答案和解析)
水煤氣是重要
燃料和化工原料,可用水蒸氣通過熾熱的炭層制得:
C (s) + H2O(g) ![]() CO (g) +H2 (g) △H= +131.3 kJ•mol-1
CO (g) +H2 (g) △H= +131.3 kJ•mol-1
(1)實際工業生產中,向炭層間隔交替通入水蒸氣和空氣,其原因是 。
(2)一定溫度下,三個容器中均進行著上述反應,各容器中炭足量,其它物質的物質的量濃度及正逆反應速率關系如下表所示。請填寫表中相應的空格。
| 容器編號 | c(H2O)/mol·L-1 | c(CO)/mol·L-1 | c(H2)/mol·L-1 | ν正、ν逆比較 |
| I | 0.06 | 0.60 | 0.10 | ν正=ν逆 |
| Ⅱ | 0.12 | 0.20 | ________ | ν正=ν逆 |
| Ⅲ | 0.10 | 0.20 | 0.40 | ν正____ν逆 |
(3)生物乙醇可由淀粉或纖維素等生物質原料發酵獲得。利用乙醇可進而獲得合成氣(CO、H2)。
用乙醇生產合成氣有如下兩條路線:
a、水蒸氣催化重整:CH3CH2OH(g)+H2O(g)→4H2(g)+2CO(g)
b、部分催化氧化:CH3CH2OH(g)+1/2O2(g)→3H2(g)+2CO(g)
某生物質能研究所準備利用乙醇得到的合成氣合成一種生物汽油。乙醇各分一半按a、b兩式反應。合成氣合成生物汽油的反應為:2mCO+(2m+n)H2→2CmHn+2mH2O。假定合成的生物汽油中含有X、Y兩種成分,且X、Y都是有8個碳原子的烴,X是苯的同系物,Y是烷烴。
①X的分子式為 ,Y的分子式為 。
②50噸質量分數為92%的乙醇經上述轉化(假定各步轉化率均為100%),則最終可獲得X的質量為多少噸?
水煤氣是重要燃料和化工原料,可用水蒸氣通過熾熱的炭層制得:
C (s) + H2O(g) CO (g) +H2 (g) △H= +131.3 kJ?mol-1(······①
CO (g) +H2 (g) △H= +131.3 kJ?mol-1(······①
(1)實際工業生產中,向炭層間隔交替通入水蒸氣和空氣,其中通入空氣的原因是由于該反應是吸熱,導致炭層溫度降低,須及時通入富氧空氣促進炭層的燃燒放熱:
C (s) + O2(g)= CO2 (g);△H = -393.5kJ·mo1-1 ······②
為保持生產的連續性,若不考慮其它熱量的產生和損耗,則每間隔應通入的水蒸氣和空氣的體積比(同溫同壓)約為多少?(設空氣中氧氣的體積占1/5)
(2)一定溫度下,三個容器中均進行著上述反應①,各容器中炭足量,其它物質的物質的量濃度及正逆反應速率關系如下表所示。請填寫表中相應的空格。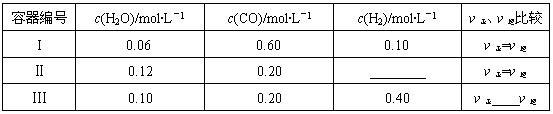
(3)生物乙醇可由淀粉或纖維素等生物質原料發酵獲得。利用乙醇可進而獲得合成氣(CO、H2)。用乙醇生產合成氣有如下兩條路線:
a、水蒸氣催化重整:CH3CH2OH(g)+H2O(g)→4H2(g)+2CO(g)
b、部分催化氧化:CH3CH2OH(g)+1/2O2(g)→3H2(g)+2CO(g)
某生物質能研究所準備利用乙醇得到的合成氣合成一種生物汽油。乙醇各分一半按a、b兩式反應。合成氣合成生物汽油的反應為:2mCO+(2m+n)H2→2CmHn+2mH2O。假定合成的生物汽油中含有X、Y兩種成分,且X、Y都是有8個碳原子的烴,X是苯的同系物,Y是烷烴。
①X的分子式為 ,Y的分子式為 。
②50噸質量分數為92%的乙醇經上述轉化(假定各步轉化率均為100%),則最終可獲得X的質量為多少噸?
水煤氣是重要燃料和化工原料,可用水蒸氣通過熾熱的炭層制得:
C (s) + H2O(g) ![]() CO (g) +H2 (g) △H= +131.3 kJ??mol-1(······①
CO (g) +H2 (g) △H= +131.3 kJ??mol-1(······①
(1)實際工業生產中,向炭層間隔交替通入水蒸氣和空氣,其中通入空氣的原因是由于該反應是吸熱,導致炭層溫度降低,須及時通入富氧空氣促進炭層的燃燒放熱:
C (s) + O2(g)= CO2 (g);△H = -393.5kJ·mo1-1 ······②
為保持生產的連續性,若不考慮其它熱量的產生和損耗,則每間隔應通入的水蒸氣和空氣的體積比(同溫同壓)約為多少?(設空氣中氧氣的體積占1/5)
(2)一定溫度下,三個容器中均進行著上述反應①,各容器中炭足量,其它物質的物質的量濃度及正逆反應速率關系如下表所示。請填寫表中相應的空格。

(3)生物乙醇可由淀粉或纖維素等生物質原料發酵獲得。利用乙醇可進而獲得合成氣(CO、H2)。用乙醇生產合成氣有如下兩條路線:
a、水蒸氣催化重整:CH3CH2OH(g)+H2O(g)→4H2(g)+2CO(g)
b、部分催化氧化:CH3CH2OH(g)+1/2O2(g)→3H2(g)+2CO(g)
某生物質能研究所準備利用乙醇得到的合成氣合成一種生物汽油。乙醇各分一半按a、b兩式反應。合成氣合成生物汽油的反應為:2mCO+(2m+n)H2→2CmHn+2mH2O。假定合成的生物汽油中含有X、Y兩種成分,且X、Y都是有8個碳原子的烴,X是苯的同系物,Y是烷烴。
①X的分子式為 ,Y的分子式為 。
②50噸質量分數為92%的乙醇經上述轉化(假定各步轉化率均為100%),則最終可獲得X的質量為多少噸?
 CO (g) +H2 (g) △H= +131.3 kJ?mol-1(······①
CO (g) +H2 (g) △H= +131.3 kJ?mol-1(······①
某研究性學習小組欲測定某綠色粉末Cu2(OH)2CO3·xH2O中的x值,并進行相關實驗探究.
已知:Cu2(OH)2CO3·xH2O固體在加熱條件下發生反應:
Cu2(OH)2CO3·xH2O![]() 2CuO+CO2↑+(x+1)H2O
2CuO+CO2↑+(x+1)H2O
(Mr[Cu2(OH)2CO3]=222;Mr(CuO)=80;Mr(CO2)=44;Mr(H2O)=18)
[實驗一]測定Cu2(OH)2CO3·xH2O中的x值.
(1)準確稱取m1g.該粉末樣品,置于坩堝中,用酒精燈緩慢加熱至完全分解,冷卻,稱得剩余固體的質量為m2g.加熱粉末時,除了坩禍、坩鍋鉗、三角架、玻璃棒、酒精燈外還要用到的儀器是________,操作中需要用玻璃棒輕輕攪拌固體,目的是________所測得的x值為________(用含m1、m2的代數式表示).
(2)下列是甲、乙兩位同學對實驗過程中綠色粉末是否已完全分解的判斷依據.
甲:觀察到粉末變成黑色,不再有水蒸氣逸出.
乙:重復加熱、冷卻、稱量,至恒重(兩次稱量的質量差不超過0.1 g).
你認為其中合理的是________(填“甲”或“乙”).
(3)測定x值還有其它方法.下列是幾位同學在實驗設計中擬測定的數據,其中無法計算得出x值的是________(填序號).
①只測定生成物CO2、CuO的質量
②只測定生成物CO2、H2O的質量
③只測定反應物Cu2(OH)2CO3·xH2O和生成物CO2的質量
④只測定反應物Cu2(OH)2CO3·xH2O和生成物H2O的質量
[實驗二]利用上述反應的分解產物氧化銅氧化乙醇制備乙醛(沸點為20.8℃).
(1)用如圖所示裝置(圖中夾持裝置已略去)進行實驗時,需要加熱的儀器是________(填標號).B裝置中收集到的物質有________.

(2)能證明氧化銅氧化乙醇的實驗現象是________試管A內發生反應的化學方程式為________.
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com