
題目列表(包括答案和解析)
一定條件下,通過下列反應可實現燃煤煙氣中硫的回收:
2CO(g)+SO2(g)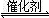 2CO2(g)+S(l) △H
2CO2(g)+S(l) △H
(1)已知2CO(g)+O2(g)= 2CO2(g) △H1=—566kJ?mol—1
S(l) +O2(g)= SO2(g) △H2=—296kJ?mol—1
則反應熱ΔH= kJ?mol-1。
(2)其他條件相同、催化劑不同時,SO2的轉化率隨反應溫度的變化如圖a。260℃時 (填Fe2O3、NiO或Cr2O3)作催化劑反應速率最快。Fe2O3和NiO作催化劑均能使SO2的轉化率達到最高,不考慮價格因素,選擇Fe2O3的主要優點是 。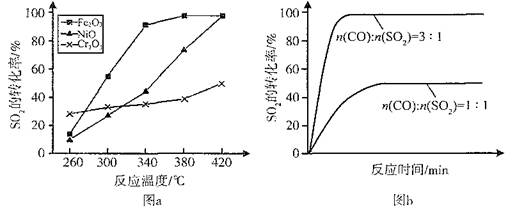
(3)科研小組在380℃、Fe2O3作催化劑時,研究了不同投料比[n(CO)∶n(SO2)]對SO2轉化率的影響,結果如圖b。請在答題卡坐標圖中畫出n(CO)∶n(SO2)="2∶1" 時,SO2轉化率的預期變化曲線。
(4)工業上還可用Na2SO3溶液吸收煙氣中的SO2:Na2SO3+SO2+H2O=2NaHSO3。某溫度下用1.0mol?L-1 Na2SO3溶液吸收純凈的SO2,當溶液中c(SO32-)降至0.2mol?L-1時,吸收能力顯著下降,應更換吸收劑。
①此時溶液中c(HSO3-)約為______mol?L-1;
②此時溶液pH=______。(已知該溫度下SO32—+H+ HSO3—的平衡常數K="8.0" × 106 L?mol-1,計算時SO2、H2SO3的濃度忽略不計)
HSO3—的平衡常數K="8.0" × 106 L?mol-1,計算時SO2、H2SO3的濃度忽略不計)
 2CO2(g)+S(l) △H
2CO2(g)+S(l) △H
 HSO3—的平衡常數K="8.0" × 106 L?mol-1,計算時SO2、H2SO3的濃度忽略不計)
HSO3—的平衡常數K="8.0" × 106 L?mol-1,計算時SO2、H2SO3的濃度忽略不計)| 催化劑 |

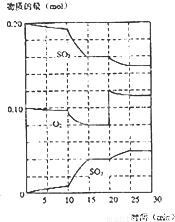
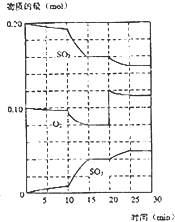 在一定條件下,二氧化硫和氧氣發生如下反應:2SO2(g)+O2(g)?2SO3(g)△H<0
在一定條件下,二氧化硫和氧氣發生如下反應:2SO2(g)+O2(g)?2SO3(g)△H<0| [SO3]2 |
| [SO2]2[O2] |
| [SO3]2 |
| [SO2]2[O2] |
1
2
3
4
5
6
7
8
D
B
C
A
C
D
D
C
9
10
11
12
13
14
╆╆╆╆╆
╆╆╆╆╆
CD
D
D
CD
B
AD
~~~~~
~~~~~
15.每空均2分,共10分
(1)吸附水中有色物質(脫色);(2)S2-+H2O2=S+2OH―(或:S2-+H2O2+2H+=S↓+2H2O);(3)將水樣可能含有的高鐵離子及鉻酸鹽還原;(4)偏低
(5)V1×2c×35.5×1000/V=71000CV1/V
16.(8分)
(1)第三周期第VIIA族 (2分)
(2) 2SO2(g)+O2(g) 2SO3(g)
△H=-196.6 kJ?mol-1 (2分)
2SO3(g)
△H=-196.6 kJ?mol-1 (2分)
(3)Al3++3AlO2-+6H2O=4Al(OH)3↓ (2分) (4) H2O (2分)
 |
17.(10分)
(1) (2分)
(2)2FeCl2+Cl2===2FeCl3 (2分)
(3)2Al+2OH-+2H2O=2AlO2-+3H2↑(2分)
(4)陽極:6O2--12e-=3O2↑;陰極:4Al3++12e-=4Al (每空1分)
(5)錯誤!未找到引用源。 (2分)
18.⑴S2- + H2O HS- +OH- HS- + H2O
HS- +OH- HS- + H2O H2S +OH-(可不寫)
H2S +OH-(可不寫)
⑵2.7×10-3 ⑶172.5 ⑷使BaSO4得到充分的還原(或提高BaS的產量)
①②為吸熱反應,炭和氧氣反應放熱維持反應所需高溫
19.(12分)
(1)D(2分)
(2)Cu(1分)
(3)H2(1分);①隨著反應進行生成鋁離子濃度增大,水解程度增大,產生H+的濃度增大,②該反應放熱,升高溫度反應加快,③銅與鋁構成原電池,加快鋁溶解。(3分)
(4)A、B、D (3分)
(5)A(1分),電解質性質(合理解答同樣給分)(1分)
20.(共10分)
(1)解: 2SO2(g) + O2(g)  2SO3(g)
2SO3(g)
起始濃度/ mol?L-1 0.050 0.030 0
平衡濃度/ mol?L-1 (0.050-0.040) (0.030-0.040/2) 0.040
= 0.010 = 0.010
所以,K = =
=  = 1.6×103 mol?L-1。(不帶單位計算也得分)
= 1.6×103 mol?L-1。(不帶單位計算也得分)
(SO2)
= ×100%
= 80% 。
×100%
= 80% 。
(2)B、C。 (3)SO2+H2O+Na2SO3=2NaHSO3。
(4)抑制Fe2+、Fe3+的水解,防止Fe2+被氧化成Fe3+。
21.(12分)
解:(1)6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O (2分)
(2)n(Fe)=×2=0.035 mol n(SO42-)==0.045 mol
n(OH-)=3×n(Fe3+)-2×n(SO42-)=3×0.035 mol-2×0.045 mol=0.015 mol (3分)
鹽基度=×100%= ×100%=14.29% (2分)
(3)n(H2O)=
=0.054 mol
化學式: Fe35(OH)15(SO4)45?54H2O (3分)
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com