
題目列表(包括答案和解析)
過氧化氫(H2O2)俗稱雙氧水,不穩定,易分解。溶液的酸堿性對H2O2的穩定性有較大影響,如在堿性溶液中,H2O2分解較快。另外,H2O2見光、遇熱、遇到大多數金屬氧化物分解也會加快。以下裝置可用于探究H2O2相關的性質。

請回答:
(1)實驗室用MnO2作催化劑分解H2O2制取氧氣,反應的化學方程式為 。
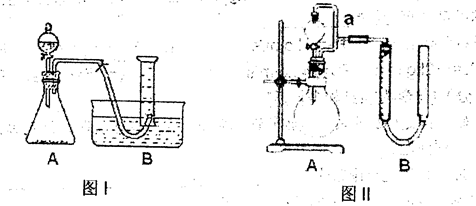
使用圖1裝置時,H2O2應該盛放在 (填“錐形瓶”或“分液漏斗”)中,讀取氧氣體積時要注意 。
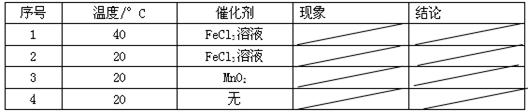
(2)取等物質的量濃度等體積H2O2溶液分別進行下列實驗,研究外界條件對該反應速率的影響,實驗報告如下表所示。

①實驗1、2研究的是 對H2O2分解速率的影響。
②實驗2、3的目的是 。
(3)用 (填“酸式”或“堿式”)滴定管量取25.00mL H2O2溶液于圖II的燒瓶中,滴入過量KMnO4酸性溶液反應,最終收集到56mLO2(已折算為標準狀況),則該H2O2溶液的物質的量濃度為 。
(已知:2KMnO4+5H2O2+3H2SO4=2MnSO4+K2SO4+5O2↑+8H2O)你認為測得的數值比理論值
(填“偏高”、“偏低”或“相等”)
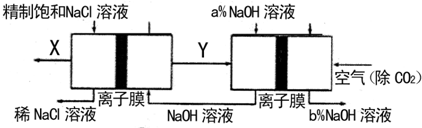
(4)實驗表明Na2O2與水反應也可生成O2。某同學猜想是Na2O2先與H2O反應生成H2O2,然后H2O2分解產生O2。為此做探究如下:取Na2O2樣品(雜質不參與反應)與過量水充分反應的少量X溶液于試管中,滴加FeCl2溶液,立即生成紅褐色沉淀,該反應的離子方程式是 。
過氧化氫(H2O2)俗稱雙氧水,不穩定,易分解。溶液的酸堿性對H2O2的穩定性有較大影響,如在堿性溶液中,H2O2分解較快。另外,H2O2見光、遇熱、遇到大多數金屬氧化物分解也會加快。以下裝置可用于探究H2O2相關的性質。
請回答:
(1)實驗室用MnO2作催化劑分解H2O2制取氧氣,反應的化學方程式為 。
使用圖1裝置時,H2O2應該盛放在 (填“錐形瓶”或“分液漏斗”)中,讀取氧氣體積時要注意 。
(2)取等物質的量濃度等體積H2O2溶液分別進行下列實驗,研究外界條件對該反應速率的影響,實驗報告如下表所示。
①實驗1、2研究的是 對H2O2分解速率的影響。
②實驗2、3的目的是 。
(3)用 (填“酸式”或“堿式”)滴定管量取25.00mL H2O2溶液于圖II的燒瓶中,滴入過量KMnO4酸性溶液反應,最終收集到56mLO2(已折算為標準狀況),則該H2O2溶液的物質的量濃度為 。
(已知:2KMnO4+5H2O2+3H2SO4=2MnSO4+K2SO4+5O2↑+8H2O)你認為測得的數值比理論值
(填“偏高”、“偏低”或“相等”)
(4)實驗表明Na2O2與水反應也可生成O2。某同學猜想是Na2O2先與H2O反應生成H2O2,然后H2O2分解產生O2。為此做探究如下:取Na2O2樣品(雜質不參與反應)與過量水充分反應的少量X溶液于試管中,滴加FeCl2溶液,立即生成紅褐色沉淀,該反應的離子方程式是 。
過氧化氫(H2O2)俗稱雙氧水,不穩定,易分解。溶液的酸堿性對H2O2的穩定性有較大影響,如在堿性溶液中,H2O2分解較快。另外,H2O2見光、遇熱、遇到大多數金屬氧化物分解也會加快。以下裝置可用于探究H2O2相關的性質。
請回答:
(1)實驗室用MnO2作催化劑分解H2O2制取氧氣,反應的化學方程式為 。
使用圖1裝置時,H2O2應該盛放在 (填“錐形瓶”或“分液漏斗”)中,讀取氧氣體積時要注意 。
(2)取等物質的量濃度等體積H2O2溶液分別進行下列實驗,研究外界條件對該反應速率的影響,實驗報告如下表所示。
①實驗1、2研究的是 對H2O2分解速率的影響。
②實驗2、3的目的是 。
(3)用 (填“酸式”或“堿式”)滴定管量取25.00mL H2O2溶液于圖II的燒瓶中,滴入過量KMnO4酸性溶液反應,最終收集到56mLO2(已折算為標準狀況),則該H2O2溶液的物質的量濃度為 。
(已知:2KMnO4+5H2O2+3H2SO4=2MnSO4+K2SO4+5O2↑+8H2O)你認為測得的數值比理論值
(填“偏高”、“偏低”或“相等”)
(4)實驗表明Na2O2與水反應也可生成O2。某同學猜想是Na2O2先與H2O反應生成H2O2,然后H2O2分解產生O2。為此做探究如下:取Na2O2樣品(雜質不參與反應)與過量水充分反應的少量X溶液于試管中,滴加FeCl2溶液,立即生成紅褐色沉淀,該反應的離子方程式是 。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com