
題目列表(包括答案和解析)
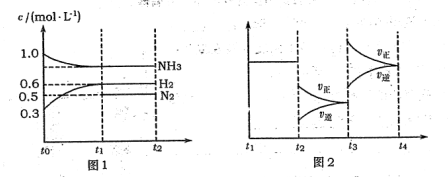
(l4分)向2L固定容積的密閉容器中加入一定量的NH3,H2和N2三種氣體。一定條件下發(fā)生反應2NH3 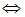 N2+3H2,各物質(zhì)濃度隨時間變化如圖1所示。圖2為t時刻后改變?nèi)萜髦袟l件,平衡體系中反應速率隨時間變化的情況,且兩個階段各改變一種不同的條件。
N2+3H2,各物質(zhì)濃度隨時間變化如圖1所示。圖2為t時刻后改變?nèi)萜髦袟l件,平衡體系中反應速率隨時間變化的情況,且兩個階段各改變一種不同的條件。
(1)能證明反應達到平衡狀態(tài)的是 (填標號,下同)。
A.容器內(nèi)壓強不再發(fā)生變化 B. N2的體積分數(shù)不再發(fā)生變化
C. 容器內(nèi)氣體質(zhì)量不再發(fā)生變化 D. 容器內(nèi)氣體密度不再發(fā)生變化
(2)若tl=15 s,則t0-t1階段以H2濃度變化表示的反應速率為 。
(3)t3-t4階段改變的條件為 。
(4)上述反應的平衡常數(shù)K= (保留兩位小數(shù));向容器中再通入1.4molNH3、0.8 molH2,平衡 移動(填“向右”、“向左”或“不移動”)。
(5)25OC時,將a mol·L-1的氨水與0.1 mol·L-1的鹽酸等體積混合。
①當溶液中離子濃度關系滿足c(NH4+)<c(Cl-)時,則反應的情況可能為
a.鹽酸不足,氨水剩余 b. 氨水與鹽酸恰好完全反應 c.鹽酸過量
②當溶液中c(NH4+)=c(Cl-)時,用含a的代數(shù)式表示NH3·H2O的電離常數(shù)Kb= 。
(l4分)向2L固定容積的密閉容器中加入一定量的NH3,H2和N2三種氣體。一定條件下發(fā)生反應2NH3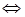 N2+3H2,各物質(zhì)濃度隨時間變化如圖1所示。圖2為t時刻后改變?nèi)萜髦袟l件,平衡體系中反應速率隨時間變化的情況,且兩個階段各改變一種不同的條件。
N2+3H2,各物質(zhì)濃度隨時間變化如圖1所示。圖2為t時刻后改變?nèi)萜髦袟l件,平衡體系中反應速率隨時間變化的情況,且兩個階段各改變一種不同的條件。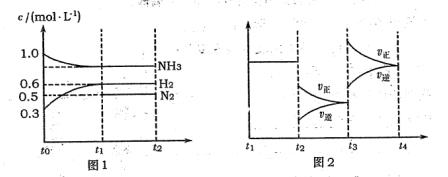
(1)能證明反應達到平衡狀態(tài)的是 (填標號,下同)。
| A.容器內(nèi)壓強不再發(fā)生變化 | B.N2的體積分數(shù)不再發(fā)生變化 |
| C.容器內(nèi)氣體質(zhì)量不再發(fā)生變化 | D.容器內(nèi)氣 體密度不再發(fā)生變化 體密度不再發(fā)生變化 |
 。
。(l4分)向2L固定容積的密閉容器中加入一定量的NH3,H2和N2三種氣體。一定條件下發(fā)生反應2NH3 ![]() N2+3H2,各物質(zhì)濃度隨時間變化如圖1所示。圖2為t時刻后改變?nèi)萜髦袟l件,平衡體系中反應速率隨時間變化的情況,且兩個階段各改變一種不同的條件。
N2+3H2,各物質(zhì)濃度隨時間變化如圖1所示。圖2為t時刻后改變?nèi)萜髦袟l件,平衡體系中反應速率隨時間變化的情況,且兩個階段各改變一種不同的條件。
(1)能證明反應達到平衡狀態(tài)的是 (填標號,下同)。
A.容器內(nèi)壓強不再發(fā)生變化 B. N2的體積分數(shù)不再發(fā)生變化
C. 容器內(nèi)氣體質(zhì)量不再發(fā)生變化 D. 容器內(nèi)氣體密度不再發(fā)生變化
(2)若tl=15s,則t0-t1階段以H2濃度變化表示的反應速率為 。
(3)t3-t4階段改變的條件為 。
(4)上述反應的平衡常數(shù)K= (保留兩位小數(shù));向容器中再通入1.4molNH3、0.8 molH2,平衡 移動(填“向右”、“向左”或“不移動”)。
(5)25OC時,將a mol·L-1的氨水與0.1mol·L-1的鹽酸等體積混合。
①當溶液中離子濃度關系滿足c(NH4+)<c(Cl-)時,則反應的情況可能為
a.鹽酸不足,氨水剩余 b. 氨水與鹽酸恰好完全反應 c.鹽酸過量
②當溶液中c(NH4+)=c(Cl-)時,用含a的代數(shù)式表示NH3·H2O的電離常數(shù)Kb= 。
(1)蓋斯定律在生產(chǎn)和科學研究中有很重要的意義。有些反應的反應熱雖然無法直接測得,但可通過間接的方法測定。現(xiàn)根據(jù)下列3個熱化學反應方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-24.8kJ·mol-1
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H=-47.4kJ·mol-1
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H=+640.5kJ·mol-1
寫出CO氣體還原FeO固體得到Fe 固體和CO2氣體的熱化學反應方程式:
。
(2)在壓強為0.1 MPa條件下,容積為V L某密閉容器中a mol CO與 2a mol H2在催化劑作用下反應生成甲醇:CO(g)+2H2(g) 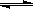 CH3OH(g);CO的轉(zhuǎn)化率與溫度、壓強的關系如圖所示。
CH3OH(g);CO的轉(zhuǎn)化率與溫度、壓強的關系如圖所示。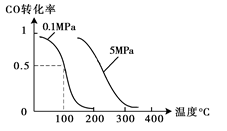
①該反應的△H 0 (填“<”、“>”或“=”)。
②在溫度容積不變的情況下,向該密閉容器再
增加a mol CO與 2a mol H2,達到新平衡時,CO的轉(zhuǎn)化率 (填“增大”、“減小”或“不變”)。
(3)實驗室中配制AgNO3溶液時通常需要向其中加入 ,目的是 ; AgCl在水中存在沉淀溶解平衡:
AgCl(s) Ag+(aq)+Cl-(aq)。25oC時,現(xiàn)將足量AgCl分別放入:①l00mL蒸餾水;②l0 0mL 0.2 mol?L-1AgNO3溶液;③100mL 0.1 mol?L-1氯化鎂溶液;④100mL 0.1 mol?L-1氯化鈉溶液。充分攪拌后,相同溫度下Ag+濃度由大到小的順序是 (填寫序號)。
Ag+(aq)+Cl-(aq)。25oC時,現(xiàn)將足量AgCl分別放入:①l00mL蒸餾水;②l0 0mL 0.2 mol?L-1AgNO3溶液;③100mL 0.1 mol?L-1氯化鎂溶液;④100mL 0.1 mol?L-1氯化鈉溶液。充分攪拌后,相同溫度下Ag+濃度由大到小的順序是 (填寫序號)。
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com