
題目列表(包括答案和解析)
二氧化硫是重要的工業原料,探究其制備方法和性質具有非常重要的意義。
(1)工業上用黃鐵礦(FeS2,其中S元素為-l價)在高溫下和氧氣反應制備SO2: ,該反應中被氧化的元素是 (填元素符號)。當該反應轉移2.75mol電子時,生成的二氧化硫在標準狀況下的體積為 L。
,該反應中被氧化的元素是 (填元素符號)。當該反應轉移2.75mol電子時,生成的二氧化硫在標準狀況下的體積為 L。
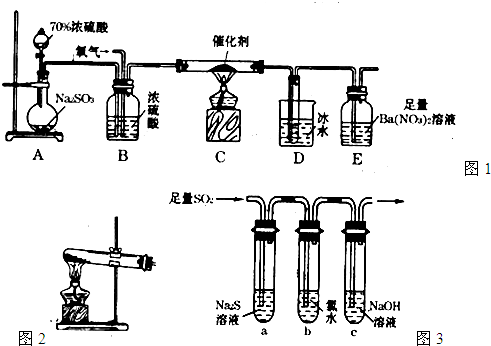
(2)實驗室中用下列裝置測定SO2催化氧化為SO3的轉化率。(已知SO3熔點為16. 8℃,假設氣體進入裝置時分別被完全吸收,且忽略空氣中CO2的影響。) 
①簡述使用分液漏斗向圓底燒瓶中滴加濃硫酸的操作是 。
②實驗過程中,需要通入氧氣。試寫出一個用右圖所示裝置制取氧氣的化學方程式 。
③當停止通入SO2,熄滅酒精燈后,需要繼續通一段時間的氧氣,其目的是 。
④實驗結束后,若裝置D增加的質量為m g,裝置E中產生白色沉淀的質量為n g,則此條件下二氧化硫的轉化率是 (用含字母的代數式表示,不用化簡)。
(3)某學習小組設計用如右圖裝置驗證二氧化硫的化學性質。
①能說明二氧化硫具有氧化性的實驗現象為 。
②為驗證二氧化硫的還原性,充分反應后,取試管b中的溶液分成三份,分別進行如下實驗: 
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品紅溶液,紅色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,產生白色沉淀
上述方案中合理的是 (填“I”、“Ⅱ”或“Ⅲ”);試管b中發生反應的離子方程式為 。
③當通入二氧化硫至試管c中溶液顯中性時,該溶液中c(Na+)= (用含硫微粒濃度的代數式表示)。)】
二氧化硫是重要的工業原料,探究其制備方法和性質具有非常重要的意義。
(1)工業上用黃鐵礦(FeS2,其中S元素為-l價)在高溫下和氧氣反應制備SO2:
 ,該反應中被氧化的元素是 (填元素符號)。當該反應轉移2.75mol電子時,生成的二氧化硫在標準狀況下的體積為 L。
,該反應中被氧化的元素是 (填元素符號)。當該反應轉移2.75mol電子時,生成的二氧化硫在標準狀況下的體積為 L。
(2)實驗室中用下列裝置測定SO2催化氧化為SO3的轉化率。(已知SO3熔點為16. 8℃,假設氣體進入裝置時分別被完全吸收,且忽略空氣中CO2的影響。)

①簡述使用分液漏斗向圓底燒瓶中滴加濃硫酸的操作是 。
②實驗過程中,需要通入氧氣。試寫出一個用右圖所示裝置制取氧氣的化學方程式 。

③當停止通入SO2,熄滅酒精燈后,需要繼續通一段時間的氧氣,其目的是 。
④實驗結束后,若裝置D增加的質量為m g,裝置E中產生白色沉淀的質量為n g,則此條件下二氧化硫的轉化率是 (用含字母的代數式表示,不用化簡)。
(3)某學習小組設計用如右圖裝置驗證二氧化硫的化學性質。
①能說明二氧化硫具有氧化性的實驗現象為 。
②為驗證二氧化硫的還原性,充分反應后,取試管b中的溶液分成三份,分別進行如下實驗:

方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品紅溶液,紅色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,產生白色沉淀
上述方案中合理的是 (填“I”、“Ⅱ”或“Ⅲ”);試管b中發生反應的離子方程式為 。
③當通入二氧化硫至試管c中溶液顯中性時,該溶液中c(Na+)= (用含硫微粒濃度的代數式表示)。)】
 8SO2+2Fe2O3,該反應中被氧化的元素是______(填元素符號).當該反應轉移2.75mol電子時,生成的二氧化硫在標準狀況下的體積為______L.
8SO2+2Fe2O3,該反應中被氧化的元素是______(填元素符號).當該反應轉移2.75mol電子時,生成的二氧化硫在標準狀況下的體積為______L.
| ||
二氧化硫是重要的工業原料,探究其制備方法和性質具有非常重要的意義。
(1)工業上用黃鐵礦(FeS2,其中S元素為-l價)在高溫下和氧氣反應制備SO2:
![]() ,該反應中被氧化的元素是 (填元素符號)。當該反應轉移2.75mol電子時,生成的二氧化硫在標準狀況下的體積為 L。
,該反應中被氧化的元素是 (填元素符號)。當該反應轉移2.75mol電子時,生成的二氧化硫在標準狀況下的體積為 L。
(2)實驗室中用下列裝置測定SO2催化氧化為SO3的轉化率。(已知SO3熔點為16.8℃,假設氣體進入裝置時分別被完全吸收,且忽略空氣中CO2的影響。)

 ①簡述使用分液漏斗向圓底燒瓶中滴加濃硫酸的操作是 。
①簡述使用分液漏斗向圓底燒瓶中滴加濃硫酸的操作是 。
②實驗過程中,需要通入氧氣。試寫出一個用右圖所示裝置制取氧氣的化學方程式 。
③當停止通入SO2,熄滅酒精燈后,需要繼續通一段時間的氧氣,其目的是 。
 ④實驗結束后,若裝置D增加的質量為m g,裝置E中產生白色沉淀的質量為n g,則此條件下二氧化硫的轉化率是 (用含字母的代數式表示,不用化簡)。
④實驗結束后,若裝置D增加的質量為m g,裝置E中產生白色沉淀的質量為n g,則此條件下二氧化硫的轉化率是 (用含字母的代數式表示,不用化簡)。
(3)某學習小組設計用如右圖裝置驗證二氧化硫的化學性質。
①能說明二氧化硫具有氧化性的實驗現象為 。
②為驗證二氧化硫的還原性,充分反應后,取試管b中的溶液分成三份,分別進行如下實驗:
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品紅溶液,紅色褪去
方案Ⅲ:向第三份溶液加入BaCl2溶液,產生白色沉淀
上述方案中合理的是 (填“I”、“Ⅱ”或“Ⅲ”);試管b中發生反應的離子方程式為 。
③當通入二氧化硫至試管c中溶液顯中性時,該溶液中c(Na+)= (用含硫微粒濃度的代數式表示)。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com