
題目列表(包括答案和解析)
(6分)在一定溫度下的某容積可變的密閉容器中,建立下列化學平衡:
C(s)+H2O(g)CO(g)+H2(g)
試分析和回答下列問題:
(1)可認定上述可逆反應在一定條件下已達到化學平衡狀態的是 (選填序號)。
A 體系的壓強不再發生變化
B v正(CO)=v逆(H2O)
C 生成n molCO的同時生成n mol H2
D 1mol H-H鍵斷裂的同時斷裂2mol H-O鍵
(2)若上述化學平衡狀態從正反應開始建立,達到平衡后,給平衡體系加壓(縮小容積.其它條件不變。下同),則容器內氣體的平均相對分子質量面將 (填寫不變.變小.變大)。,達到平衡后,試討論:
①容積內氣體混合物的平均相對分子質量 的取值范圍是 。
的取值范圍是 。
②若給平衡體系加壓,請參照起始投放的氣體物質的平均相對分子質量(設定為 1),分別給出
1),分別給出![]() 的變化:(填“增大”.“減小”.“不變”)
的變化:(填“增大”.“減小”.“不變”)
|
|
|
|
|
|
|
| 不變 |
|
|
|
(6分)在一定溫度下的某容積可變的密閉容器中,建立下列化學平衡:
C(s)+H2O(g)
 CO(g)+H2(g)
CO(g)+H2(g)
試分析和回答下列問題:
(1)可認定上述可逆反應在一定條件下已達到化學平衡狀態的是 (選填序號)。
A 體系 的壓強不再發生變化
的壓強不再發生變化
B v正(CO)=v逆(H2O)
C 生成n molCO的同時生成n mol H2
D 1mol H-H鍵斷裂的同時斷裂2mol H-O鍵
(2)若上述化學平衡狀態從 正反應開始建立,達到平衡后,給平衡體系加壓(縮小容積.其它條件不變。下同),則容器內氣體的平均相對分子質量面將 (填寫不變.變小.變大)。[來源:學科
正反應開始建立,達到平衡后,給平衡體系加壓(縮小容積.其它條件不變。下同),則容器內氣體的平均相對分子質量面將 (填寫不變.變小.變大)。[來源:學科
(3)若上述化學平衡狀態從正.逆兩反應同時建立[即起始時同時投放C(s).H2O(g).CO(g).H2(g)],達到平衡后,試討論:
①容積內氣體混合物的平均相對分子質量 的取值范圍是 。
的取值范圍是 。
②若給平衡體系加壓,請參照起始投放的氣體物質的平均相對分子質量(設定為 1),分別給出
1),分別給出 的變化:(填“增大”.“減小”.“不變”)
的變化:(填“增大”.“減小”.“不變”)
 1的取值 1的取值 |  的變化 的變化 |
 1<12 1<12 | |
 1=12 1=12 | 不變 |
 1>12 1>12 | |
(6分)在一定溫度下的某容積可變的密閉容器中,建立下列化學平衡:
C(s)+H2O(g) CO(g)+H2(g)
CO(g)+H2(g)
試分析和回答下列問題:
(1)可認定上述可逆反應在一定條件下已達到化學平衡狀態的是 (選填序號)。
A 體系的壓強不再發生變化
B v正(CO)=v逆(H2O)
C 生成n molCO的同時生成n mol H2
D 1mol H-H鍵斷裂的同時斷裂2mol H-O鍵
(2)若上述化學平衡狀態從正反應開始建立,達到平衡后,給平衡體系加壓(縮小容積.其它條件不變。下同),則容器內氣體的平均相對分子質量面將 (填寫不變.變小.變大)。[來源:學科
(3)若上述化學平衡狀態從正.逆兩反應同時建立[即起始時同時投放C(s).H2O(g).CO(g).H2(g)],達到平衡后,試討論:
①容積內氣體混合物的平均相對分子質量 的取值范圍是
。
的取值范圍是
。
②若給平衡體系加壓,請參照起始投放的氣體物質的平均相對分子質量(設定為 1),分別給出
1),分別給出 的變化:(填“增大”.“減小”.“不變”)
的變化:(填“增大”.“減小”.“不變”)
|
|
|
|
|
|
|
|
不變 |
|
|
|
在一定溫度下的某容積可變的密閉容器中,建立下列化學平衡:
C(s)+H2O(g)![]() CO(g)+H2(g)
CO(g)+H2(g)
試分析和回答下列問題:
(1)可認定上述可逆反應在一定條件下已達到化學平衡狀態的是 (選填序號)。
A 體系的壓強不再發生變化
B v正(CO)=v逆(H2O)
C 生成n molCO的同時生成n mol H2
D 1mol H-H鍵斷裂的同時斷裂2mol H-O鍵
(2)若上述化學平衡狀態從![]() 正反應開始建立,達到平衡后,給平衡體系加壓(縮小容積.其它條件不變。下同),則容器內氣體的平均相對分子質量面將 (填寫不變.變小.變大)。,達到平衡后,試討論:
正反應開始建立,達到平衡后,給平衡體系加壓(縮小容積.其它條件不變。下同),則容器內氣體的平均相對分子質量面將 (填寫不變.變小.變大)。,達到平衡后,試討論:
①容積內氣體混合物的平均相對分子質量![]() 的取值范圍是 。
的取值范圍是 。
②若給平衡體系加壓,請參照起始投放的氣體物質的平均相對分子質量(設定為![]() 1),分別給出
1),分別給出![]() 的變化:(填“增大”.“減小”.“不變”)
的變化:(填“增大”.“減小”.“不變”)
|
|
|
|
| |
|
| 不變 |
|
|

 CO(g)+H2(g)
CO(g)+H2(g) 的壓強不再發生變化
的壓強不再發生變化 正反應開始建立,達到平衡后,給平衡體系加壓(縮小容積.其它條件不變。下同),則容器內氣體的平均相對分子質量面將 (填寫不變.變小.變大)。
正反應開始建立,達到平衡后,給平衡體系加壓(縮小容積.其它條件不變。下同),則容器內氣體的平均相對分子質量面將 (填寫不變.變小.變大)。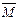 的取值范圍是 。
的取值范圍是 。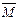 1),分別給出
1),分別給出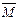 的變化:(填“增大”.“減小”.“不變”)
的變化:(填“增大”.“減小”.“不變”)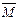 1的取值 1的取值 | 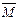 的變化 的變化 |
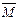 1<12 1<12 | |
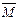 1=12 1=12 | 不變 |
 1>12 1>12 | |
命題人:李孝平 審題人:李白仲
一、二選擇題:(1―10題每題2分,11-18每題3分,共44分)
題 號
1
2
3
4
5
6
7
8
9
10
答 案
B
D
A
B
D
C
C
B
B
C
題 號
11
12
13
14
15
16
17
18
答 案
D
B
B
C
C
D
A
A
三、填空題:(本題共5小題,共46分)
19、①、③、⑧; ②、④; ⑤; ⑥、⑦;(每空1分)
20、(1) 略 3分 ;(2)略 4分
(3)c3>c1>c2;CH3COOH; D。(各2分)
21、(1)、4;(2分) (2)、大于(1分);因為升溫水的電離平衡右移,離子濃度增大,Kw增大;(2分)
22、(1)H-O-O-H(2分) (2)N2H4(l)+H2O2(l) == N2(g) +2H2O(l) △H=-644.25 KJ/mol(3分)(3)產物不會造成環境污染。(1分)
23、(10分)(1)1 (2分) (2)否、(2分) 大于(1分) 因為
試卷.files/image027.gif)
試卷.files/image029.jpg)
試卷.files/image031.jpg)
= = <K平衡向右移動(3分)
(3)增大 減小(各1分)
24、(1)加快 (2)D (3)40% 試卷.files/image033.gif) L (各2分)
L (各2分)
25、(10分)⑴、反應產生氣泡快慢或反應完成的先后或試管壁的冷熱程度 ;
控制陰離子相同,排除陰離子的干擾 ; 將FeCl3改為Fe2(SO4)3
⑵、關閉A處活塞,將注射器活塞拉出一定距離,一段時間后松開活塞,觀察活塞是否回到原位 一定時間內收集到的氣體體積或收集一定體積的氣體所需要的時間 ( 合理答案同樣給分) 各2分
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com