��15�֣���1��25��r��0��1 mol��L
��1��HA��Һ��c(H
+)/c(OH
-)��10
10��Ո�ش����І��}��
��HA��________(���(qi��ng)늽��|(zh��)������늽��|(zh��)��)��
���ڼ�ˮϡ�HA��Һ���^���У��S��ˮ�������Ӷ��pС����________(����ĸ)��
A��c(H
+)/c(HA)�� B��c(HA)/(A
-) C��c(H
��)�cc(OH
��)�ij˷e �� D��c(OH
��)
����M��Һ��������HA��ҺV
1 mL�cpH = 12��NaOH��ҺV
2 mL��ϳ�ַ���(y��ng)���ã��t�����f�������_����
A������ҺM�����ԣ��t��ҺM��c(H
+) + c(OH
-) = 2��0��10
-7 mol��L
-1B����V
1 =V
2 ���t��ҺM��pHһ������7
C������ҺM�����ԣ�V
1һ������V
2D������ҺM�ʉA�ԣ�V
1һ��С��V
2��2������֪��25�棬AgCl��K
sp = 1��8��10
-10���F(xi��n)������AgCl�քe���룺��100 mL ���sˮ�У���100 mL 0��2mol��L
-1 AgNO
3��Һ�У���100 mL 0��1mol��L
-1 AlCl
3��Һ�У���100 mL 0��1mol��L
-1�}���У����?j��n)������ͬ�ض���c(Ag
+)�ɴ�С�������
������̖�B�ӣ�
��3����1mol SO
2(g)������1mol SO
3(g)�Ħ�H ����99kJ��mol
��1�����|(zh��)���ȼ�����296kJ��mol
��1���t��S(s)����3 mol SO
3(g)�Ħ�H =
��4������2NO
2(g)

N
2O
4(g) ��H < 0����(y��ng)���ڜضȞ�T
1��T
2�r��ƽ���wϵ��NO
2���w�e��?j��n)?sh��)�S����(qi��ng)׃��������D��ʾ���t�����f�����_����
��

�٣�A��C���c(di��n)�ķ���(y��ng)���ʣ�A>C
�ڣ�A��C���c(di��n)���w���ɫ��A�C�\
�ۣ�B��C���c(di��n)�Ě��w��ƽ�������|(zh��)����B<C
�ܣ��ɠ�B(t��i)B����B(t��i)A�������üӟ᷽��
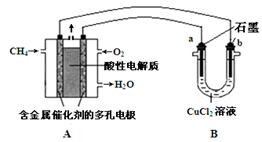
��5���D�����ü���ȼ��늳�늽�50 mL 2 mol��L
-1���Ȼ��~��Һ���b��ʾ��D��

Ո�ش�
�� ����ȼ��늳ص�ؓ(f��)�O����(y��ng)ʽ��
��
�� ��(d��ng)��·����0��2 mol���ͨ�^�r��ꎘO����____g��

 HCO3-+OH-
HCO3-+OH- HCO3-+OH-
HCO3-+OH- C2D4��g������H��0���ں�غ��ݗl���£���һ����CD2��C2D4�Ļ�Ϛ��wͨ���ݷe��2L�����]�����У�����(y��ng)�^���и����|(zh��)�����|(zh��)�������c�S�r�gt��׃���P(gu��n)ϵ��D��ʾ��
C2D4��g������H��0���ں�غ��ݗl���£���һ����CD2��C2D4�Ļ�Ϛ��wͨ���ݷe��2L�����]�����У�����(y��ng)�^���и����|(zh��)�����|(zh��)�������c�S�r�gt��׃���P(gu��n)ϵ��D��ʾ��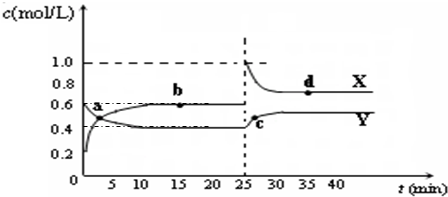
 2NO2��g������H=+57kJ��mol-1���ڜضȞ�T1��T2��ƽ���wϵ��NO2�w�e��?j��n)?sh��)�S����(qi��ng)׃�����������D��ʾ�������f�����_����
2NO2��g������H=+57kJ��mol-1���ڜضȞ�T1��T2��ƽ���wϵ��NO2�w�e��?j��n)?sh��)�S����(qi��ng)׃�����������D��ʾ�������f�����_����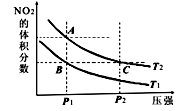
 N2O4(g) ��H < 0����(y��ng)���ڜضȞ�T1��T2�r��ƽ���wϵ��NO2���w�e��?j��n)?sh��)�S����(qi��ng)׃��������D��ʾ���t�����f�����_���� ��
N2O4(g) ��H < 0����(y��ng)���ڜضȞ�T1��T2�r��ƽ���wϵ��NO2���w�e��?j��n)?sh��)�S����(qi��ng)׃��������D��ʾ���t�����f�����_���� ��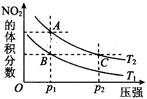
 N2O4(g) ��H < 0����(y��ng)���ڜضȞ�T1��T2�r��ƽ���wϵ��NO2���w�e��?j��n)?sh��)�S����(qi��ng)׃��������D��ʾ���t�����f�����_���� ��
N2O4(g) ��H < 0����(y��ng)���ڜضȞ�T1��T2�r��ƽ���wϵ��NO2���w�e��?j��n)?sh��)�S����(qi��ng)׃��������D��ʾ���t�����f�����_���� ��

 ��֪NO2��N2O4������D(zhu��n)����2NO2��g��?N2O4��g����H��0���F(xi��n)��һ����NO2��N2O4�Ļ�Ϛ��wͨ���w�e��2 L�ĺ�����]�����У�����(y��ng)�����S�r�g׃���P(gu��n)ϵ��D��ʾ��
��֪NO2��N2O4������D(zhu��n)����2NO2��g��?N2O4��g����H��0���F(xi��n)��һ����NO2��N2O4�Ļ�Ϛ��wͨ���w�e��2 L�ĺ�����]�����У�����(y��ng)�����S�r�g׃���P(gu��n)ϵ��D��ʾ��