
題目列表(包括答案和解析)
某學習小組用如圖所示裝置測定鋅銅合金中銅的質量分數。(已知:金屬與酸時放出一定的熱量)

(1)實驗前,先將鋅銅合金在稀酸中浸泡片刻,其目的是 ;
(2)實驗操作步驟有:檢查氣密性,將藥品和水裝入各儀器中,連接好裝置后,再進行的操作還有:①記錄C的液面位置;②待B中不再有氣體產生并恢復至室溫后,記錄C的液面位置;③由A向B滴加足量試劑;④檢查氣密性。
上述再進行的操作的順序是 (填序號);
(3)該裝置的氣密性的檢驗方法是打開分液漏斗旋塞,從D管注入經濟易得的 ,使U型管左右液面相平,關閉分液漏斗旋塞,提高D管, ,說明裝置的氣密性好;
(4)待B中不再有氣體產生,記錄C的液面位置前,需將溫度恢復至室溫和 ;
(5)若實驗用鋅銅合金的質量為ag,與稀硫酸充分反應后,測得氫氣體積為V L,為求出合金中銅的質量分數,還缺少的一個數據是 ;
A.反應前加入稀硫酸的體積 B.反應前加入稀硫酸的質量分數
C.實驗前反應裝置中空氣的體積 D.實驗條件下氫氣的密度
(6)若a為0.4g,V為80mL,求合金中銅的質量分數。(在實驗條件下,H2的密度為0.09g/L,5分)
(7)實驗過程中,若未冷卻就讀取氣體體積,則測得鋅的質量分數將 (填 “偏大”、“偏小”或“不受影響”)。
(8)可指導老師認為,利用上述實驗裝置,測量結果總會偏小,原因是 ,改進方法是 。
【解析】(1) 先將鋅銅合金在稀酸中浸泡片刻,其目的是除去表面氧化物(2)根據實驗操作的步驟進行解答(3)根據裝置的氣密性的檢驗方法進行解答(5)根據質量=體積乘以密度進行解答(6)由題可知氫氣的質量,根據化學方程式求得鋅的質量,可求得銅的質量分數(7) 未冷卻氫氣體積偏大,即氫氣的質量偏大,求得鋅的質量分數將偏大,(8)根據能影響生成氣體體積的因素進行解答
通過學習化學,相信你已經初步掌握了實驗室制取氣體的有關知識。請結合圖示回答問題。
A B C D E F
(1)寫出圖中標示的儀器名稱:② 。
(2)注射器A可用于檢查裝置C的氣密性,步驟如下:
①向錐形瓶中加入少量水至 處。
②將注射器A連接到裝置C的橡膠管(或導管口)處。
③緩慢拉動注射器A的活塞,觀察到 ,表示裝置C的氣密性良好。
(3)實驗室用加熱氯酸鉀與二氧化錳混合物的方法制取氧氣,應選擇的發生裝置和收集裝置是 ,寫出該反應的文字表達式 。
小芳發現,氯酸鉀與氧化銅混合加熱,也能較快產生氧氣,于是進行如下探究:
【提出猜想】除Mn02、CuO外,Fe203也可以作KCl03分解的催化劑。
【完成實驗】按下表進行實驗:測定分解溫度(分解溫度越低,催化效果越好)。
| 實驗編號 | 實驗藥品 | 分解溫度(℃) |
| ① | KCl03 | 580 |
| ② | KCl03、Mn02(質量比1:1) | 350 |
| ③ | KCl03、CuO(質量比l:1) | 370 |
| ④ | KCl03、Fe203(質量比1:1) | 390 |
通過學習化學,相信你已經初步掌握了實驗室制取氣體的有關知識。請結合圖示回答問題。
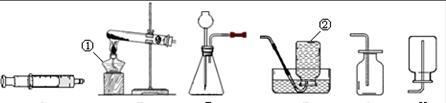
A B C D E F
(1)寫出圖中標示的儀器名稱:② 。
(2)注射器A可用于檢查裝置C的氣密性,步驟如下:
①向錐形瓶中加入少量水至 處。
②將注射器A連接到裝置C的橡膠管(或導管口)處。
③緩慢拉動注射器A的活塞,觀察到 ,表示裝置C的氣密性良好。
(3)實驗室用加熱氯酸鉀與二氧化錳混合物的方法制取氧氣,應選擇的發生裝置和收集裝置是 ,寫出該反應的文字表達式 。
小芳發現,氯酸鉀與氧化銅混合加熱,也能較快產生氧氣,于是進行如下探究:
【提出猜想】除Mn02、CuO外,Fe203也可以作KCl03分解的催化劑。
【完成實驗】按下表進行實驗:測定分解溫度(分解溫度越低,催化效果越好)。
|
實驗編號 |
實驗藥品 |
分解溫度(℃) |
|
① |
KCl03 |
580 |
|
② |
KCl03、Mn02(質量比1:1) |
350 |
|
③ |
KCl03、CuO(質量比l:1) |
370 |
|
④ |
KCl03、Fe203(質量比1:1) |
390 |
【分析數據、得出結論】(1)由實驗____________與實驗④對比,證明猜想合理
(2)實驗所用的三種金屬氧化物,催化效果最好的是_____________________。
【反思】(1)若要證明Fe203是該反應的催化劑,還要驗證它在化學反應前后的質量和___不變;
(2)同種催化劑,顆粒大小可能影響催化效果,請設計實驗方案進行驗證___________ 。
【整理實驗臺】實驗結束后,對實驗儀器進行清洗。大試管清洗干凈的標志是 。

| 實驗編號 | 實驗藥品 | 分解溫度(℃) |
| ① | KCl03 | 580 |
| ② | KCl03、Mn02(質量比1:1) | 350 |
| ③ | KCl03、CuO(質量比l:1) | 370 |
| ④ | KCl03、Fe203(質量比1:1) | 390 |
已知某純堿粗產品僅含有NaCl雜質,為測定該純堿粗產品中純堿的質量分數,某興趣小組的同學設計了下圖所示的實驗裝置,取10.0 g粗產品進行實驗。

【說明】堿石灰是CaO與NaOH 的固體混合物,能吸收水和二氧化碳。E裝置中的飽和NaHCO3溶液是為了除去二氧化碳氣體中的氯化氫,發生的反應為NaHCO3 十HC1 = NaCl十CO2↑十H2O。
實驗主要操作步驟如下:
①連接好裝置,檢查氣密性;②打開彈簧夾C,在A處緩緩通入一段時間空氣;③稱量 G的質量;④關閉彈簧夾C,慢慢滴加濃鹽酸至過量,直至D中無氣泡冒出;⑤打開彈簧夾C,再次緩緩通入一段時間空氣;⑥再次稱量 G的質量,測得質量增加了0.48 g。
請回答下列問題
(1)F中的試劑應為___________________________。
(2)B裝置的作用是__________________________,B裝置中發生反應的化學方程式為:
____________________________________________________________________________
(3)H裝置的作用是 。
(4)事實上10.0 g粗產品只能產生0.40g CO2。請你仔細分析上述實驗,解釋G的質量增加了0.48 g的原因(假設操作均正確) 。
一、選擇題:(共30分)
一
題號
1
2
3
4
5
6
7
8
答案
D
D
D
B
B
C
C
D
題號
9
10
11
12
13
14
15
答案
A
B
C
B
C
C
A
二、填空題:(共30分)
16、(2分)2PbO?PbO2 ,Pb2(PbO4)或Pb(PbO2)2
17、(3分)CO+PdCl2+H2O==2HCl+Pd+CO2;還原。
18、(3分)(1)燃燒產物中存在CO2;⑵存在;中的澄清石灰水變渾濁。
19、(2分)將肥皂水分別逐滴滴入這四種待測溶液并振蕩,根據肥皂水滴入后開始產生泡沫時的不同滴數來區分 。
20、(2分)揮發出來的HCl進入石灰水,與Ca(OH)2作用而阻礙了CO2與Ca(OH)2的作用 (1分) ;CO2與生成的CaCO3作用,生成Ca(HCO3)2 (1分 )。
21、(2分)Si3N4 ;H2SiO3。
22、(6分)⑴用玻璃棒把待測溶液滴在一張pH試紙上,并約一分鐘內把試紙顯示的顏色跟比色卡對照; ⑵堿;酸。⑶洗發;護發。
23、(6分)
⑴ ① H2S+Na2CO3=NaHCO3+NaHS ;② NaHS+RNO+H2O=S↓+NaOH+RNHOH ;
③ NaOH+Na HCO3=Na2CO3+H2O ;④ 2RNHOH+O2=2RNO+2H2O
⑵ 2H2S+O2=2S↓+2H2O;催化
三、實驗題:(共29分)
24、(11分)⑴除去鼓入空氣中的二氧化碳;防止空氣中的二氧化碳和水進入B中影響實驗結果;防止D中的水蒸氣進入B中;用除去二氧化碳的空氣趕走體系中的二氧化碳;用除去二氧化碳的空氣將反應產生的二氧化碳 全部趕入B中; 不能 ,①空氣中含少量二氧化碳、②反應后裝置中殘留二氧化碳均會造成結論偏差。⑵ 43.4 ;95.4% 。
25、(12分) (1) 乙;因為鐵是化學性質較活潑的金屬,尤其是鐵粉顆粒小,常溫下更易與空氣中的氧氣、水蒸氣反應而生銹。 (2)
實驗步驟
預期的實驗現象
結論
①用磁鐵充分接觸濾紙上的脫氧劑粉末
絕大部分黑色粉末被吸引
脫氧劑的成分是鐵粉
②將紅色物質放入小試管中,加入足量稀硫酸觀察現象。繼續滴加足量的NaOH溶液。
紅色物質溶解,溶液呈黃棕色,產生紅褐色沉淀
紅色物質是Fe203
此項可有多種答案,只要原理正確,各項敘述清楚,能確定鐵粉及氧化鐵的存在,均可給分。
(3) Fe203 + 3H2SO4 = Fe2( SO4 )3十3H2O
Fe2( SO4 )3 + 6NaOH === 2Fe (OH)3↓+3Na2 SO4
26、(6分) 換一根長的導管,并用濕毛巾包住導管,然后再在導管的另一端做點火試驗。
⑷導管口同樣能點燃,去掉毛巾,導內壁看不到冷凝的固體;
導管口不能點燃,去掉毛巾,導管內壁可看到有冷凝的固體
導管口能點燃,但火焰較小,去掉毛巾,導管內壁能看到冷凝的固體。
⑸2CnH2n+2+(3n+1)O2 點燃 2nCO2+(2n+2) H2O
四、計算題
27、 (l)84.8%,
實驗次數
每次產生的CO2的質量(g)
第一次先逐滴加鹽酸100g
0
第二次再逐滴加鹽酸100g
第三次再逐滴加鹽酸100g
②關系圖。
.files/image007.gif) CO2
CO2
.files/image008.gif) |
.files/image009.gif)
.files/image010.gif)
.files/image011.gif) 質量/g
質量/g
8.8
0 100 200 300 稀鹽酸質量/g
本資料由《七彩教育網》www.7caiedu.cn 提供!
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com