
題目列表(包括答案和解析)
黃鐵礦主要成分是FeS2。某硫酸廠在進行黃鐵礦成分測定時,取2.000g樣品在空氣中充分灼燒(假設雜質不參加反應),將生成的SO2氣體與足量Fe2(SO4)3溶液完全反應后,用濃度為0.3360mol·L-1的KMnO4標準溶液滴定至終點,消耗KMnO4溶液25.00mL。
已知:①4FeS2+11O2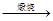 2Fe2O3+8SO2
2Fe2O3+8SO2
②SO2+2Fe3++2H2O→SO42-+2Fe2++4H+
③MnO4-+5Fe2++8H+→Mn2++5Fe3++4H2O
(1)樣品中FeS2的質量分數是 。(用小數表示,保留三位,下同)
(2)煅燒1000 t該黃鐵礦生產出997.9 t硫酸銨,若黃鐵礦制取硫酸時的利用率為0.800,則在制取硫酸銨時硫酸的利用率為 。
(3)為使黃鐵礦充分燃燒,工業上使用過量空氣(設空氣中O2的體積分數為0.200),當空氣過量20%時,煅燒后氣體中SO2的體積分數是多少?
(4)若接觸室導出的氣體中含體積分數為0.0672的SO3。把出口氣體送進吸收塔,用質量分數為0.980的硫酸吸收,可得到“發煙H2SO4”(H2SO4和SO3的混合物,其中含質量分數為0.200的SO3)。計算吸收106 m3出口氣體(已折算為標準狀況)所需要質量分數為0.980的硫酸的質量。
黃鐵礦主要成分是FeS2。某硫酸廠在進行黃鐵礦成分測定時,取2.000g樣品在空氣中充分灼燒(假設雜質不參加反應),將生成的SO2氣體與足量Fe2(SO4)3溶液完全反應后,用濃度為0.3360mol·L-1的KMnO4標準溶液滴定至終點,消耗KMnO4溶液25.00mL。
已知:①4FeS2+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
②SO2+2Fe3++2H2O→SO42-+2Fe2++4H+
③MnO4-+5Fe2++8H+→Mn2++5Fe3++4H2O
(1)樣品中FeS2的質量分數是 。(用小數表示,保留三位,下同)
(2)煅燒1000 t該黃鐵礦生產出997.9 t硫酸銨,若黃鐵礦制取硫酸時的利用率為0.800,則在制取硫酸銨時硫酸的利用率為 。
(3)為使黃鐵礦充分燃燒,工業上使用過量空氣(設空氣中O2的體積分數為0.200),當空氣過量20%時,煅燒后氣體中SO2的體積分數是多少?
(4)若接觸室導出的氣體中含體積分數為0.0672的SO3。把出口氣體送進吸收塔,用質量分數為0.980的硫酸吸收,可得到“發煙H2SO4”(H2SO4和SO3的混合物,其中含質量分數為0.200的SO3)。計算吸收106 m3出口氣體(已折算為標準狀況)所需要質量分數為0.980的硫酸的質量。
 2Fe2O3+8SO2
2Fe2O3+8SO2 2Fe2O3+8SO2。把2g含雜質(不可燃)的黃鐵礦試樣在氧氣中燃燒后得殘渣1.52g。此黃鐵礦的純度為()。
2Fe2O3+8SO2。把2g含雜質(不可燃)的黃鐵礦試樣在氧氣中燃燒后得殘渣1.52g。此黃鐵礦的純度為()。湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com