
題目列表(包括答案和解析)

 CH3CH2OH(g)+3H2O(g) △H=a kJ/mol 在一定壓強下,測得上述反應的實驗數據如下表。
CH3CH2OH(g)+3H2O(g) △H=a kJ/mol 在一定壓強下,測得上述反應的實驗數據如下表。 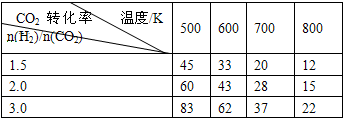


 CH3CH2OH(g)+3H2O(g) △H=a kJ/mol 在一定壓強下,測得上述反應的實驗數據如下表。
CH3CH2OH(g)+3H2O(g) △H=a kJ/mol 在一定壓強下,測得上述反應的實驗數據如下表。 

酸、堿、鹽都是電解質,在水中都能電離出離子。根據下列化合物:(1)NaOH(2)CH3COOH(3)NH4Cl(4)NH3·H2O(5)CH3COONa請回答下列問題: (1)上述幾種電解質中屬于弱電解質的是 ,溶液呈酸性的有 (填序號) (2)常溫下0.01mol/L NaOH溶液的PH= ;PH=11的CH3COONa溶液中由水電離產生的c(OH-) = (3)用離子方程式表示NH4Cl溶液呈酸性的原因 ,其溶液中離子濃度按由大到小的順序為 (4)將等PH等體積的NaOH和NH3·H2O分別稀釋m倍和n倍,稀釋后兩溶液的PH仍相等,則m n (填“大于、等于、小于”) (5)常溫下,向100 mL 0.01 mol·L-1HA溶液中逐滴加入0.02 mol·L-1MOH溶液,圖中所示曲線表示混合溶液的pH變化情況(體積變化忽略不計)。回答下列問題: 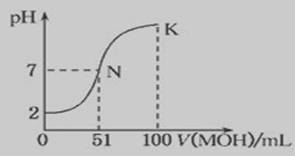
①由圖中信息可知HA為________酸(填“強”或“弱”),理由是____________ 。
② K點對應的溶液中,c(M+)+c(MOH)________2c(A-)(填“>”、“<”或“=”)。
| 溶質 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.1 | 8.8 | 11.6 | 10.3 | 11.1 | 11.3 |
| 溶質 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.1 | 8.8 | 11.6 | 10.3 | 11.1 | 11.3 |
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com