
題目列表(包括答案和解析)

 泥和普通玻璃都需用到的共同的主要原料是 ▲ 。
泥和普通玻璃都需用到的共同的主要原料是 ▲ 。 型。有機(jī)玻璃是一種 ▲ 材料(選填“硅酸鹽”或“纖維”或“塑料”)。導(dǎo)電塑料的結(jié)構(gòu)可表示為
型。有機(jī)玻璃是一種 ▲ 材料(選填“硅酸鹽”或“纖維”或“塑料”)。導(dǎo)電塑料的結(jié)構(gòu)可表示為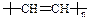 ,則其單體的結(jié)構(gòu)簡(jiǎn)式為 ▲ 。
,則其單體的結(jié)構(gòu)簡(jiǎn)式為 ▲ 。()食品和藥品關(guān)系人的生存和健康。
①市場(chǎng)上銷(xiāo)售的食鹽品種很多。下列食鹽中,所添加的元素不屬于人體必需微量元素的是 ▲ (填字母)。
A.加鋅鹽 B.加碘鹽 C.加鈣鹽
②纖維素被稱(chēng)為“第七營(yíng)養(yǎng)素”。食物中的纖維素雖然不能為人體提供能量,但能促進(jìn)腸道蠕動(dòng)、吸附排出有害物質(zhì)。從化學(xué)成分看,纖維素是一種 ▲ (填字母)。
A.多糖 B.蛋白質(zhì) C.脂肪
③某同學(xué)感冒發(fā)燒,他可服用下列哪種藥品進(jìn)行治療 ▲ (填字母)。
A.麻黃堿 B.阿司匹林 C.抗酸藥
(2)材料是人類(lèi)賴以生存和發(fā)展的重要物質(zhì)基礎(chǔ)。
①生產(chǎn)硅酸鹽水泥和普通玻璃都需用到的共同的主要原料是 ▲ 。
②生活中有大量的鋁制品。家用鋁鍋不能經(jīng)常用熱堿水洗滌去污,原因是(用離子方程式表示) ▲ 。
③有機(jī)玻璃受熱時(shí)會(huì)軟化,易于加工成型。有機(jī)玻璃是一種 ▲ 材料(選填“硅酸鹽”或“纖維”或“塑料”)。導(dǎo)電塑料的結(jié)構(gòu)可表示為![]() ,則其單體的結(jié)構(gòu)簡(jiǎn)式為 ▲ 。
,則其單體的結(jié)構(gòu)簡(jiǎn)式為 ▲ 。
(3)保護(hù)環(huán)境、保護(hù)地球是人類(lèi)共同的呼聲。
①向煤中加入石灰石作為脫硫劑,可以減少煤燃燒時(shí)產(chǎn)生的SO2。發(fā)生反應(yīng)的化學(xué)方程式為 ▲ 。
②天然水中含有的細(xì)小懸浮顆粒可以用 ▲ 做混凝劑(寫(xiě)名稱(chēng))進(jìn)行凈化處理。工業(yè)廢水中含有的Cr3+離子,可用熟石灰作沉淀劑,在pH為8~9時(shí)生成沉淀而除去,該反應(yīng)的離子方程式是 ▲ 。
③城市餐飲業(yè)會(huì)產(chǎn)生大量污染環(huán)境的“地溝油”。“地溝油”的主要成分是油脂。綜合利用“地溝油”的一種方法是將“地溝油”中的油脂水解以獲取甘油和 ▲ 。生活中會(huì)產(chǎn)生大量廢棄塑料,將廢棄塑料進(jìn)行 ▲ 處理,可以獲得乙烯、丙烯等化工原料。
(14分)近年來(lái),隨著我國(guó)經(jīng)濟(jì)的快速發(fā)展,對(duì)電力的需求越來(lái)越高,這也促進(jìn)了我國(guó)電力工業(yè)高速發(fā)展,但我國(guó)電力結(jié)構(gòu)中,火電比重非常大,占發(fā)電裝機(jī)總?cè)萘康?5%以上,且火電比重還在逐年上升。火力發(fā)電廠釋放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等氣體會(huì)造成環(huán)境污染。對(duì)燃煤廢氣進(jìn)行脫硝、脫硫和脫碳等處理,可實(shí)現(xiàn)綠色環(huán)保、節(jié)能減排、廢物利用等目的。
(1)脫硝。利用甲烷催化還原NOx:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g);ΔH1=-574kJ·mol-1
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g);ΔH2=-1160kJ·mol-1
甲烷直接將NO2還原為N2的熱化學(xué)方程式為: 。
(2)脫碳。將CO2轉(zhuǎn)化為甲醇的熱化學(xué)方程式為:
CO2(g)+3H2(g)CH3OH(g)+H2O(g);ΔH3
①取五份等體積CO2和H2的混合氣體(物質(zhì)的量之比均為1∶3),分別加入溫度不同、容積相同的恒容密閉容器中,發(fā)生上述反應(yīng),反應(yīng)相同時(shí)間后,測(cè)得甲醇的體積分?jǐn)?shù)φ(CH3OH)與反應(yīng)溫度T的關(guān)系曲線如右圖所示,則上述CO2轉(zhuǎn)化為甲醇的反應(yīng)的ΔH3 0(填“>”、“<”或“=”)。
②在一恒溫恒容密閉容器中充入1mol CO2和3mol H2,進(jìn)行上述反應(yīng)。測(cè)得CO2和CH3OH(g)的濃度隨時(shí)間變化如下圖所示。下列說(shuō)法正確的是 (填字母代號(hào))。
A.第10min后,向該容器中再充入1mol CO2和3mol H2,則再次達(dá)到平衡時(shí)c(CH3OH)=1.5mol·L-1
B.0~10min內(nèi),氫氣的平均反應(yīng)速率為0.075mol/(L·min)
C.達(dá)到平衡時(shí),氫氣的轉(zhuǎn)化率為0.75
D.升高溫度將使n(CH3OH)/n(CO2)減小
③甲醇?jí)A性燃料電池工作時(shí)負(fù)極的電極反應(yīng)式可表示為 。
(3)脫硫。某種脫硫工藝中將廢氣經(jīng)處理后,與一定量的氨氣、空氣反應(yīng),生成硫酸銨和硝酸銨的混合物作為副產(chǎn)品化肥。設(shè)煙氣中的SO2、NO2的物質(zhì)的量之比為1∶1,則該反應(yīng)的化學(xué)方程式為: 。
(4)硫酸銨和硝酸銨的水溶液的pH<7,其中原因可用一個(gè)離子方程式表示為: ;在一定物質(zhì)的量濃度的硝酸銨溶液中滴加適量的NaOH溶液,使溶液的pH=7,則溶液中:c(Na+)+c(H+) c(NO)+c(OH-)(填寫(xiě)“>”“=”或“<”)。
(14分)近年來(lái),隨著我國(guó)經(jīng)濟(jì)的快速發(fā)展,對(duì)電力的需求越來(lái)越高,這也促進(jìn)了我國(guó)電力工業(yè)高速發(fā)展,但我國(guó)電力結(jié)構(gòu)中,火電比重非常大,占發(fā)電裝機(jī)總?cè)萘康?5%以上,且火電比重還在逐年上升。火力發(fā)電廠釋放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等氣體會(huì)造成環(huán)境污染。對(duì)燃煤廢氣進(jìn)行脫硝、脫硫和脫碳等處理,可實(shí)現(xiàn)綠色環(huán)保、節(jié)能減排、廢物利用等目的。
(1)脫硝。利用甲烷催化還原NOx:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g);ΔH1=-574kJ·mol-1
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g);ΔH2=-1160kJ·mol-1
甲烷直接將NO2還原為N2的熱化學(xué)方程式為: 。
(2)脫碳。將CO2轉(zhuǎn)化為甲醇的熱化學(xué)方程式為: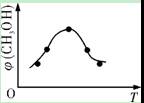
CO2(g)+3H2(g) CH3OH(g)+H2O(g);ΔH3
CH3OH(g)+H2O(g);ΔH3
①取五份等體積CO2和H2的混合氣體(物質(zhì)的量之比均為1∶3),分別加入溫度不同、容積相同的恒容密閉容器中,發(fā)生上述反應(yīng),反應(yīng)相同時(shí)間后,測(cè)得甲醇的體積分?jǐn)?shù)φ(CH3OH)與反應(yīng)溫度T的關(guān)系曲線如右圖所示,則上述CO2轉(zhuǎn)化為甲醇的反應(yīng)的ΔH3 0(填“>”、“<”或“=”)。
②在一恒溫恒容密閉容器中充入1mol CO2和3mol H2,進(jìn)行上述反應(yīng)。測(cè)得CO2和CH3OH(g)的濃度隨時(shí)間變化如下圖所示。下列說(shuō)法正確的是 (填字母代號(hào))。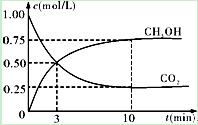
| A.第10min后,向該容器中再充入1mol CO2和3mol H2,則再次達(dá)到平衡時(shí)c(CH3OH)=1.5mol·L-1 |
| B.0~10min內(nèi),氫氣的平均反應(yīng)速率為0.075mol/(L·min) |
| C.達(dá)到平衡時(shí),氫氣的轉(zhuǎn)化率為0.75 |
| D.升高溫度將使n(CH3OH)/n(CO2)減小 |
百度致信 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專(zhuān)區(qū) | 電信詐騙舉報(bào)專(zhuān)區(qū) | 涉歷史虛無(wú)主義有害信息舉報(bào)專(zhuān)區(qū) | 涉企侵權(quán)舉報(bào)專(zhuān)區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com