
題目列表(包括答案和解析)
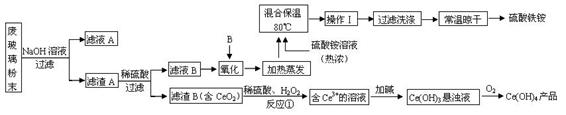
(13分)平板電視顯示屏生產過程中產生大量的廢玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物質)。某課題以此粉末為原料,設計如下工藝流程對資源進行回收,得到Ce(OH)4和硫酸鐵銨:
已知:
ⅰ.酸性條件下,鈰在水溶液中有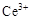 、
、 兩種主要存在形式,
兩種主要存在形式,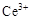 易水解,
易水解, 有較強氧化性。
有較強氧化性。
ⅱ.CeO2不溶于稀硫酸
ⅲ.硫酸鐵銨[aFe2(SO4) 3·b(NH4) 2SO4·cH2O]廣泛用于水的凈化處理。
(1).操作Ⅰ的名稱是 ,檢驗硫酸鐵銨溶液中含有NH4+的方法是: 。
(2).反應①之前先要洗滌濾渣B,其目的是為了除去 (填離子符號)。
(3).寫出反應①的化學方程式 。
(4).用滴定法測定制得的Ce(OH)4產品純度。
滴定時所用定量儀器的讀數精確為 ;若所用FeSO4溶液在空氣中露置一段時間后再進進行滴定,則測得該Ce(OH)4產品的質量分數 。(填“偏大”、“偏小”或“無影響”)
(5).稱取14.00g硫酸鐵銨樣品,將其溶于水配制成100mL溶液,分成兩等份,向其中一份加入足量NaOH溶液,過濾洗滌沉淀并烘干灼燒至恒重得到1.60g固體;向另一份溶液中加入0.5mol/L Ba(NO3)2溶液100mL,恰好完全反應。則該硫酸鐵銨的化學式為 。
 、
、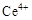 兩種主要存在形式,
兩種主要存在形式, 易水解,
易水解,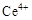 有較強氧化性。
有較強氧化性。
⑴.玻璃棒是化學實驗中常用的儀器,其作用是用于攪拌、過濾或轉移液體時引流。下列有關實驗過程中,肯定不需要使用玻璃棒進行操作的是 ▲ 。(可以多選)
A.用pH試紙測定Na2CO3溶液的pH
B.從氯酸鉀和二氧化錳制取氧氣的剩余固體中提取KCl
C.實驗室用新制的FeSO4溶液和預處理過的NaOH溶液制備Fe(OH)2白色沉淀
D.配制一定物質的量濃度的氯化鈉溶液
E.取某溶液做焰色反應實驗,說明該溶液中含有鈉元素。
F.用適量的蔗糖、濃硫酸和水在小燒杯中進行濃硫酸的脫水性實驗。
G.促使過飽和的硝酸鉀溶液析出晶體
H.用傾析法進行分離、洗滌顆粒較大的沉淀。
⑵.下列實驗能達到實驗目的且符合安全要求的是 ▲ 。(可以多選)
⑶. 化學實驗的微型化可有效地減少污染,實現化學實驗綠色化的要求。某學生按下列操作做一個實驗:在一塊下襯白紙的玻璃片的不同位置分別滴加濃度為0.1 mol·L-1的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每種液滴彼此分開,圍成半徑小于表面皿的圓形(如右圖所示),在圓心處放置2粒芝麻粒大小的KMnO4晶體,向KMnO4晶體中滴加一滴濃鹽酸,再立即將表面皿蓋好。已知:2KMnO4+16HCl(濃)===2KCl+2MnCl2+5Cl2↑+8H2O
化學實驗的微型化可有效地減少污染,實現化學實驗綠色化的要求。某學生按下列操作做一個實驗:在一塊下襯白紙的玻璃片的不同位置分別滴加濃度為0.1 mol·L-1的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每種液滴彼此分開,圍成半徑小于表面皿的圓形(如右圖所示),在圓心處放置2粒芝麻粒大小的KMnO4晶體,向KMnO4晶體中滴加一滴濃鹽酸,再立即將表面皿蓋好。已知:2KMnO4+16HCl(濃)===2KCl+2MnCl2+5Cl2↑+8H2O
①.e處發生反應的離子方程式為 ▲ ,該反應中發生反應的氧化劑和還原劑的物質的量
之比為 ▲ 。
②.b處的實驗現象為 ▲ ,d處的實驗現象為 ▲ 。
③.c處反應的化學方程式為 ▲ ,標準狀況下,當有0.224 L Cl2被NaOH溶液吸收后,
轉移電子的物質的量為 ▲ mol。
④.通過該實驗能否比較Cl2、FeCl3、KMnO4三種物質氧化性的強弱? ▲ (填“能”或
“不能”),若能,其氧化性由強到弱的順序是 ▲ 。
(1)下列敘述中正確的是………………………………( )
A.用酒精萃取溴水中的溴時,可用分液漏斗待靜置分層后分液。
B.向酒精燈中添加酒精時,需在熄滅后,用小漏斗向酒精燈中添加滿酒精。
![]() C.稀釋濃硫酸時,應將濃H2SO4沿燒杯壁慢慢加入水中,并不斷攪拌。
C.稀釋濃硫酸時,應將濃H2SO4沿燒杯壁慢慢加入水中,并不斷攪拌。
D.稱取NaOH固體時,不能直接放在托盤上,而應用稱量紙稱量,并慢慢稱取以使稱量更準確。
E.見光易分解的藥品如濃HNO3、AgNO3等應保存在棕色瓶中,并置于陰暗處。
F.過濾過程中洗滌沉淀時,應向沉淀上加水并不斷攪拌,使水自然流下,并重復2—3次。
(2)右圖是滴定管的一部分(每小格為0.1mL),圖中液面的讀數為 mL;如果右圖是量筒的一部分(每小格為0.1mL),則圖中液面的讀數為 mL。

湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com