
題目列表(包括答案和解析)
 最近霧霾天氣肆虐我國大部分地區.其中SO2是造成空氣的污染的主要原因,利用鈉堿循環法可除去SO2.
最近霧霾天氣肆虐我國大部分地區.其中SO2是造成空氣的污染的主要原因,利用鈉堿循環法可除去SO2.| O | 2- 3 |
| O | - 3 |
| O | - 3 |
| O | 2- 3 |
N(SO
|
91:9 | 1:1 | 1:91 | ||||
| pH | 8.2 | 7.2 | 6.2 |
2- 3 |
- 3 |
- 3 |
2- 3 |
2- 3 |
2- 3 |
- 3 |
(8分)最近霧霾天氣又開始肆虐我國大部分地區。其中SO2是造成空氣污染的主要原因,利用鈉堿循環法可除去SO2。
(1)鈉堿循環法中,吸收液為Na2SO3溶液,該吸收反應的離子方程式是
(2)已知H2SO3的電離常數為 K1=1.54×10-2 , K2=1.02×10-7, H2CO3的電離常數為 K1=4.30×10-7, K2= 5.60×10-11,則下列微粒可以共存的是_____________。
A.CO32- HSO3- B.HCO3- HSO3-
C.SO32- HCO3- D.H2SO3 HCO3-
(3)吸收液吸收SO2的過程中,pH隨n(SO3²﹣):n(HSO3﹣)變化關系如下表:
|
n(SO3²﹣):n(HSO3﹣) |
91 :9 |
1 :1 |
1 :91 |
|
pH |
8.2 |
7.2 |
6.2 |
①上表判斷NaHSO3溶液顯 性,從原理的角度解釋原因
②在NaHSO3溶液中離子濃度關系不正確的是(選填字母):
A.(Na+)= 2c(SO32-)+ c(HSO3-),
B.(Na+)> c(HSO3-)> c(H+)> c(SO32-)> c(OH-),
C.(H2SO3)+ c(H+)= c(SO32-)+ (OH-),
D.(Na+)+ c(H+)= 2 c(SO32-)+ c(HSO3-)+ c(OH-)
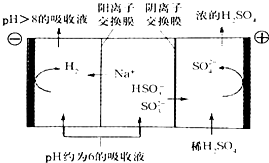
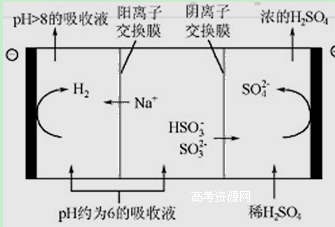
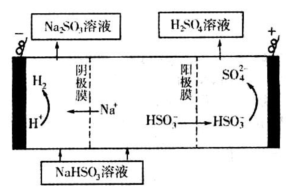
(4)當吸收液的pH降至約為6時,需送至電解槽再生 。再生示意圖如下:

① 吸收液再生過程中的總反應方程式是 。
② 當電極上有1mol電子轉移時陰極產物為 克.
(8分)最近霧霾天氣又開始肆虐我國大部分地區。其中SO2是造成空氣污染的主要原因,利用鈉堿循環法可除去SO2。
(1)鈉堿循環法中,吸收液為Na2SO3溶液,該吸收反應的離子方程式是
(2)已知H2SO3的電離常數為 K1=1.54×10-2 , K2=1.02×10-7, H2CO3的電離常數為 K1=4.30×10-7, K2= 5.60×10-11,則下列微粒可以共存的是_____________。
A.CO32- HSO3- B.HCO3- HSO3-
C.SO32- HCO3- D.H2SO3 HCO3-
(3)吸收液吸收SO2的過程中,pH隨n(SO3²﹣):n(HSO3﹣)變化關系如下表:
| n(SO3²﹣):n(HSO3﹣) | 91 :9 | 1 :1 | 1 :91 |
| pH | 8.2 | 7.2 | 6.2 |
 N2(g)+CO2(g)某研究小組向恒容密閉容器中加入一定量的活性炭和NO,恒溫(T℃)條件下反應,反應進行到不同時間測得各物質的濃度如下:
N2(g)+CO2(g)某研究小組向恒容密閉容器中加入一定量的活性炭和NO,恒溫(T℃)條件下反應,反應進行到不同時間測得各物質的濃度如下:| 濃度(mol/L) 時間(min) | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
(10 分)SO2和NOx的排放是造成酸雨的兩大罪魁禍首。下圖表示了某地區在1940~2002年間,空氣中SO2和NOx含量因燃料燃燒、工業生產、交通運輸以及其他因素的影響而發生變化的基本統計數據。
(1)結合上圖數據,判斷下列說法正確的是 ▲ 。
| A.在交通運輸中排放的NOx與燃料的不充分燃燒有關 |
| B.在上世紀60年代以前,在交通運輸中排放的SO2主要是使用燃煤的內燃機所致 |
| C.近年來在工業生產中SO2排放量的下降,主要是減少了燃燒的煤的質量 |
| D.隨著汽車工業的發展,在形成酸雨的因素中,NOx所占比重在逐漸增大 |
 N2 + 2CO2將有害的污染物轉化為可參與大氣循環的N2和CO2。
N2 + 2CO2將有害的污染物轉化為可參與大氣循環的N2和CO2。| 時間/h | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol·L-1 | 1.00×10-3 | 4.5×10-4 | 2.5×10-4 | 1.5×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol·L-1 | 3.6×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |



 在上述條件下反應能夠自發進行,則反應的
在上述條件下反應能夠自發進行,則反應的 ▲ 0(“>”、“<”、“=”)。
▲ 0(“>”、“<”、“=”)。 在該溫度下,反應的平衡常數K= ▲ 。
在該溫度下,反應的平衡常數K= ▲ 。湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com