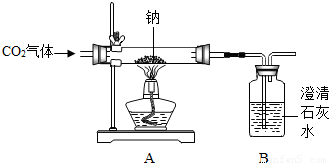
某化學課外興趣小組為探究Na與CO
2的反應進行了如下實驗(實驗部分裝置如右圖所示):向盛有Na的裝置A中通入純凈、干燥的CO
2,當觀察到裝置B中剛好出現渾濁時,點燃酒精燈,同時繼續緩緩通入CO
2,Na劇烈燃燒,產生白煙,燃燒結束后裝置A中有黑色固體和白色固體生成.
【資料卡】
(1)K、Ca、Na等活潑金屬的氧化物均可與水反應生成對應的堿;
(2)鈉為銀白色金屬,過氧化鈉為淡黃色固體.
【提出問題】白色固體含有什么物質?
【猜想與假設】小李猜:白色固體含有①______;
小剛猜:白色固體含有Na
2O;
小芳猜:白色固體含有NaOH
【實驗驗證】
| 實驗操作步驟 | 實驗現象 | 實驗結論 |
| (1)取少量白色固體放入足量水中 | 白色固體完全溶解 | |
| (2)取(1)中少量溶液,加入②______ | 產生大量氣泡 | 小李的猜想成立 |
| (3)另取(1)中少量溶液③______ | ④______ | 小剛的猜想成立 |
小李和小剛一致認為小芳的猜想不成立,他們的理由是⑤______.
【反思提高】Na在CO
2中燃燒存在多個反應、生成多種物質.請你寫出其中生成物僅為一種白色固體與一種黑色固體的反應的化學方程式:⑥______ 2Na
2CO
3+C或
4Na+CO
2 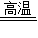
2Na
2O+C
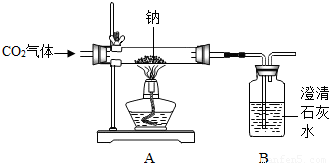

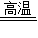 2Na2O+C
2Na2O+C
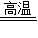 2Na2O+C
2Na2O+C