
科目: 來源: 題型:
接觸法制硫酸通常在400~500℃、常壓和催化劑的作用下,用SO2與過量的O2反應生成SO3 。2SO2(g)+O2(g)![]() 2SO3(g) △H<0,在上述條件下,SO2的轉化率約為90%。但是部分發達國家采用高壓條件獲得SO3 ,采取加壓措施的目的
2SO3(g) △H<0,在上述條件下,SO2的轉化率約為90%。但是部分發達國家采用高壓條件獲得SO3 ,采取加壓措施的目的
A.發達國家電能過量,以此消耗大量能源
B.高壓將使平衡向正反應方向移動,有利于進一步提高SO2的轉化率
C.加壓可使SO2全部轉化為SO3 ,消除SO2對空氣的污染
D.高壓有利于加快反應速率,提高生產效率
查看答案和解析>>
科目: 來源: 題型:
火箭推進器常以聯氨(N2H4)為燃料、過氧化氫為助燃劑。已知下列各物質反應的熱化學方程式:
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH1=-533.23 kJ·mol-1
H2O(g)=H2O (l) DH2=–44 kJ·mol-1
2H2O2(l)=2H2O(l)+ O2(g) DH3=–196.4 kJ·mol-1
則聯氨與過氧化氫反應的熱化學方程式可表示為
A.N2H4(g)+2H2O2(l)= N2(g)+4H2O(l) ΔH=+817.63 kJ·mol-1
B.N2H4(g)+2H2O2(l)= N2(g)+4H2O(g) ΔH=-641.63 kJ·mol-1
C.N2H4(g)+2H2O2(l)= N2(g)+4H2O(l) ΔH=-641.63 kJ·mol-1
D.N2H4(g)+2H2O2(l)= N2(g)+4H2O(g) ΔH=-817.63 kJ·mol-1
查看答案和解析>>
科目: 來源: 題型:
火箭推進器中盛有強還原劑液態肼(N2H4)和強氧化劑液態雙氧水。當把0.4mol液態肼和0.8mol H2O2混合反應,生成氮氣和水蒸氣,放出256.7kJ的熱量(相當于25℃、101 kPa下測得的熱量)。
(1)反應的熱化學方程式為 。
(2)又已知H2O(l)=H2O(g) ΔH=+44kJ/mol。則16g液態肼與液態雙氧水反應生成液態水時放出的熱量是 kJ。
(3)此反應用于火箭推進,除釋放大量熱和快速產生大量氣體外,還有一個很大的優點是 。
(4)蓋斯定律在生產和科學研究中有很重要的意義。已知把煤作為燃料可通過下列兩種途徑:
途徑I:C(s) +O2 (g) == CO2(g) △H1<0 ①
途徑II:先制成水煤氣:C(s) +H2O(g) == CO(g)+H2(g) △H2>0 ②
再燃燒水煤氣:2CO(g)+O2 (g) == 2CO2(g) △H3<0 ③
2H2(g)+O2 (g) == 2H2O(g) △H4<0 ④
則△H1、△H2、△H3、△H4的數學關系式是 。
查看答案和解析>>
科目: 來源: 題型:
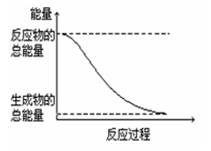
下列變化屬于放熱反應的是
A.H2O(g)=H2O(l) △H=-44.0 kJ/mol
B.2HI(g)=H2(g)+I2(g) △H=+14.9 kJ/mol
C.形成化學鍵時放出能量的化學反應
D.能量變化如右圖所示的化學反應
查看答案和解析>>
科目: 來源: 題型:
下列敘述中正確的是( )
A.1 mol CO的質量是28 g
B.硝酸的摩爾質量63 g
C.2 g氫氣所含原子數目為1 mol
D.鐵的摩爾質量在數值上等于鐵原子的相對原子質量
查看答案和解析>>
科目: 來源: 題型:
用0.01mol/LH2SO4滴定0.01mol/LNaOH溶液,中和后加水至100ml,若滴定時終點判斷有誤差:①多加了1滴H2SO4;②少加了1滴H2SO4(設1滴為0.05ml),則①和
②c(H+)之比是( )
A.10 B.50 C.5×103 D.104
查看答案和解析>>
科目: 來源: 題型:
不同濃度的硫酸與鋅反應時,硫酸可以被還原為SO2,也可被還原為氫氣。為了驗證這一事實,某同學擬用下圖裝置進行實驗(實驗時壓強為10l kPa,溫度為0℃)。
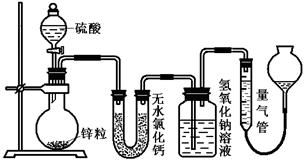
(1)若在燒瓶中放入1.30g鋅粒,與c mol/L H2SO4反應,為保證實驗結論的可靠,量氣管的適宜規格是_____________ 。
A.200 mL B.400 mL C.500mL
(2)若1.30g鋅粒完全溶解,測得盛氫氧化鈉溶液的洗氣瓶增重l.28 g ,則圓底燒瓶中發生反應的化學方程式為:_______________________________________。
(3)若燒瓶中投入a g鋅且完全反應,氫氧化鈉洗氣瓶增重b g量氣管中收集到VmL氣體,則有方程:a g/65g·mol-1=b g/64g·mol-1+V mL / 22400 mL·mol-1,其依據的原理是____________________________。
(4)若在燒瓶中投入d g鋅,再加入V L c mol/L 濃硫酸,充分反應后鋅有剩余,測得盛氫氧化鈉溶液的洗氣瓶增重m g,則整個實驗過程產生的混和氣體中H2和SO2物質的量之比 n(H2)/n(SO2)=_______________(用含字母的代數式表示)。若撤走盛有無水氯化鈣的U型管,n(H2)/n(SO2)的比值將 (填
偏大、偏小或無影響)
查看答案和解析>>
科目: 來源: 題型:
納米科技從本世紀初開始成為產業,為世人所矚目,這是因為納米粒子的直徑在幾納米到100納米之間,由納米材料作為分散質的分散系具有的性質是( )
A.能透過濾紙,屬最穩定的分散系 B.不能透過半透膜,屬介穩體系
C.有丁達爾現象,沒有布朗運動 D.一定能導電
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com