
科目: 來源: 題型:
某氯化鐵與氯化亞鐵的混合物。現要測定其中鐵元素的質量分數,實驗按以下步驟進行:

Ⅰ.請根據上面流程,回答以下問題:
(1)操作I所用到的玻璃儀器除燒杯、玻璃棒外,還必須有 、 ,(填儀器名稱)
(2)請寫出加入溴水發生的離子反應方程式 ,
(3)將沉淀物加熱,冷卻至室溫,用天平稱量其質量為b1 g,再次加熱并冷卻至室溫稱量其質量為b2 g,若b1-b2=0.3g,則接下來還應進行的操作是
。
若蒸發皿質量是W1 g,蒸發皿與加熱后固體總質量是W2 g,則樣品中鐵元素的質量分數是
Ⅱ.有同學提出,還可以采用以下方法來測定:

(1)溶解樣品改用了硫酸,而不用鹽酸,為什么
(2)選擇的還原劑是否能用鐵 (填“是”或“否”),原因是:
(3)若滴定用掉c mol/L KMnO4溶液bmL,則樣品中鐵元素的質量分數是
查看答案和解析>>
科目: 來源: 題型:
用NA表示阿伏加德羅常數,下列說法不正確 的是
A.2g氫氣所含分子數目為NA
B.在標準狀況下,NA個水分子所占有的體積約為22.4 L
C.18g水中含有的電子數為10NA
D.1L 0.3mol·L-1Na2SO4溶液中,含有Na+和SO42- 總數為0.6NA
查看答案和解析>>
科目: 來源: 題型:
中學化學中幾種常見物質的轉化關系如圖所示(圖中部分反應物或生成物及反應條件未列出)。
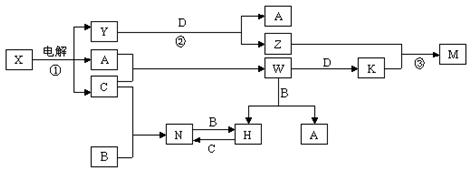
已知:A、B、C、D是單質,其余是化合物。其中B、D是常見金屬,且組成B的元素屬于過渡元素。又知A在C中點燃有蒼白色火焰,M既可溶于鹽酸又可溶于NaOH溶液。請回答下列問題:
(1)W的電子式是_______________。
(2)寫出N的化學式 。
(3)寫出下列反應的離子方程式:
反應① ,
反應③__________________________________________________________,
K溶液和過量氨水反應____________________________________________。
查看答案和解析>>
科目: 來源: 題型:
將3.9g鎂鋁合金,投入到500mL2mol·L-1的鹽酸中,金屬完全溶解,再加入4mol·L-1
的NaOH溶液,若要生成的沉淀最多,加入的這種NaOH溶液的體積是
A.125mL B.200mL C.250mL D.560mL
查看答案和解析>>
科目: 來源: 題型:
X、Y、Z三種常見的短周期元素可以形成XY2、Z2Y、XY3、Z2Y2、Z2X等化合物,已知Y的離子和Z的離子有相同的電子層結構,X離子比Y離子多一個電子層。試回答:
(1)寫出X、Y、Z三種元素的符號和名稱: ;
(2)分析Z2Y2中含有的化學鍵類型: ;
(3)寫出Z2Y2與二氧化碳反應的方程式: ;
(4)用電子式表示X和Z兩元素形成化合物的過程: 。
查看答案和解析>>
科目: 來源: 題型:
下列措施不符合節能減排的是
A.大力發展火力發電,解決廣東電力緊張問題
B.在屋頂安裝太陽能熱水器為居民提供生活用熱水
C.用石灰對煤燃燒后形成的煙氣脫硫,并回收石膏
D.用雜草、生活垃圾等有機廢棄物在沼氣池中發酵產生沼氣,用做家庭燃氣
查看答案和解析>>
科目: 來源: 題型:
若aAm+與bBn-的核外電子排布相同,則下列關系不正確的是
A.b=a-n-m B.離子半徑Am+<Bn-
C.原子半徑A<B D.A的原子序數比B大(m+n)
查看答案和解析>>
科目: 來源: 題型:閱讀理解
(1)人們對酸堿的認識,已有幾百年的歷史,經歷了一個由淺入深、由低級到高級的認識過程。目前中學課本中的酸堿理論是1889年阿侖尼烏斯(Arrhenius)提出的電離理論。
①1905年富蘭克林(FranKlin)深入研究了水和液氨的相似性,把阿侖尼烏斯以水為溶劑的個別現象,推廣到任何溶劑,提出了酸堿溶劑理論。溶劑理論認為:凡能電離而產生溶劑正離子的物質為酸,凡能電離而產生溶劑負離子的物質為堿。試寫出液氨自身電離的方程式: 。
②1923年丹麥化學家布朗斯特(Bronsted)和英國化學家勞萊(Lowey)提出質子理論。凡是能夠釋放質子(氫離子)任何含氫原子的分子或離子都是酸;凡是能夠與質子(氫離子)結合的分子或離子都是堿。
按質子理論:下列粒子在水溶液既可以看作酸又可看堿的是 。
A、H2O B、NH4+ C、OH- D、HCO3- E、CH3COO- F、Cl-
③1923年路易斯(Lewis)提出廣義的酸堿概念。凡是能給出電子對而形成化學鍵的物質都是堿;凡是能夠和電子對結合的物質都是酸。
酸(電子對接受體)+堿(電子對給予體)→反應產物,如:H++OH-→H2O。
試指出下列兩個反應中的酸或堿:
(Ⅰ)H3BO3 +H2O ![]() H++B(OH)4-,該反應中的堿是 (填H3BO3或H2O);
H++B(OH)4-,該反應中的堿是 (填H3BO3或H2O);
(Ⅱ)NaH+H2O ==NaOH+H2↑,該反應中的酸是 (填NaH 或H2O)。
(2)已知A元素原子的K、L層電子數之和比M、L層電子數之和多一個電子;B元素原子核外電子占有9個軌道,且有1個未成對電子;C元素原子核外3p亞層中3個軌道還需5個電子才能達到全充滿。D元素只有兩個電子層,且最高化合價與最低化合價的代數和為零;E原子半徑最小;F元素最外層電子排布為nSnnPn+1。按要求填寫
① B的電子排布式是: ,A、B兩元素形成的化合物的晶體類型是 。
②D元素單質的晶體類型是 ,C單質的制備方法是: 。
③E和F形成的化合物空間構型為 ,該物質比D與E形成的化合物更容易液化的原因是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com