
科目: 來源: 題型:
下列各元素的氧化物中, 既能與鹽酸反應, 又能夠與 NaOH 溶液反應的是: ( )
A.元素X: 它的原子中 M 層比L 層少 2 個電子
B.元素Y: 它的二價陽離子核外電子總數與氬原子相同
C.元素Z: 位于元素周期表中的第三周期, ⅢA 族
D.元素W: 它的焰色反應顏色呈淺紫色
查看答案和解析>>
科目: 來源: 題型:
正硼酸(H3BO3)是一種片層狀結構白色晶體,層內的H3BO3分子通過氫鍵相連(如下圖)。下列有關說法正確的是

A.正硼酸晶體屬于原子晶體
B.H3BO3分子的穩定性與氫鍵無關
C.分子中硼原子最外層為8e-穩定結構
D.含1molH3BO3的晶體中有3mol氫鍵
查看答案和解析>>
科目: 來源: 題型:
A、B、C、D、E、F均為前四周期的元素,原子序數依次增大,A的核外電子數等于其電子層數,B的最外層電子數是次外層電子數的3倍,A和C、B和E同主族,B、C、D的離子具有相同的電子層結構,D的離子是同周期中離子半徑最小的,F原子中共有6個未成對電子。
請回答下列問題:
⑴寫出下列元素的元素符號:A ▲ 、C ▲ 、E ▲ 、F ▲ 。
⑵元素A和元素B可以形成A2B物質甲,寫出甲的分子式 ▲ ,甲為 ▲ (填“極性”或“非極性”)分子。
⑶元素A和元素E形成化合物乙,用電子式表示化合物乙 ▲ ;常溫下甲為液態,乙為氣態,試解釋原因 ▲ 。
⑷元素A與元素C形成化合物丙,丙的水溶液顯堿性,試用化學方程式解釋其原因:
▲ 。
⑸元素C、元素D的最高價氧化物的水化物相互反應的離子方程式是 ▲ 。
⑹寫出元素F的外圍電子排布式 ▲ 。
查看答案和解析>>
科目: 來源: 題型:
(共10分)已知在一定條件下可實現下列轉變:
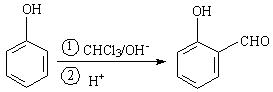
逆推法是常用的有機合成線路設計方法。所謂逆推法就是從產物逆推出原料,設計出合理的合成線路。在逆推過程中,需要逆向尋找能順利合成目標分子的中間有機物,直至選出合適的起始原料。下面是是采用逆推法設計乙酰水楊酸的合成線路:
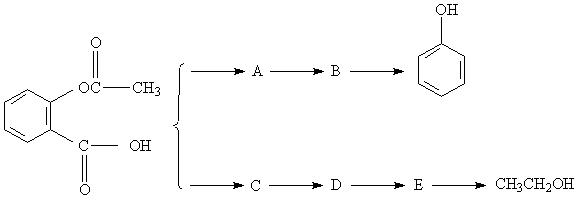
請寫出適當的中間有機物A、B、C、D、E的結構簡式:
A B
C D
查看答案和解析>>
科目: 來源: 題型:
A、B、C均為短周期元素,可形成A2C和BC2兩種化合物。A、B、C的原子序數依次遞增,A原子的K層的電子數目只有一個,B位于A的下一周期,它的最外能層電子數比K層多2個,而C原子核外的最外能層電子數比次外層電子數少2個。
(1)它們的元素符號分別為:A ;B ;C ;
(2)BC2是由 鍵組成的 (填“極性”或“非極性”)分子。
(3)畫出C原子的軌道表示式 。
(4)A2C和BC2的空間構形分別是 和 。
查看答案和解析>>
科目: 來源: 題型:
在2A+B![]() 3C+4D反應中,表示該反應速率最快的是
3C+4D反應中,表示該反應速率最快的是
A.υ(A)= 0.5 mol/(L·s) B.υ(B)= 0.3 mol/(L·s)
C.υ(C)= 0.8 mol/(L·s) D.υ(D)= 1 mol/(L·s)
查看答案和解析>>
科目: 來源: 題型:
下列溶液中的各組離子,在一定條件下可能大量共存的是
A.加入Al能放出H2的溶液中:Ca2+、NH4+、ClO-、Cl-
B.含0.1 mol/L NO3-的溶液中:H+、Fe2+、Mg2+、Br-
C.由水電離產生的c(H+)=10-13 mol/L的溶液中:Na+、K+、SO32-、AlO2-
D.無色透明的溶液中:Al3+、Na+、SO42-、HCO3-
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com