
科目: 來源: 題型:
以下是分析硫鐵礦中FeS2含量的三種方法,各方法的操作流程圖如下:
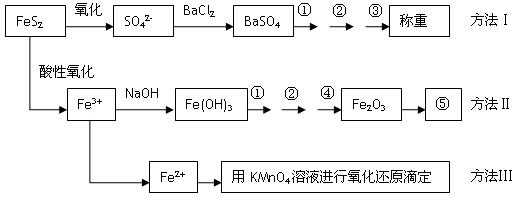
請回答下列問題:
(1)流程圖中操作①、②、③分別指的是:①___________、②__________、③________。
操作④、⑤用到的主要儀器是:④_____________、⑤_____________(每空填1-2個儀器)。
(2)判斷溶液中SO42-離子已沉淀完全的方法是
。
(3)某同學用方法Ⅲ測定試樣中Fe元素的含量,準確稱取一定量的礦石試樣,試樣經溶解、預處理后,(A)用帶有刻度的燒杯配制成100 mL試樣溶液。(B)用量筒量取25.00 mL待測溶液,(C)并置于錐形瓶中。(D)用蒸餾水洗滌滴定管后裝入KMnO4標準溶液,用該標準溶液滴定待測試樣,(E)當溶液變成淡紫紅色時,停止滴定,如30秒內不褪色,(F)讀取并計算滴定管中消耗的KMnO4標準溶液體積,計算試樣中的Fe元素含量。
請指出該實驗過程中錯誤操作步驟的編號:____________________。
(4)某同學采用方法Ⅱ分析礦石中的Fe含量,發現測定結果總是偏高,則產生誤差的可能原因是________________________________________________ _____
。
(5)稱取礦石試樣1.60 g, 按方法Ⅰ分析,稱得BaSO4的質量為4.66 g,假設礦石中的硫元素全部來自于FeS2,則該礦石中FeS2的質量分數是________。
查看答案和解析>>
科目: 來源: 題型:
根據圖中包含的信息分析,下列敘述正確的是( )
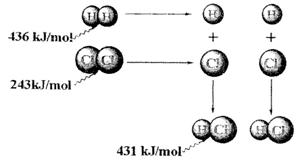
A.氫氣與氯氣反應生成1mol氯化氫氣體,反應的![]() =+248kJ/mol
=+248kJ/mol
B.436 kJ/mol是指斷開1 mol H2中的H-H鍵需要放出436 kJ的能量
C.氫氣與氯氣反應生成2mol氯化氫氣體,反應的![]() =-183kJ/mol
=-183kJ/mol
D.該反應的熱化學方程式是H2(g)+Cl2(g)==2HCl(g) ![]() =+183kJ/mol
=+183kJ/mol
查看答案和解析>>
科目: 來源: 題型:閱讀理解
化學在能源開發與利用中起到十分關鍵的作用。氫氣是一種新型的綠色能源,又是一種重要的化工原料。
Ⅰ (1)在298K、101kPa時,2g H2完全燃燒生成液態水,放出285.8kJ熱量。則表示氫氣燃燒熱的熱化學方程式為: 。
氫氧燃料電池能量轉化率高,具有廣闊的發展前景。現用氫氧燃料電池進行下圖飽和食鹽水電解實驗(圖中所用電極均為惰性電極)。分析該裝置、回答下列問題:
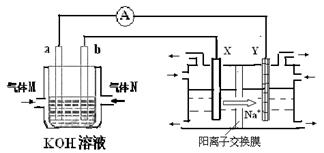
(2)氫氧燃料電池中,a電極為電池的是 (填“正極”或“負極”),氣體M的分子式 ,a電極上發生的電極反應式為: 。
(3)若右上圖裝置中盛有100mL5.0mol/LNaCl溶液,電解一段時間后須加入10.0mol/L鹽酸溶液50mL(密度為1.02g/mL)才能使溶液恢復至原來狀態。則在此電解過程中導線上轉移的電子數為 mol。(保留小數點后2位)
Ⅱ 氫氣是合成氨的重要原料。工業上合成氨的反應是:
N2(g)+3H2(g)![]() 2NH3 (g) ΔH=-92.2kJ·mol-1
2NH3 (g) ΔH=-92.2kJ·mol-1
(4)下列事實中,不能說明上述可逆反應已經達到平衡的是 。
① N2、H2 、NH3的體積分數不再改變;
② 單位時間內生成2n mol NH3的同時生成3n mol H2;
③ 單位時間內生成3n mol N—H鍵的同時生成n mol N≡N;
④ 用N2、H2 、NH3的物質的量濃度變化表示的反應速率之比為1:3:2;
⑤ 混合氣體的平均摩爾質量不再改變;
⑥ 混合氣體的總物質的量不再改變。
(5)已知合成氨反應在某溫度下2.00L的密閉容器中反應,測得如下數據:

根據表中數據計算:
①反應進行到2小時時放出的熱量為 kJ。
②0~1小時內N2的平均反應速率 mol·L-1·h-1。
③此條件下該反應的化學平衡常數K== (保留兩位小數)。
④反應達到平衡后,若往平衡體系中再加入N2、H2 和NH3各1 mol,化學平衡向 方向移動(填“正反應”或“逆反應”或“不移動”。)
查看答案和解析>>
科目: 來源: 題型:
以下說法中正確的是:
A. △H<0的反應均能自發進行。
B. △S為負值的反應均不能自發進行。
C. 冰在室溫下自動熔化成水,是熵增加的結果。
D. 碳酸氫銨固體加熱分解是一個熵減小的過程。
查看答案和解析>>
科目: 來源: 題型:
1943年,侯德榜先生研究成功了聯合制堿法,該方法不僅提高了食鹽的利用率,還在得到純堿的同時獲得了重要的副產品氯化銨。下列關于Na2CO3溶液和NH4Cl溶液的說法正確的是 ( )
A.適當升溫,兩溶液的pH均增大
B.常溫下pH=10的碳酸鈉溶液與pH=4的氯化銨溶液中水的電離程度相同
C.0.1 mol/L Na2CO3溶液中![]()
D.0.1 mol/L NH4Cl溶液中![]()
查看答案和解析>>
科目: 來源: 題型:
在二氧化碳的水溶液中存在著如下平衡:
C02(g) ![]() C02(aq) C02(aq)+H20
C02(aq) C02(aq)+H20![]() H2C03(aq)
H2C03(aq)
H2C03(aq) ![]() H+ (aq)+HCO3-(aq) HCO3-(aq)
H+ (aq)+HCO3-(aq) HCO3-(aq) ![]() H+(aq)+CO32-(aq)
H+(aq)+CO32-(aq)
下列有關說法正確的是( )
A.水中溶解的二氧化碳的濃度,夏天時比冬天時高
B.如果海水略呈堿性,海水中二氧化碳的濃度比純水高
C.氣壓升高,水中c(HCO3-)增大
D.常溫下,二氧化碳的水溶液中,由水電離出的c(H+)與c(OH-)的乘積等于1×lO-14
查看答案和解析>>
科目: 來源: 題型:
通常情況下,下列各選項中的兩個量,前者一定大于后者的是
A.物質的量濃度相等的醋酸鈉溶液和次氯酸鈉溶液的pH
B.25℃的純水和100℃的純水中的c(H+)
C.物質的量濃度相等的硫酸氫銨溶液和氯化銨溶液中c(NH4+)
D.讀取量筒中一定體積的液體時,仰視的讀數和俯視的讀數
查看答案和解析>>
科目: 來源: 題型:
已知:A、E是非金屬固體單質,氣體F能使品紅溶液褪色,C分子中有22個電子。A—H有如下轉化關系(有部分產物略去):
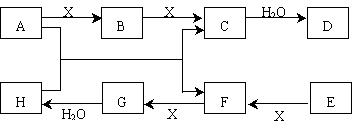
請回答:
(1)C的化學式 該分子的電子式為: 。
該分子為: (填極性、非極性)分子。
F的化學式 。
(2)X的一種同素異形體與人類生存環境密切相關,該物質的化學式是 ,
X轉化成它的方程式是: 。
(3)單質A與單質E化合生成的物質的化學式為 。
(4)寫出A+H→C+F的化學反應方程式并標出電子轉移的方向和數目:
。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com