
科目: 來源: 題型:
下列實驗設計能完成或實驗結論合理的是
A.證明一瓶紅棕色氣體是溴蒸氣還是二氧化氮,可用濕潤的碘化鉀-淀粉試紙檢驗,觀察試紙顏色的變化
B.某溶液中加入碳酸鈉溶液產生白色沉淀,再加鹽酸沉淀消失,說明該溶液中有Ca2+
C.測氯水的pH,可用玻璃棒蘸取氯水點在pH試紙上,待其變色后和標準比色卡比較
D.用核磁共振氫譜圖鑒別乙醇和乙酸
查看答案和解析>>
科目: 來源: 題型:
我國從澳大利亞進口的某高爐生鐵(用A表示)的成分如下(其余是鐵):
| C | Si | Mn | P | S |
| 4.070% | 2.900% | 0.495% | 0.165% | 0.010% |
(1)稱取100.000g A經過一系列處理(最后一步是在空氣中灼燒)后,錳全部轉變為某種氧化物,其質量為0.687g,則其化學式為 。
(2)磷肥的肥效以相當含P2O5多少來表示。煉鋼時,P元素形成爐渣Ca3(PO4)2,后者再與濃硫酸反應制得普通過磷酸鈣[即普鈣,成分是CaSO4、Ca(H2PO4)2和少量其它雜質]。若某普鈣中Ca(H2PO4)2的質量分數為45.25%,則含P2O5的質量分數為 %。
(3)錳的質量分數為30%的高錳鋼有很好的性能,可制作火車車輪。將A冶煉成含碳0.4%、含錳30%的高錳鋼(設鐵無損耗,其它雜質已除去,可補充錳),則100噸A可制得高錳鋼
噸。
(4)某煉鋼廠的煙塵成分和質量分數如下表:
| FeO | Fe2O3 | CaO | |
| 煙塵煅燒前(%) | 86.40 | 4.00 | 9.60 |
為了減少煙塵的排放,將煙塵與CO混合后在空氣中煅燒,得到鐵的氧化物和CaO的燒結物,其中CaO的質量分數為8.92%(金屬元素無損耗),燒結物分離出CaO后,鐵的氧化物的組成和物質的量之比如何 (若無確定值,請表示某組分物質的量分數的取值范圍)?
查看答案和解析>>
科目: 來源: 題型:
鋼鐵生銹的過程十分復雜,已知某鐵銹含有Fe2O3•nH2O(n≤1),還可能有Fe(OH)3和FeCO3。某學習小組做了以下實驗:
①取12.574g鐵銹隔絕空氣加熱至恒重,得到固體10.528g。
②另取6.287g鐵銹,在205.00 mL 1.000mol/L的稀硝酸中恰好完全溶解,產生NO氣體89.60 mL(標準狀況)。
(1)根據實驗①,鐵銹中是否只含Fe2O3•nH2O?試通過計算回答。
(2)根據實驗②,能否確定鐵銹中含有FeCO3?理由是什么?
(3)若n=0.8,試通過計算確定6.287g鐵銹的成分以及它們的物質的量。
查看答案和解析>>
科目: 來源: 題型:
水處理劑能使工業循環冷卻系統保持良好狀態。以下是兩種新型水處理劑的合成方法。
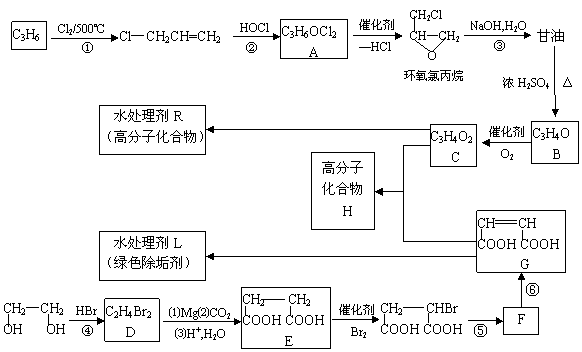 完成下列填空:
完成下列填空:
(1)寫出反應類型。反應① 反應② 。
(2)反應④通常用一種鹽和一種酸代替HBr參加反應,它們的名稱是 和 。
(3)寫出化學方程式。
B與新制氫氧化銅反應生成C ;
反應⑤ 。
(4)D轉化為E的過程中,E分子中增加的碳原子來源于 ________(寫物質的名稱)。
(5)寫出H的結構簡式 。
 (6)E有多種同分異構體,其中能發生銀鏡反應、能發生縮聚反應,還能兩分子生成六元環狀化合物的物質的結構簡式為 。
(6)E有多種同分異構體,其中能發生銀鏡反應、能發生縮聚反應,還能兩分子生成六元環狀化合物的物質的結構簡式為 。
查看答案和解析>>
科目: 來源: 題型:
已知:苯環上連有的基團不同時,新的基團可能進入間位,也可能進入鄰、對位。
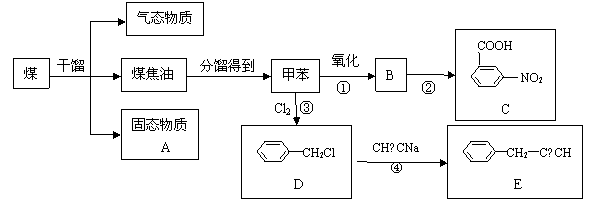
煤是非再生能源,我國煤炭儲量占能源總儲量約94%。下圖是煤干餾得到的主要產物,以及產物之一甲苯的有關反應。回答下列問題:

(1) 煤的干餾是指 。固態物質A是
(寫名稱),它是冶金工業的重要原料,還用于 (再寫一種用途)。
(2)由甲苯制備物質C時,若反應①和②的順序交換,得到的物質不是C,而可能是 (寫結構簡式,一種即可)。
(3)反應③的反應條件是 ;反應④是 反應(填反應類型)。
(4)與E含相同基團(苯基和—C≡C—)的E的同分異構體(包括E)共 種。
查看答案和解析>>
科目: 來源: 題型:
某化工廠聯合生產純堿、鎂、阻燃劑。以白云石(CaCO3·MgCO3)為原料冶煉鎂:經高溫煅燒生成的氧化物在還原爐中經1200℃用硅鐵還原生成鎂蒸汽(鐵化合價不變),鎂蒸汽經冷凝為粗鎂;同時以海水為原料制堿和制阻燃劑。具體流程如下:

![]()
|
|
|
|
|
|
|
|
(1)分別寫出A、B、C的化學式 、 、 ;沉淀池中反應的化學方程式是 。
(2)硅鐵還原生成鎂蒸汽時選擇低壓和1200℃,試分析選擇這種反應條件的原因
。
(3)精制鹵水中的MgCl2與適量石灰乳反應生成堿式氯化鎂[Mg(OH)Cl]沉淀,此時溶液中主要溶質是(寫化學式) 。
(4)描述流程中相關操作Ⅰ包括過濾、 、 。
(5)已知:Mg(OH)2(s)→MgO(s)+H2O(g)-81.5kJ;Al(OH)3(s)→0.5Al2O3(s)+1.5 H2O(g)-87.7kJ
①Mg(OH)2能起阻燃作用,其原因是 。
②等質量Mg(OH)2和Al(OH)3相比,阻燃效果較好的是 。
(6)某化工廠利用上圖所示流程聯合生產純堿、鎂、阻燃劑,試分析該生產的優點
。
查看答案和解析>>
科目: 來源: 題型:
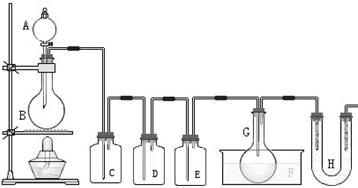
用圖示裝置制取PCl3,在E中放入足量白磷,將氯氣不間斷地通入E,氯氣與白磷就會發生反應,并放出熱量(溫度高于75℃)。已知:PCl3和 PCl5遇水強烈反應,
 它們熔沸點數據如下:
它們熔沸點數據如下:
| 熔點 | 沸點 | |
| PCl3 | -112℃ | 75℃ |
| PCl5 | 148℃ | 200℃ |
|
| ||||||
| |||||||
請根據圖中裝置回答下列問題:
(1)檢查該裝置氣密性的方法是 。
(2)為得到氯氣,若B中加入MnO2,則A中應加入 ,反應的化學方程式為___________________________________ 。
(3)若發現C中氣泡產生過猛,需要進行的操作或對裝置進行的改進是 。
(4)在反應開始時主要生成PCl3,而后來主要生成PCl5,原因可能是 ;從PCl3和PCl5的混合物中分離出PCl3的方法是 (選填序號)。
a.蒸餾 b.過濾 c.分液 d.升華
(5)生成的PCl3在G中收集,則F中盛有 ,作用是___________________________。
(6)C、D、H所盛的試劑分別是(選填序號):C ; D ; H 。
a.飽和食鹽水 b.濃硫酸 c.無水氯化鈣 d.堿石灰
(7)如果E中反應放熱較多,G處的導管可能發生堵塞,其原因是 。
查看答案和解析>>
科目: 來源: 題型:閱讀理解
大氣固氮(閃電時N2轉化為NO)和工業固氮(合成氨)是固氮的重要形式。下表列舉了不同溫度下大氣固氮和工業固氮的部分K值(K表示平衡常數):
| N2+O2 | N2+3H2 | |||
| 溫度 | 25℃ | 2000℃ | 25℃ | 400℃ |
| K | 3.84×10-31 | 0.1 | 5×108 | 200 |
(1)固氮是指 的過程,自然界固氮的另一途徑為 。
(2)根據表中的數據,并結合所學知識分析,下列說法正確的是 。
a.人類大規模模擬大氣固氮實際意義很小
b.常溫下,大氣固氮與工業固氮完成程度相差很大
c.兩種固氮都是放熱反應 d.在常溫下,大氣固氮幾乎不可能,而工業固氮很容易進行
(3)為研究反應條件的改變對化學平衡移動的影響,將N2和H2在一固定體積的密閉容器中進行反應,得到如下的圖像。下列有關條件改變(每次只改變一個條件)的說法,正確的是 。
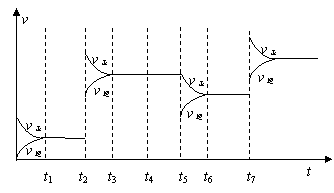 a.t2可能是增加了原料的物質的量
a.t2可能是增加了原料的物質的量
b.t4可能是充入了He氣
c.t5是從反應體系中分離出氨氣
d.t7時可能是升高溫度,使平衡向
正反應方向移動
(4)目前工業固氮采用的是哈伯法,即在
20~50MPa的高壓和500℃左右的高溫下,并用鐵觸媒作為催化劑。俄勒岡大學的化學家使用了一種名為trans-Fe(DMeOPrPE)的新催化劑,在常溫下合成氨,反應的化學方程式為:N2 +3H2![]() 2NH3 。有關說法正確的是 。
2NH3 。有關說法正確的是 。
a.新法不需要高溫條件,可節約大量能源
b.新法能在常溫下進行是因為不需要斷裂化學鍵
c.在相同溫度下不同的催化劑其催化活性不同
查看答案和解析>>
科目: 來源: 題型:
已知溶液中:還原性HSO3->I-,氧化性IO3-> I2 > SO42-。
在含3 molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3
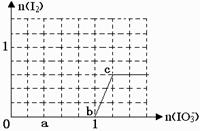 和析出的I2的物質的量的關系曲線如右圖所示,試回答下列問題:
和析出的I2的物質的量的關系曲線如右圖所示,試回答下列問題:
(1)寫出a點反應的離子方程式 ;
反應中還原劑是 ;被還原的元素是 。
(2)寫出b點到c點反應的離子方程式 。
(3)當溶液中的I-為0.4 mol時,加入的KIO3為 mol 。
(4)若往100 mL1mol/L的KIO3溶液中滴加NaHSO3溶液,反應開始時的離子方程式為
。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com