
科目: 來源: 題型:
某研究性學習小組查閱資料得知,漂白粉與硫酸反應可以制得氯氣,化學方程式為:Ca(ClO)2+CaCl2+2H2SO4![]() 2CaSO4+2Cl2↑+2H2O 。他們設計了如下制取氯氣并驗證其性質的實驗。
2CaSO4+2Cl2↑+2H2O 。他們設計了如下制取氯氣并驗證其性質的實驗。
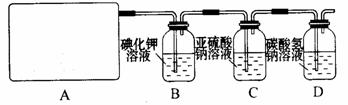
試回答:
(1)該實驗中A部分的裝置是 (填寫裝置的序號)。

(2)請你設計一個實驗,證明洗氣瓶C中的Na2SO3已經被氧化(簡述實驗步驟):
。
(3)寫出D裝置中發生反應的離子方程式 。
(4)該實驗存在明顯的缺陷,請你提出改進的方法 。
(5)該小組又進行了如下實驗:稱取漂白粉2.0 g ,研磨后溶解,配制成250 ml 溶液,取25 ml 加入到錐形瓶中,再加入過量的KI溶液和過量的H2SO4溶液,靜置。待完全反應后,用0.1 mol/L的Na2S2O3溶液作標準溶液滴定反應生成的碘,已知反應式為:
2Na2S2O3 + I2 = Na2S4O6 + 2NaI
反應完成時,共用去Na2S2O3 20.0 ml。則該漂白粉中Ca(ClO)2的質量分數為:
查看答案和解析>>
科目: 來源: 題型:
實驗室要配制1mol/L的稀硫酸250mL,回答下列問題:
(1)需要98%密度為1.84g/cm3的濃硫酸 mL
(2)配制時,必須使用的儀器有 (填代號)
①燒杯 ②100 mL量筒 ③20 mL量筒 ④1000 mL容量瓶 ⑤250 mL容量瓶 ⑥托盤天平(帶砝碼) ⑦玻璃棒 還缺少的儀器是 。
(3)配制時,該實驗兩次用到玻璃棒,其作用分別是 、 。
(4)配制過程中出現以下情況,對所配溶液濃度有何影響(填“偏高”“偏低”“不影響”)
①沒有洗滌燒杯和玻璃棒。 。
②如果加水超過了刻度線,取出水使液面恰好到刻度線。 。
③容量瓶沒有干燥。
查看答案和解析>>
科目: 來源: 題型:
現有m g某氣體,它由雙原子分子構成,它的摩爾質量為M g· mol-1。若阿伏加德羅常數用NA表示,則:
(1)該氣體的物質的量為________mol。 (2)該氣體所含原子總數為_______ 個。
(3)該氣體在標準狀況下的體積為_________L。
(4)該氣體溶于1L水中(不考慮反應),其溶液中溶質的質量分數為______ 。
查看答案和解析>>
科目: 來源: 題型:
有一瓶澄清溶液,可能含有NH+4、K+、
Mg2+、Ba2+、Al3+、Fe3+、SO2― 4、CO2― 3、NO― 3、Cl―、I―現進行如下實驗:
(1)測知溶液顯強酸性;
(2)取樣加少量CCl4和數滴新制氯水,CCl4層為紫紅色;
(3)另取樣滴加稀NaOH溶液,使溶液變為堿性,此過程中均無沉淀生成;
(4)取少量上述堿性溶液,加Na2CO3溶液出現白色沉淀;
(5)將實驗(3)中的堿性溶液加熱,有氣體放出,該氣體能使濕紅色石蕊試紙變藍。
問:①原溶液中肯定存在的離子是____________________;
②肯定不存在的離子是______________________________;
③不能確定是否存在的離子是______________________________。
查看答案和解析>>
科目: 來源: 題型:
將銅片投入盛有稀硫酸的試管中無反應。當加入少量硝酸鉀晶體后,試管內產生一種無色氣體,這種氣體在試管口變成紅棕色。這種無色氣體是__________。寫出有關的離子反應方程式.________________________________________________________
查看答案和解析>>
科目: 來源: 題型:
已知硫酸鉛難溶于水,也難溶于硝酸,卻可溶于醋酸銨溶液形成無色溶液,其化學方程式是 PbSO4+2CH3COONH4==Pb(CH3COO)2+(NH4)2SO4。當在Pb(CH3COO)2(醋酸鉛)溶液中通入H2S時,有黑色沉淀PbS生成。表示這個反應的有關離子方程式正確的是
A.Pb(CH3COO)2+H2S==PbS↓+2CH3COOH
B.Pb2++H2S==PbS↓+2H+
C.Pb2++2CH3COO-+H2S==PbS↓+2CH3COOH
D.Pb2++2CH3COO-+2H++S2-==PbS↓+2 CH3COOH
查看答案和解析>>
科目: 來源: 題型:
被稱為萬能還原劑的NaBH4溶于水并和水發生反應:NaBH4+2H2O=NaBO2+4H2↑,下列說法中正確的是(NaBH4中H為-1價)
A.被氧化的元素與被還原的元素質量比為1︰1 B.NaBH4是氧化劑,H2O是還原劑
C.硼元素被氧化,氫元素被還原 D. NaBH4既是氧化劑又是還原劑
查看答案和解析>>
科目: 來源: 題型:
將Cu片放入0.1mol/L FeCl3溶液中,反應一定時間后取出Cu片,溶液中c(Fe3+):c(Fe2+)=2:3,則Cu2+與Fe3+的物質的量之比
A.3:2 B.3:5 C.4:3 D.3:4
查看答案和解析>>
科目: 來源: 題型:
在濃鹽酸中H3AsO3與SnCl2反應的離子方程式為:3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62-+6M 關于該反應的說法中正確的組合是
① 氧化劑是H3AsO3; ② 還原性:Cl->As;
③ 每生成1molAs,反應中轉移電子的物質的量為3mol;
④ M為OH-;⑤ SnCl62-是氧化產物。
A.①③⑤ B.①②④⑤ C.①②③④ D.只有①③
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com