
科目: 來源: 題型:
據報道,科學家已成功合成了少量O4(其結構式是![]() ),有關O4的說法正確的是( )
),有關O4的說法正確的是( )
A.在O4分子中含有極性共價鍵 B.O4是氧的一種新的同位素
C.相同質量的O4與O3所含原子個數比為4∶3
D.O4與O3、O2都是氧元素的同素異形體高考資源網
查看答案和解析>>
科目: 來源: 題型:
將一塊銅板浸泡在一定濃度的FeCl3溶液中一段時間后取出,得到一混合溶液,某校化學興趣小組的同學為分析該混合溶液的組成,進行了如下實驗:
① 取50.0mL混合溶液,向其中加入足量的AgNO3溶液,得白色沉淀,過濾、干燥、稱量,沉淀質量為86.1 g;
② 另取50.0mL混合溶液,向其中加入1.40 g鐵粉,結果鐵粉全部溶解但未見固體析出;
③ 再取50.0mL混合溶液,向其中加入20.0 mL稀硝酸,得到一種無色氣體,其體積換算成標準狀況時為0.448 L ;
請根據以上實驗中得到的數據分析計算:
(1)原FeCl3溶液物質的量濃度(反應過程中過程中溶液體積的變化忽略不計);
(2)所得混合溶液中c(Cu2+)的取值范圍;
(3)若要進一步求得混合溶液中c(Cu2+)的具體數值,在只單獨使用AgNO3溶液、鐵粉或稀硝酸的前題下,還可測出哪些數據,必須進行哪些實驗?
查看答案和解析>>
科目: 來源: 題型:
將等物質的量的NaCl和CuSO4的溶解于水配成200mL混合溶液,通電電解到陰極剛有氣體放出時停止電解,將陽極產生的氣體在一定條件下恰好與5.6L標況下的H2反應。試求原溶液中兩種溶質的物質的量濃度。
查看答案和解析>>
科目: 來源: 題型:
2SO2(g)+O2(g) =2SO3(g)反應過程的能量變化如圖所示。已知1mol SO2(g)氧化為1mol SO3的ΔH=-99kJ·mol-1.請回答下列問題:

(1)圖中A、C分別表示 、 ,E的大小對該反應的反應熱有無影響? 。該反應通常用V2O5作催化劑,加V2O5會使圖中B點升高還是降低? ,理由是 ;
(2)圖中△H= KJ·mol-1;
(3)V2O5的催化循環機理可能為:V2O5氧化SO2時,自身被還原為四價釩化合物;四價釩化合物再被氧氣氧化。寫出該催化循環機理的化學方程式 ;
(4)如果反應速率υ(SO2)為0.05 mol·L-1·min-1,則υ(O2)= mol·L-1·min-1、υ(SO3)= mol·L-1·min-1;
(5)已知單質硫的燃燒熱為296 KJ·mol-1,計算由S(s)生成3 molSO3(g)的△H (要求計算過程)。
查看答案和解析>>
科目: 來源: 題型:
現有A、B、C、D、E、F六種化合物,已知它們的陽離子有![]() ,
,![]() 陰離子有
陰離子有![]() ,現將它們分別配成
,現將它們分別配成![]() 的溶液,進行如下實驗:
的溶液,進行如下實驗:
①測得溶液A、C、E呈堿性,且堿性為A>E>C;
②向B溶液中滴加稀氨水,先出現沉淀,繼續滴加氨水,沉淀消失;
③向D溶液中滴加![]() 溶液,無明顯現象;
溶液,無明顯現象;
④向F溶液中滴加氨水,生成白色絮狀沉淀,沉淀迅速變成灰綠色,最后變成紅褐色。
根據上述實驗現象,回答下列問題:
(1)實驗②中反應的化學方程式是
;
(2)E溶液是 ,判斷依據是
;
(3)寫出下列四種化合物的化學式:A 、C 、
D 、F .
查看答案和解析>>
科目: 來源: 題型:
有五種短周期主族元素A、B、C、D、E,已知:五種元素原子序數依次增大,其中A、E的單質在常溫下是氣體,B元素原子的最外層電子數是電子層數的2倍,D元素的單質常用于野外焊接鐵軌,C元素是所在周期主族元素中原子半徑最大的一種。
(1)試寫出A、B兩種元素形成的不含有非極性鍵的化合物的電子式: ;
(2)試寫出工業上用電解方法冶煉D單質的化學方程式 ;
(3)寫出C單質在空氣中燃燒的化學方程式,并標出電子轉移的方向和數目: ;
(4)寫出實驗室制取單質E的化學方程式: 。
查看答案和解析>>
科目: 來源: 題型:
Zn-MnO2干電池應用廣泛,其電解質溶液是ZnCl2-NH4Cl混合溶液。
(1)該電池的負極材料是 。電池工作時,電子流向 (填“正極”或“負極”)。
(2)若ZnCl2-NH4Cl混合溶液中含有雜質Cu2+,會加速某電極的腐蝕,其主要原因是 。欲除去Cu2+,最好選用下列試劑中的 (填代號)。
a.NaOH b.Zn c.Fe d.NH3·H2O
(3)MnO2的生產方法之一是以石墨為電極,電解酸化的MnSO4溶液。陰極的電極反應式是 。若電解電路中通過2mol電子,MnO2的理論產量為 。
查看答案和解析>>
科目: 來源: 題型:
某溶液中可能含有Na+、K+、Mg2+、I—、SO32—、SO42—等離子中的全部或其中的幾種。現分別進行以下實驗操作:①用潔凈的鉑絲蘸取溶液在無色火焰上灼燒,焰色呈黃色;②取原溶液,滴加少量溴水,振蕩后溶液仍為無色。③取原溶液,加入鹽酸酸化的Ba(NO3)2溶液后,產生白色沉淀。
(1)原溶液中一定存在的離子是 ,一定不存在的離子是 。
(2)上述①~③,的操作中, 是錯誤的,應改為 ,以便確定 離子的存在。
(3)為確定 離子是否存在,應補充的實驗是① ② 。
查看答案和解析>>
科目: 來源: 題型:
超音速飛機在平流層飛行時,尾氣中的![]() 會破壞臭氧層。科學家正在研究利用催化技術將尾氣中的
會破壞臭氧層。科學家正在研究利用催化技術將尾氣中的![]() 和
和![]() 轉變成
轉變成![]() 和
和![]() ,化學方程式如下:
,化學方程式如下:
![]()
為了測定在某種催化劑作用下的反應速率,在某溫度下用氣體傳感器測得不同時間的NO和CO濃度如表:
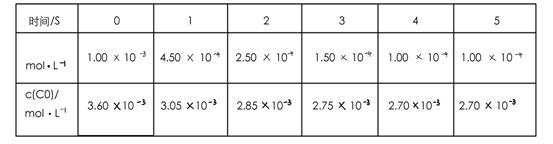 請回答下列問題(均不考慮溫度變化對催化劑催化效率的影響):
請回答下列問題(均不考慮溫度變化對催化劑催化效率的影響):
(1)在上述條件下反應能夠自發進行,則反應的![]() 0(填寫“>”、“<”、“=”。
0(填寫“>”、“<”、“=”。
(2)前2s內的平均反應速率v(N2)=_____________。
(3)在該溫度下,反應的平衡常數K= 。
(4)假設在密閉容器中發生上述反應,達到平衡時下列措施能提高NO轉化率的是 。
A.選用更有效的催化劑 B.升高反應體系的溫度
C.降低反應體系的溫度 D.縮小容器的體積
(5)研究表明:在使用等質量催化劑時,增大催化劑比表面積可提高化學反應速率。為了分別驗證溫度、催化劑比表面積對化學反應速率的影響規律,某同學設計了三組實驗,部分實驗條件已經填在下面實驗設計表中。
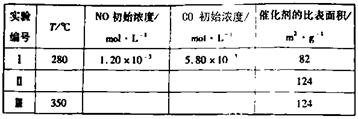
①請在上表格中填入剩余的實驗條件數據。
②請在給出的坐標圖中,畫出上表中的三個實驗條件下混合氣體中NO濃度隨時間變化的趨勢曲線圖,并標明各條曲線是實驗編號。

查看答案和解析>>
科目: 來源: 題型:閱讀理解
某實驗小組設計用50 mL1.0mol/L鹽酸跟
50mL1.1mol/L氫氧化鈉溶液在下圖裝置中進行中
和反應。在大燒杯底部墊泡沫塑料(或紙條),使
放入的小燒杯杯口與大燒杯杯口相平。然后再在大、
小燒杯之間填滿碎泡沫塑料(或紙條),大燒杯上用泡沫塑料板(或硬紙板)作蓋板,在板中間開兩個小孔,正好使溫度計和環形玻璃攪拌棒通過。通過測定反應過程中所放出的熱量可計算中和熱。試回答下列問題:

(1)本實驗中用稍過量的NaOH的原因教材中說是為保證鹽酸完全被中和。試問:鹽酸在反應中若因為有放熱現象,而造成少量鹽酸在反應中揮發,則測得的中和熱數值 (填偏高、偏低或不變);
(2)該實驗小組做了三次實驗,每次取溶液各50mL,并記錄如下原始數據。
| 實驗序號 | 起始溫度t1/℃ | 終止溫度(t2)℃ | 溫差(t2-t1)℃ | ||
| 鹽酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
| 2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
已知鹽酸、NaOH溶液密度近似為1.00g/cm3中和后混和液的比熱容 C=4.18J(g.·℃)則該反應的中和熱為△H=___________________________________;
(3)若用等濃度的醋酸與NaOH溶液反應,則測得的中和熱的數值會 (填偏高、偏低或不變),其原因是 ;
(4)影響中和熱測定結果的關鍵因素在于:
為減小實驗誤差,可采取的措有: 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com