
科目: 來源: 題型:
足量MnO2與V mL 10 mol·L-1的鹽酸共熱制氯氣,在標準狀況下制2.24 L Cl2,則V的取值應為()
A.V=20 B.20<V<40 C.V=40 D.V>40
查看答案和解析>>
科目: 來源: 題型:
硫酸銨在強熱條件下分解產生SO2、NH3、N2和H2O,反應中生成的氧化產物和還原產物的物質的量之比是( )
A.1∶3 B.2∶3 C.1∶1 D.4∶3
查看答案和解析>>
科目: 來源: 題型:
Mg、Al、Fe三種金屬的混合物與足量的稀硫酸反應生成標準狀況下的氫氣2.8 L,則金屬混合物中三種金屬的物質的量之和不可能是( )
A.0.12 mol B.0.15 mol
C.0.08 mol D.0.10 mol
查看答案和解析>>
科目: 來源: 題型:
(1)某同學用托盤天平稱量燒杯的質量,天平平衡后的狀態如下圖。由圖中可以看出,該同學在操作時的一個錯誤是____________________,燒杯的實際質量為_______________g。
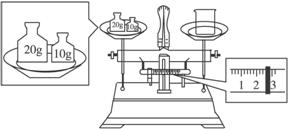
(2)指出下面實驗中各存在的兩個錯誤:
A.需配制150 mL 0.2 mol·L-1NaCl溶液,右圖是該同學轉移溶液的示意圖。

_______________________________________________________________________。
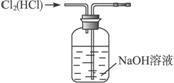
B.除去氯氣中的氯化氫氣體:
_______________________________________________________________________。
(3)用98%密度為1.84 g·cm-3的濃硫酸配制1 000 mL 0.1 mol·L-1稀硫酸。
①應用量筒量取濃硫酸___________________mL。
②配制硫酸溶液時需要用到的儀器有________________。(除量筒外,寫出其余四種)
③下列操作結果,所配溶液物質的量濃度偏低的是________________。
A.沒有將洗滌液轉移到容量瓶中
B.容量瓶洗凈后未經干燥處理
C.定容時仰視觀察液面
D.搖勻后立即觀察,發現溶液未達刻度線,再用滴管加幾滴蒸餾水至刻度線
查看答案和解析>>
科目: 來源: 題型:
“速力菲”是一種人工合成的補鐵劑,某研究性學習小組為探究其主要成分,進行了如下實驗:
(1)打開這種藥片的密封膜,發現其外觀為淡黃色。
(2)將“速力菲”投入小試管中,加入少量蒸餾水,充分振蕩后發現溶液變渾濁;慢慢加入稀硫酸后溶液變得澄清透明并顯黃色;滴加KSCN溶液,立即變為血紅色。學生甲由此斷定“速力菲”的主要成分是三價鐵鹽。
(3)學生乙的操作與甲大致相同,所不同的是他動作敏捷,且在振蕩前用橡皮塞塞緊試管口。結果發現:溶液僅顯示淡紅色。乙同學認為“速力菲”的主要成分不是三價鐵鹽而是亞鐵鹽。
(4)為了確認甲、乙的結論是否正確,學生丙將乙所得的淡紅色溶液分成兩份繼續進行實驗:

試完成下列問題:
(1)甲、乙兩位同學的結論中比較正確的是________,另一同學的結論不合理的原因是
________________________。
(2)丙的實驗①說明維生素C具有較強的________性(填“氧化”或“還原”)。
(3)寫出與②中現象對應的離子反應方程式________________________________。
(4)關于③中的實驗現象,丙同學提出了兩種假設:一種是過量的雙氧水與Fe3+結合生成了某種穩定的新物質;另一種則是過量的雙氧水將SCN-氧化了。請你設計一個實驗方案以確認哪種假設更合理________________________________。
(5)針對實驗目的,本次實驗尚未完成的任務是__________________。
查看答案和解析>>
科目: 來源: 題型:
下列各組物質在溶液中的反應,可用同一離子方程式表示的是
A.Cu(OH)2和鹽酸、Cu(OH)2和醋酸
B.BaCl2和Na2SO4、Ba(OH)2和(NH4)2SO4
C.NaHCO3和NaHSO4、Na2CO3和NaHSO4
D.過量NaHCO3和Ca(OH)2、Ca(HCO3)2和過量NaOH
查看答案和解析>>
科目: 來源: 題型:
配制一定物質的量濃度的KOH溶液時,導致濃度偏低的原因可能是
A.容量瓶中原有少量的蒸餾水
B.移液時,沒有洗滌燒杯和玻璃棒
C.溶解后沒有冷卻就轉移到容量瓶中
D.定容時俯視觀察刻度線和液面
查看答案和解析>>
科目: 來源: 題型:
設NA代表阿伏加德羅常數,下列說法正確的是
A.6.4 g金屬銅與硫反應時失去的電子數目為0.2NA
B.標準狀況下,2.24 L NO和1.12 L O2混合所得氣體中氮原子數目為0.1NA
C.在常溫常壓下11.2 L氯氣所含的原子數目為NA
D.32 g氧氣所含的原子數目為NA
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com