
科目: 來源: 題型:
【題目】常溫下,用0.10mol·L-1鹽酸分別滴定20.00 mL濃度均為0.10 mol·L-1CH3COONa溶液和NaCN溶液,所得滴定曲線如圖(忽略體積變化)。下列說法正確的是( )
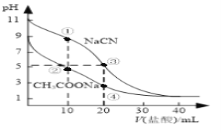
A. 溶液中陽離子的物質的量濃度之和:點②等于點③
B. 點①所示溶液中:c(CN-)+c(HCN)﹤2c(Cl-)
C. 點②所示溶液中:c(Na+)> c(Cl-)> c(CH3COO-)>c(CH3COOH)
D. 點④所示溶液中:c(Na+)+c(CH3COOH)+c(H+)>0.10mol·L-1
查看答案和解析>>
科目: 來源: 題型:
【題目】人工腎臟可用間接電化學方法除去代謝產物中的尿素[CO(NH2)2]。下列有關說法正確的是( )
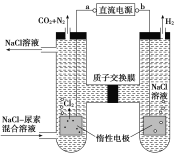
A. a為電源的負極
B. 電解結束后,陰極室溶液的pH與電解前相比將升高
C. 除去尿素的反應為:CO(NH2)2+2Cl2+H2O== N2+CO2+4HCl
D. 若兩極共收集到氣體0.6mol,則除去的尿素為0.12mol(忽略氣體溶解,假設氯氣全部參與反應)
查看答案和解析>>
科目: 來源: 題型:
【題目】[化學一有機化學基礎](13分)
對二甲苯(英文名稱p-xylene,縮寫為PX)是化學工業的重要原料。
(1)寫出PX的結構簡式 。
(2)PX 可發生的反應有 、 (填反應類型)。
(3)增塑劑(DEHP)存在如下圖所示的轉化關系,其中A 是PX的一種同分異構體。

① B 的苯環上存在2 種不同化學環境的氫原子,則B 的結構簡式是 。
② D 分子所含官能團是 (填名稱)。
③ C 分子有1個碳原子連接乙基和正丁基,DEHP的結構簡式是
(4)F 是B 的一種同分異構體,具有如下特征:
a.是苯的鄰位二取代物;b.遇FeCl3溶液顯示特征顏色;c.能與碳酸氫鈉溶液反應。
寫出F 與NaHCO3溶液反應的化學方程式
查看答案和解析>>
科目: 來源: 題型:
【題目】A、B、C、D是中學化學中常見的四種物質,且A、B、C中含有同一種元素,其轉化關系如圖所示。下列說法正確的是( )
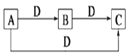
A. 若B為一種兩性氫氧化物,則D可能是強酸,也可能是強堿
B. 若A為固態非金屬單質,D為O2,則A可以為單質硫
C. 若A為強堿,D為CO2,則B的溶解度一定大于C的溶解度
D. 若A為18電子氣態氫化物,D為O2,則A只能是C2H6
查看答案和解析>>
科目: 來源: 題型:
【題目】某學習小組對人教版教材實驗“在200mL燒杯中放入20g蔗糖(C12H22O11),加入適量水,攪拌均勻,然后再加入15mL質量分數為98%濃硫酸,迅速攪拌”進行如下探究;
(1)觀察現象:蔗糖先變黃,再逐漸變黑,體積膨脹,形成疏松多孔的海綿狀黑色物質,同時聞到刺激性氣味,按壓此黑色物質時,感覺較硬,放在水中呈漂浮狀態,同學們由上述現象推測出下列結論:
①濃硫酸具有強氧化性 ②濃硫酸具有吸水性 ③濃硫酸具有脫水性④濃硫酸具有酸性 ⑤黑色物質具有強吸附性
其中依據不充分的是_________(填序號);
(2)為了驗證蔗糖與濃硫酸反應生成的氣態產物,同學們設計了如下裝置:

試回答下列問題:
①圖1的A中最好選用下列裝置_________(填編號);
②圖1的 B裝置所裝試劑是_________;D裝置中試劑的作用是_________;E裝置中發生的現象是_________;
③圖1的A裝置中使蔗糖先變黑的化學反應方程式為_________,后體積膨脹的化學方程式為:_________;
④某學生按圖2進行實驗時,發現D瓶品紅不褪色,E裝置中有氣體逸出,F裝置中酸性高錳酸鉀溶液顏色變淺,推測F裝置中酸性高錳酸鉀溶液顏色變淺的原因_________,其反應的離子方程式是_________。
查看答案和解析>>
科目: 來源: 題型:
【題目】為測定某品牌洗廁精的酸(鹽酸)含量,某學生欲用已知物質的量濃度的NaOH溶液來測定該洗廁精(鹽酸)的物質的量濃度時,選擇酚酞作指示劑。請填寫下列空白:
(1)堿式滴定管的使用方法,正確步驟的先后順序為____(填字母)。
A.用NaOH溶液潤洗儀器并加入NaOH溶液
B.放出NaOH溶液進行滴定
C.調節起始讀數
D.查漏,再水洗2~3遍
(2)用標準的NaOH溶液滴定待測的鹽酸時,左手控制堿式滴定管的玻璃球,右手搖動錐形瓶,眼睛應注視___。
(3)若滴定開始和結束時,堿式滴定管中的液面如圖所示,則所用NaOH溶液的體積為___mL。
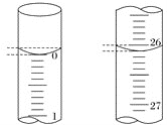
(4)某學生根據三次實驗分別記錄有關數據如下表:
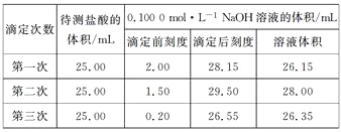
請選用其中合理的數據計算該洗廁精中酸(鹽酸)的物質的量濃度:c(HCl)=____。
(5)分析下列操作對所測洗廁精的酸(鹽酸)的濃度的影響:
A.若取待測液時,開始仰視讀數,后俯視讀數,則____(填“偏大”、“偏小”或“無影響”,下同);
B.若堿式滴定管在滴定前有氣泡,滴定后氣泡消失,則____。
查看答案和解析>>
科目: 來源: 題型:
【題目】下列各選項有機物同分異構體的數目,與分子式為C5H12O且含有兩個甲基的醇的有機物數目相同的是(不含立體異構):
A.分子式為CH2BrCl 的鹵代烴
B.分子式為C4H8O2的酯
C.![]() 的一溴代物
的一溴代物
D.立方烷(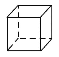 )的二氯代物
)的二氯代物
查看答案和解析>>
科目: 來源: 題型:
【題目】用NA表示阿伏加德羅常數的值。下列說法正確的是( )
A. 0.1molCH4和0.1molCl2充分反應,生成的C-Cl鍵和H-Cl鍵的數目均為0.2NA
B. 7.8gNa2S和Na2O2的混合物中所含陰離子的數目等于0.2NA
C. 18g固態水(冰)中含有的氫鍵的數目為2NA
D. 25℃時,Ksp(AgI)=1.0×10-16,則AgI飽和溶液中Ag+數目為1.0×10-8NA
查看答案和解析>>
科目: 來源: 題型:
【題目】氯化亞銅(CuCl)常用作有機合成工業中的催化劑,在空氣中迅速被氧化變成綠色;見光分解變成褐色。如圖是工業上用制作印刷電路的廢液(含Fe3+、Cu2+、Fe2+、Cl)生產CuCl的流程:
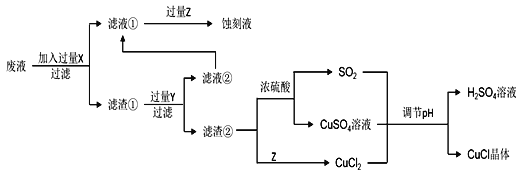
根據以上信息回答下列問題:
(1)生產過程中X的化學式為____。
(2)寫出產生CuCl的離子方程式:____。
(3)實驗探究pH對CuCl產率的影響如表所示:
pH | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
CuCl產率/% | 70 | 90 | 82 | 78 | 75 | 72 | 70 |
析出CuCl晶體最佳pH為____,當pH較大時CuCl產率變低原因是____。調節pH時,___(填“能”或“不能”)用相同pH的硝酸代替硫酸,理由是____。
(4)氯化亞銅的定量
①稱取樣品0.25g和過量的FeCl3溶液于錐形瓶中,充分溶解。
②用0.10mol·L1硫酸鈰標準溶液滴定。已知:CuCl+FeCl3=CuCl2+FeCl2、Fe2++Ce4+=Fe3++Ce3+。三次平行實驗結果如表(平行實驗結果相差不能超過1%):
平行實驗次數 | 1 | 2 | 3 |
0.25g樣品消耗硫酸鈰標準溶液的體積(mL) | 24.35 | 24.05 | 23.95 |
則樣品中CuCl的純度為_____。(結果保留三位有效數字)。
(5)由CuCl水解再熱分解可得到納米Cu2O。第一步CuCl水解的離子方程式為:CuCl(s)+H2O(l)![]() CuOH(s)+Cl (aq)+H+(aq),第二步CuOH熱分解的化學方程式為____。第一步CuCl水解反應的平衡常數K與此溫度下KW、Ksp(CuOH)、Ksp(CuCl)的關系為K=____。
CuOH(s)+Cl (aq)+H+(aq),第二步CuOH熱分解的化學方程式為____。第一步CuCl水解反應的平衡常數K與此溫度下KW、Ksp(CuOH)、Ksp(CuCl)的關系為K=____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com