
科目: 來源: 題型:
【題目】將一定量的氯氣通入300 mL 濃度為lmol/L的NaOH 溶液中恰好完全反應,加熱少許時間后溶液中形成NaCl、NaClO及NaClO3的共存體系.下列判斷不正確的是
A. n(Na+):n(C1-)可能為7:3
B. n(NaCl):n(NaClO):n(NaClO3)可能為11:1:2
C. 參加反應氯氣物質的量為0.15mol
D. 反應中轉移電子物質的量n的范圍:0.15mol<n<0.25mol
查看答案和解析>>
科目: 來源: 題型:
【題目】石蠟油分解可產生乙烯。乙烯是一種重要的化工原料,某同學設計實驗探究工業制備乙烯的原理和乙烯的主要化學性質,實驗裝置如圖所示。
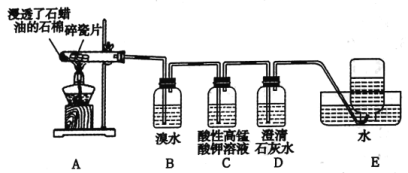
(1)用化學反應方程式解釋B裝置中的實驗現象:_________。
(2)C裝置中的現象是_________,其發生反應的類型是__________。
(3)查閱資料可知,乙烯與酸性高錳酸鉀溶液反應產生二氧化碳。根據本實驗中裝置_______(填序號)中的實驗現象可判斷該資料是否真實。
查看答案和解析>>
科目: 來源: 題型:
【題目】運用有關概念判斷下列敘述正確的是( )
A.1mol H2燃燒放出的熱量為H2的燃燒熱
B.Na2SO3和H2O2的反應為氧化還原反應
C.![]() 和
和![]() 互為同系物
互為同系物
D.BaSO4的水溶液不導電,故BaSO4是弱電解質
查看答案和解析>>
科目: 來源: 題型:
【題目】下列離子方程式與所述事實相符的是( )。
A.鍋爐水垢中的CaSO4用飽和Na2CO3溶液浸泡:![]() +CaSO4=CaCO3+
+CaSO4=CaCO3+![]()
B.向氯化亞鐵溶液中加入稀硝酸:Fe2++2H++![]() =Fe3++H2O+NO2↑
=Fe3++H2O+NO2↑
C.用鐵電極電解飽和食鹽水:2Cl-+2H2O=Cl2↑+H2↑+2OH-
D.向碳酸氫銨溶液中加入足量石灰水:Ca2++![]() +OH-=CaCO3↓+H2O
+OH-=CaCO3↓+H2O
查看答案和解析>>
科目: 來源: 題型:
【題目】設NA為阿伏加德羅常數的值。下列說法正確的是( )。
①3.9 g苯與足量的H2反應時,參與反應的碳碳雙鍵數為0.15NA
②3.1 g氧化鈉和3.9 g過氧化鈉的混合物中含有的陰離子總數為0.1NA
③1.8 g 14CH4和水蒸氣(H218O)的混合氣體中含有的電子數目為NA
④常溫下1 L 0.5 mol·L-1 NH4Cl溶液與2 L 0.25 mol·L-1 NH4Cl溶液所含![]() 的數目相同
的數目相同
⑤常溫下,4.6 g NO2和N2O4的混合氣體中所含原子總數為0.3NA
⑥將1 mol Cl2通入足量水中,溶液中HClO、Cl-、ClO-數目之和為2NA
⑦高溫下,16.8 g Fe與足量水蒸氣完全反應轉移的電子數為0.8NA
A.①②④⑥B.②⑤⑦
C.②③⑥⑦D.③⑤⑥⑦
查看答案和解析>>
科目: 來源: 題型:
【題目】某研究小組為了探究一種淺綠色鹽X(僅含四種元素,不含結晶水,M(X)<908gmol-1)的組成和性質,設計并完成了如下實驗:
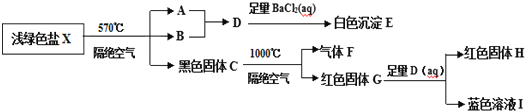
取一定量的淺綠色鹽X進行上述實驗,充分反應后得到23.3g白色沉淀E、28.8g紅色固體G和12.8g紅色固體H。
已知:①淺綠色鹽X在570℃、隔絕空氣條件下受熱分解為非氧化還原反應;
②常溫下B呈液態且1個B分子含有10個電子。
請回答如下問題:
(1)寫出B分子的電子式___。
(2)已知G溶于稀硝酸,溶液變成藍色,并放出無色氣體。請寫出該反應的離子方程式為___。
(3)在隔絕空氣、570℃溫度下加熱X至完全分解的化學反應方程式為___。
(4)一定條件下,NH3與黑色固體C發生氧化還原反應得到紅色固體和氣體丙(丙是大氣主要成分之一),寫出一個可能的化學反應方程式___。
查看答案和解析>>
科目: 來源: 題型:
【題目】(1)一種銅金合金晶體具有面心立方體結構,在晶胞中Cu原子處于面心,Au原子處于頂點,則該合金中Cu原子與Au原子數量之比為________。
(2)上述晶體具有儲氫功能,氫原子可進入到由Cu原子與Au原子構成的四面體空隙中。若將Cu原子與Au原子等同看待,該晶體儲氫后的晶胞結構與CaF2(如下圖)的結構相似,該晶體儲氫后的化學式應為________。
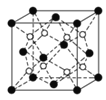
(3)立方BP(磷化硼)的晶胞結構如下圖所示,晶胞中含B原子數目為________。
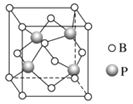
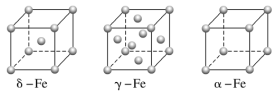
(4)鐵有δ、γ、α三種同素異形體,γ晶體晶胞中所含有的鐵原子數為________,δ、α兩種晶胞中鐵原子的配位數之比為________。
查看答案和解析>>
科目: 來源: 題型:
【題目】![]() 銅鎂合金完全溶解于50mL密度為
銅鎂合金完全溶解于50mL密度為![]() 、質量分數為
、質量分數為![]() 的濃硝酸中,得到
的濃硝酸中,得到![]() 和
和![]() 的混合氣體
的混合氣體![]() ,向反應后的溶液中加入
,向反應后的溶液中加入![]() NaOH溶液,當金屬離子全部沉淀時,得到
NaOH溶液,當金屬離子全部沉淀時,得到![]() 沉淀。下列說法不正確的是
沉淀。下列說法不正確的是![]()
A.該合金中銅與鎂的物質的量之比是2:1
B.得到![]() g沉淀時,加入NaOH溶液的體積是600mL
g沉淀時,加入NaOH溶液的體積是600mL
C.![]() 和
和![]() 的混合氣體中,
的混合氣體中,![]() 的體積分數是
的體積分數是![]()
D.該濃硝酸中![]() 的物質的量濃度是
的物質的量濃度是![]()
![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】為研究鐵質材料與熱濃硫酸的反應,某學習小組用碳素鋼(即鐵和碳的合金)進行了以下探究活動:
[探究一](1)將已去除表面氧化物的鐵釘(碳素鋼)放入冷濃硫酸中,10分鐘后移入硫酸銅溶液中,片刻后取出觀察,鐵釘表面無明顯變化,其原因是_____________________。
(2)稱取碳素鋼6.0 g放入15.0 mL濃硫酸中,加熱,充分反應后得到溶液X并收集到混合氣體Y。
①甲同學認為X中除Fe3+之外還可能含有Fe2+。若要確認其中的Fe2+,應選用_______(選填序號)。
A.KSCN溶液和氯水 B.鐵粉和KSCN溶液C.濃氨水 D.酸性KMnO4溶液
②乙同學取560 mL(標準狀況)氣體Y通入足量溴水中,發生SO2+Br2+2H2O=2HBr+H2SO4反應,然后加入足量BaCl2溶液,經適當操作后得干燥固體4.66 g。由此推知氣體Y中SO2的體積分數為_______。
[探究二]根據上述實驗中SO2體積分數的分析,丙同學認為氣體Y中還可能含有Q1和Q2兩種氣體,其中Q1氣體,在標準狀況下,密度為0.0893 g·L-1。為此設計了下列探究實驗裝置(假設有關氣體完全反應)。
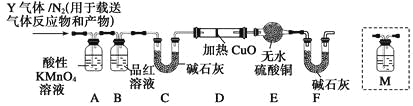
(3)裝置B中試劑的作用是_______________________。
(4)分析Y氣體中的Q2氣體是如何生成的_____________(用化學方程式表示)。
(5)已知洗氣瓶M中盛裝澄清石灰水,為確認Q2的存在,需在裝置中添加洗氣瓶M于_______(填序號)。
A.A之前 B.A—B間
C.B—C間 D.C—D間
(6)如果氣體Y中含有Q1,預計實驗現象應是___________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com