
科目: 來源: 題型:
【題目】脫落酸是一種抑制生長的植物激素,因能促使葉子脫落而得名,其結構簡式如下圖所示,則有關脫落酸的說法中正確的是
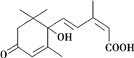
A. 脫落酸的分子式為C15H18O4
B. 脫落酸只能和醇類發生酯化反應
C. 1 mol 脫落酸最多可以和2 mol 金屬鈉發生反應
D. 1 mol脫落酸最多可以和2 mol 氫氣發生加成反應
查看答案和解析>>
科目: 來源: 題型:
【題目】乙酸乙酯是一種用途廣泛的精細化工產品。工業生產乙酸乙酯的方法很多,如圖:

下列說法正確的是
A. 反應①、②均是取代反應
B. 反應③、④的原子利用率均為100%
C. 與乙酸乙酯互為同分異構體的酯類化合物有2種
D. 乙醇、乙酸、乙酸乙酯三種無色液體可用Na2CO3溶液鑒別
查看答案和解析>>
科目: 來源: 題型:
【題目】汽車發動機工作時會產生包括CO、NOx等多種污染氣體,涉及到如下反應:
①N2(g)+O2(g)![]() 2NO(g)
2NO(g)
②2NO(g)+O2(g)![]() 2NO2(g)
2NO2(g)
③NO2(g)+CO(g)![]() CO2(g)+NO(g)
CO2(g)+NO(g)
弄清上述反應的相關機理,對保護大氣環境意義重大,回答下列問題:
(1)請根據下表數據填空:N2(g)+O2(g) ![]() 2NO(g) △H=________。
2NO(g) △H=________。
物質 | N2 | O2 | NO |
能量(kJ) | 946 | 497 | 811.25 |
(斷開1mol物質中化學鍵所需要的能量)
(2)實驗測得反應2NO(g)+O2(g)![]() 2NO2(g) △H<0的即時反應速率滿足以下關系式:
2NO2(g) △H<0的即時反應速率滿足以下關系式:
v正=k正·c2(NO)·c(O2);v逆=k逆·c2(NO2),k正、k逆為速率常數,受溫度影響
①溫度為T1時,在1L的恒容密閉容器中,投入0.6 molNO和0.3 molO2達到平衡時O2為0.2 mol;溫度為T2時,該反應存在k正=k逆,則T1_______ T2 (填“大于”、“小于”或“等于”)。
②研究發現該反應按如下步驟進行:
第一步:NO+NO![]() N2O2 快速平衡 第二步:N2O2 +O2
N2O2 快速平衡 第二步:N2O2 +O2![]() 2NO2 慢反應
2NO2 慢反應
其中可近似認為第二步反應不影響第一步的平衡,第一步反應中:v1正=k1正×c2(NO);v1逆=k1逆×c(N2O2)
下列敘述正確的是______
A.同一溫度下,平衡時第一步反應的![]() 越大反應正向程度越大
越大反應正向程度越大
B.第二步反應速率低,因而轉化率也低
C.第二步的活化能比第一步的活化能低
D.整個反應的速率由第二步反應速率決定
(3)科學家研究出了一種高效催化劑,可以將CO和NO2兩者轉化為無污染氣體,反應方程式為:2NO2(g)+4CO(g) =4CO2(g)+N2(g) △H<0
某溫度下,向10L密閉容器中分別充入0.1molNO2和0.2 molCO,發生上述反應,隨著反應的進行,容器內的壓強變化如下表所示:
時間/min | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
壓強/kPa | 75 | 73.4 | 71.95 | 70.7 | 69.7 | 68.75 | 68.75 |
回答下列問題:
①在此溫度下,反應的平衡常數Kp=_________kPa-1(Kp為以分壓表示的平衡常數,計算結果精確到小數點后2位);若保持溫度不變,再將CO、CO2氣體濃度分別增加一倍,則平衡_____(填“右移”或“左移”或“不移動”);
②若將溫度降低,再次平衡后,與原平衡相比體系壓強(p總)如何變化?_______(填“增大”、“減小”或“不變”),原因是__________。
查看答案和解析>>
科目: 來源: 題型:
【題目】許多含氮物質是農作物生長的營養物質。
(1)肼(N2H4)、N2O4常用于航天火箭的發射。已知下列反應:
①N2(g)+O2(g) =2NO(g) ΔH=+180kJ·mol-1
②2NO(g)+O2(g)![]() 2NO2(g) ΔH=-112kJ·mol-1
2NO2(g) ΔH=-112kJ·mol-1
③2NO2(g)![]() N2O4(g) ΔH=-57kJ·mol-1
N2O4(g) ΔH=-57kJ·mol-1
④2N2H4(g)+N2O4(g) =3N2(g)+4H2O(g) ΔH=-1136kJ·mol-1
則N2H4與O2反應生成氮氣與水蒸氣的熱化學方程式為_________________。
(2)一定溫度下,向某密閉容器中充入1 mol NO2,發生反應:2NO2(g)![]() N2O4(g),測得反應體系中氣體體積分數與壓強之間的關系如圖所示:
N2O4(g),測得反應體系中氣體體積分數與壓強之間的關系如圖所示:
①a、b、c三點逆反應速率由大到小的順序為_______。平衡時若保持壓強、溫度不變,再向體系中加入一定量的Ne,則平衡_______移動(填“正向”“逆向”或“不”)。
②a點時NO2的轉化率為___________,用平衡分壓代替平衡濃度也可求出平衡常數Kp,則該溫度下Kp=________Pa-1。
(3)已知在一定溫度下的可逆反應N2O4(g)![]() 2NO2(g)中,v正=k正c(N2O4),v逆=k逆c2(NO2)(k正、k逆只是溫度的函數)。若該溫度下的平衡常數K=10,則k正=______k逆。升高溫度,k正增大的倍數_______(填“大于”“小于”或“等于”)k逆增大的倍數。
2NO2(g)中,v正=k正c(N2O4),v逆=k逆c2(NO2)(k正、k逆只是溫度的函數)。若該溫度下的平衡常數K=10,則k正=______k逆。升高溫度,k正增大的倍數_______(填“大于”“小于”或“等于”)k逆增大的倍數。
(4)氨氣是合成眾多含氮物質的原料,利用H2-N2—生物燃料電池,科學家以固氮酶為正極催化劑、氫化酶為負極催化劑,X交換膜為隔膜,在室溫條件下即實現了合成NH3的同時還獲得電能。其工作原理圖如下:

則X膜為___________交換膜,正極上的電極反應式為______________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】將1 mol乙醇(其中的氧用18O標記)在濃硫酸存在條件下與足量乙酸充分反應。下列敘述不正確的是( )
A. 生成的乙酸乙酯中含有18OB. 生成的水分子中含有18O
C. 可能生成44 g乙酸乙酯D. 不可能生成90 g乙酸乙酯
查看答案和解析>>
科目: 來源: 題型:
【題目】常溫下,下列有關敘述正確的是![]()
A.飽和氯水中滴加NaOH至溶液呈中性:![]()
B.100mL![]() 的
的![]() 溶液和200
溶液和200![]() 的
的![]() 溶液所含的
溶液所含的![]() 相同
相同
C.![]() 的一元酸和
的一元酸和![]() 的一元強堿等體積混合后的溶液;
的一元強堿等體積混合后的溶液;![]()
D.常溫下,![]() 、濃度均為
、濃度均為![]() 。
。![]() 的
的![]() 、
、![]() COONa混合溶液
COONa混合溶液![]()
![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】某化學實驗小組以電鍍廢渣(Cr2O3、CuO、Fe2O3及CaO)為原料制取銅粉和K2Cr2O7。主要流程如圖:
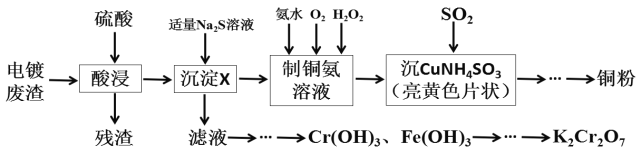
(1)加入適量Na2S溶液后生成的沉淀X為___,若加入的Na2S溶液過量,除生成X外還會發生反應的離子方程式為___。
(2)請配平[Cu(NH3)4]SO4·H2O加熱發生分解反應的化學方程式。
___[Cu(NH3)4]SO4·H2O![]() ___Cu+___NH3↑+___SO2↑+___N2↑+___H2O
___Cu+___NH3↑+___SO2↑+___N2↑+___H2O
(3)“沉CuNH4SO3”時可用如圖裝置(夾持、加熱儀器略):
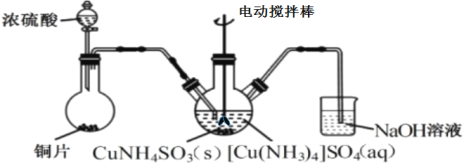
①“沉CuNH4SO3”時,反應溫度需控制在45℃,合適的加熱方式是___。
②NaOH溶液的作用是___。
(4)測定產品中K2Cr2O7含量的方法如下:稱取產品試樣2.0g配成250mL溶液,取出25.00mL于錐形瓶中,加入足量稀硫酸酸化后,再加入幾滴指示劑,用0.1000mol/L硫酸亞鐵銨(NH4)2Fe(SO4)2標準液進行滴定,重復進行三次實驗。(已知Cr2O72-被還原為Cr3+)
①若三次實驗消耗(NH4)2Fe(SO4)2標準液的平均體積為20.00mL,則所得產品K2Cr2O7的純度為___%。
②上述流程中K2Cr2O7發生氧化還原反應后所得溶液中除含有Cr3+,還含有一定濃度的Fe3+,可通過調pH的方法使兩者轉化為沉淀。假設兩種離子初始濃度均為2×10-3mo/L,當溶液中剛開始析出Cr(OH)3沉淀時,c(Fe3+)=___mo/L。{已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31}
查看答案和解析>>
科目: 來源: 題型:
【題目】設![]() 為阿伏加德羅常數的值。下列敘述錯誤的是
為阿伏加德羅常數的值。下列敘述錯誤的是![]()
![]()
A.![]() 和
和![]() 中含有的中子數均為
中含有的中子數均為![]()
B.常溫常壓下,![]() 含甲醛
含甲醛![]() 的冰醋酸中含有的原子總數為
的冰醋酸中含有的原子總數為![]()
C.常溫下,![]() 的氨水中,發生電離的水分子數為
的氨水中,發生電離的水分子數為![]()
D.一定條件下,足量氧氣通過Na單質后,若固體增重![]() ,則轉移的電子數一定為
,則轉移的電子數一定為![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】如圖表示AlCl3溶液與NaOH溶液滴加過程中微粒數量的關系曲線。 判斷下列說法不正確的是( )
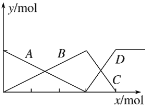
A.A線表示Al3+的物質的量的變化
B.x表示NaOH的物質的量
C.C線表示Al(OH)3的物質的量的變化
D.D線表示Al(OH)3的物質的量的變化
查看答案和解析>>
科目: 來源: 題型:
【題目】甲胺鉛碘(CH3NH3PbI3)可用作全固態鈣鈦礦敏化太陽能電池的敏化劑,該物質可由甲胺(CH3NH2)、PbI2及HI為原料來合成。請回答下列問題:
(1)制取甲胺的反應為CH3OH(g)+NH3(g)===CH3NH2(g)+H2O(g),已知該反應中相關化學鍵的鍵能數據如下表所示:

則該反應的△H=___________kJ·mol-1
(2)工業上利用水煤氣合成甲醇的反應為CO(g)+2H2(g)![]() CH3OH(g) △H<0。一定溫度下,向體積為2L的密閉容器中加人CO和H2,5min末反應達到化學平衡狀態,測得各組分濃度如下表所示。
CH3OH(g) △H<0。一定溫度下,向體積為2L的密閉容器中加人CO和H2,5min末反應達到化學平衡狀態,測得各組分濃度如下表所示。

①0~5min內,用CO表示的平均反應速率為___________。
②既能加快反應速率,又能提高氫氣轉化率的措施有___________(答一條即可)。
③能說明上述反應已達化學平衡狀態的是___________(填字母)。
A.v正(CO)=2v逆(H2)
B.混合氣體密度保持不變
C.反應容器內壓強保持不變
D.混合氣體的平均摩爾質量不變
(3)PbI2可由Pb3O4和HI反應制備,反應的化學方程式為___________。
(4)常溫下PbI2飽和溶液中c(I-)=2.0×10-3mol·L-1,則Ksp(PbI2)=___________;已知Ksp(PbS)=4.0×10-28,則反應PbI2(s)+S2-(aq)![]() PbS(s)+2I-(aq)的平衡常數K=___________。
PbS(s)+2I-(aq)的平衡常數K=___________。
(5)HI的分解反應曲線和液相法制備HI的反應曲線分別如圖1和圖2所示:

①反應H2(g)+I2(g)![]() 2HI(g)的△H___________(填“>”或“<")0。
2HI(g)的△H___________(填“>”或“<")0。
②將SO2通入碘水中會發生反應:SO2+I2+2H2O===4H++SO42-+2I-,I2+I-![]() I3-。圖2中曲線b所代表的微粒是___________(填微粒符號)。
I3-。圖2中曲線b所代表的微粒是___________(填微粒符號)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com