
科目: 來源: 題型:
【題目】在一定溫度下,將氣體X和氣體Y各![]() 充入10L恒容密閉容器中,發生反應
充入10L恒容密閉容器中,發生反應![]() ,一段時間后達到平衡。反應過程中測定的數據如表:下列說法不正確的是
,一段時間后達到平衡。反應過程中測定的數據如表:下列說法不正確的是
| 2 | 4 | 7 | 9 |
|
|
|
|
|
A.反應前2min的平均速率![]()
B.其他條件不變,升高溫度,反應達到新平衡前![]() 正
正![]() 逆
逆![]()
C.該溫度下此反應的平衡常數![]()
D.其他條件不變,再充入![]() ,平衡時X的體積分數增大
,平衡時X的體積分數增大
查看答案和解析>>
科目: 來源: 題型:
【題目】下列說法正確的是
A.麥芽糖水解的產物互為同分異構體
B.甘氨酸與苯丙氨酸互為同系物
C.CH3CH2OOCCOOCH2CH3 的名稱是乙二酸乙二酯
D.天然油脂大多是由混合甘油酯分子組成的混合物
查看答案和解析>>
科目: 來源: 題型:
【題目】設阿伏加德羅常數的值為NA,下列說法中正確的是
A.常溫常壓下,15g的—12CH3中含有中子數6NA
B.46 g乙醇和46 g甲酸含有的氧原子數均為NA
C.32g甲醇中含有C—H鍵的數目為4NA
D.標準狀況下,1L甲醛完全燃燒所生成的氣態產物的分子數為![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】實驗室用Cl2與KOH溶液反應制備KClO溶液,其裝置如下圖所示。以KClO溶液及廢鐵屑等為原料,可制備高效水處理劑聚合硫酸鐵![]() 。
。
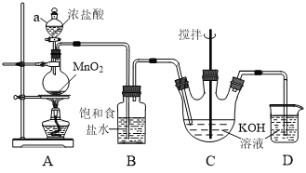
已知:C中反應是放熱反應
(1)裝置A中儀器a的名稱是______;裝置B的作用是_______。
(2)Cl2和KOH在較高溫度下反應生成KClO3,在不改變KOH溶液的濃度和體積的條件下,控制反應在0℃~5℃進行,實驗中可采取的措施是_______(回答一點即可)。
(3)裝置D發生反應的離子方程式為______。
(4)聚合硫酸鐵![]() (其中Fe元素為+3價)的組成可通過下列實驗測定:
(其中Fe元素為+3價)的組成可通過下列實驗測定:
①稱取一定質量的聚合硫酸鐵溶于稀鹽酸中,往所得溶液中滴加BaCl2溶液至沉淀完全,過濾、洗滌、干燥至恒重,得到白色固體11.65 g;
②另稱取與①等質量的聚合硫酸鐵溶于稀硫酸中,加入足量銅粉,充分反應后過濾、洗滌,將濾液和洗液合并配成250.00 mL溶液B;
③準確量取25.00 mL溶液B,用0.1000 mol·L-1的KMnO4溶液滴定至終點,消耗KMnO4溶液8.00 mL。該步反應為:![]() 。通過計算確定該聚合硫酸鐵的化學式(寫出計算過程)。______。
。通過計算確定該聚合硫酸鐵的化學式(寫出計算過程)。______。
查看答案和解析>>
科目: 來源: 題型:
【題目】現代人追求“低碳生活” ,二氧化碳的回收并利用是環保領域研究的熱點和重點。試分析并回答:
(1)有一最新美國科學家的研究成果,利用金屬鈦和某些裝置等,模仿太陽的藍色波長,使CO2慢慢發生人工“光合作用” 后,被還原成太陽能燃料——甲酸等,該化學方程式是_____________________________;
(2)另有一種用CO2生產甲醇燃料的方法:
CO2+3H2=CH3OH+H2O。已知298 K和101 kPa條件下:
CO2(g)+3H2(g)=CH3OH(g)+H2O(l) ΔH=-a kJ·mol-1;
2H2(g)+O2(g)=2H2O(l) ΔH=-b kJ·mol-1;
CH3OH(g)=CH3OH(l) ΔH=-c kJ·mol-1,
則CH3OH(l)的標準燃燒熱ΔH=________。
(3)工業上合成尿素的反應如下:
2NH3(g)+CO2(g)=CO(NH2)2(l)+H2O(l) ΔH<0,某實驗小組模擬工業上合成尿素的條件,在恒定溫度下,將氨氣和二氧化碳按2∶1的物質的量之比充入一體積為10 L的密閉容器中(假設容器體積不變,生成物的體積忽略不計),經20 min達到平衡,各物質濃度的變化曲線如圖所示。
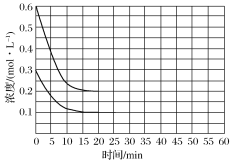
①為提高尿素的產率,下列可以采取的措施有________;
A.縮小反應容器的容積
B.升高溫度
C.平衡體系中分離出部分CO(NH2)2
D.使用合適的催化劑
②若保持平衡的溫度和壓強不變,再向容器中充入3 mol的氨氣,則此時v正________v逆(填“>”“=”或“<”),判斷理由_____________________________;
③若保持平衡的溫度和體積不變,25 min時再向容器中充入2 mol氨氣和1 mol二氧化碳,在40 min時重新達到平衡,請在上圖中畫出25~50 min內氨氣的濃度變化曲線________________。
(4)多孔Al2O3薄膜可作為催化劑載體、模板合成納米材料等用途。現以高純鋁片作為陽極,不銹鋼作為陰極,一定溶度的磷酸溶液作為電解質進行電解,即可初步制取多孔Al2O3膜。請寫出該制取過程的陽極電極反應:__________________________________________。
(5)要實現CO2直接加H2合成汽油,關鍵是_____________________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】利用廢蝕刻液(含FeCl2、CuCl2及FeCl3)制備堿性蝕刻液[Cu(NH3)4Cl2溶液]和FeCl36H2O的主要步驟:用H2O2氧化廢蝕刻液,制備氨氣,制備堿性蝕刻液[CuCl2+4NH3=Cu(NH3)4Cl2]、固液分離,用鹽酸溶解沉淀并制備FeCl36H2O。下列實驗原理和裝置不能達到實驗目的的是( )
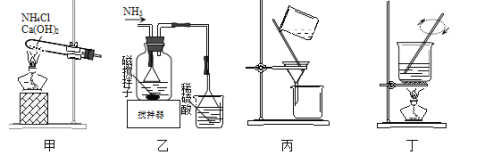
A.用裝置甲制備NH3B.用裝置乙制備Cu(NH3)4Cl2并沉鐵
C.用裝置丙分離Cu(NH3)4Cl2溶液和Fe(OH)3D.用裝置丁將FeCl3溶液蒸干制備FeCl36H2O
查看答案和解析>>
科目: 來源: 題型:
【題目】工業上用CO與H2合成甲醇,CO(g)+2H2(s)![]() CH3OH(g) △H=—90.8kJ/mol。300℃時,在容積相同的3個密閉容器中,按不同方式投入反應物,保持恒溫、恒容,測得反應達到平衡時的有關數據如下
CH3OH(g) △H=—90.8kJ/mol。300℃時,在容積相同的3個密閉容器中,按不同方式投入反應物,保持恒溫、恒容,測得反應達到平衡時的有關數據如下
容量 | 甲 | 乙 | 丙 | |
反應物投入量 | 1 molCO、2molH2 | 1mol CH3OH | 2mol CH3OH | |
平衡時數據 | CH3OH的濃度(mol/L) | c1 | c2 | c3 |
反應的能量變化 | a kJ | b kJ | c kJ | |
體系壓強(Pa) | P1 | P2 | P3 | |
反應物轉化率 | a1 | a2 | a3 | |
下列說法正確的是
A.2c1>c3B.a+b<90.8C.2P2<P3D.a1+a3<1
查看答案和解析>>
科目: 來源: 題型:
【題目】以含鋰電解鋁廢渣(主要成分為LiF、AlF3、NaF,少量CaO等)為原料,生產碳酸鋰的工藝流程如下:(已知:常溫下,LiOH可溶于水,Li2CO3微溶于水)
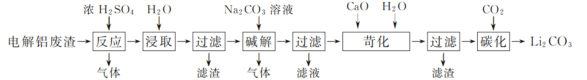
(1)含鋰電解鋁廢渣與濃硫酸在200~400 ℃條件下反應2 h,加水浸取后過濾,得到的濾渣主要成分是________(填化學式)。
(2)流程中浸取后的過濾操作需要趁熱在恒溫裝置中進行,否則會導致Li2SO4的收率下降,原因是________。(已知部分物質的溶解度數據見下表)
溫度/℃ | Li2SO4/g | Al2(SO4)3/g | Na2SO4/g |
0 | 36.1 | 31.2 | 4.9 |
10 | 35.4 | 33.5 | 9.1 |
20 | 34.8 | 36.5 | 19.5 |
30 | 34.3 | 40.4 | 40.8 |
40 | 33.9 | 45.7 | 48.8 |
(3)40℃下進行堿解反應,得到粗碳酸鋰與氫氧化鋁的混合濾渣,生成氫氧化鋁的離子方程式為________。
(4)苛化過程中加入的氧化鈣將不溶性的碳酸鋰轉化成氫氧化鋰溶液。若氧化鈣過量,則可能會造成________。
(5)碳化反應中,CO2的吸收采用了氣、液逆流的方式,這樣做的優點是________。整個工藝流程中可以循環利用的物質有________。
查看答案和解析>>
科目: 來源: 題型:
【題目】常溫下,下列各組離子在指定溶液中一定能大量共存的是( )
A. 含大量Fe3+的溶液中:Na+、Mg2+、SO42-、SCN-
B. ![]() =106的溶液中:NH4+、K+、AlO2-、NO3-
=106的溶液中:NH4+、K+、AlO2-、NO3-
C. 能使甲基橙變紅的溶液中:Cu2+、Mg2+、SO42-、Cl-
D. 1.0mol·L-1的KNO3溶液中:Fe2+、H+、Cl-、I-
查看答案和解析>>
科目: 來源: 題型:
【題目】(改編)在稀硫酸與鋅反應制取氫氣的實驗中,探究加入硫酸銅溶液的量對氫氣生成速率的影響。實驗中Zn粒過量且顆粒大小相同,飽和硫酸銅溶液用量0~4.0mL,保持溶液總體積為100.0mL,記錄獲得相同體積(336mL)的氣體所需時間,實驗結果如圖所示(氣體體積均轉化為標況下)。據圖分析,下列說法不正確的是

A.飽和硫酸銅溶液用量過多不利于更快收集氫氣
B.a、c兩點對應的氫氣生成速率相等
C.b點對應的反應速率為v(H2SO4) = 1.0×10-3 mol·L-1·s-1
D.d點沒有構成原電池,反應速率減慢
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com