
科目: 來源: 題型:
【題目】下列說法正確的是![]()
![]()
A.海水淡化的常用方法有蒸餾法、電滲析法和過濾法
B.pH相等的三種溶液:![]() 溶液
溶液![]() 溶液
溶液![]() 溶液,其濃度大小順序為
溶液,其濃度大小順序為![]()
C.在![]() 和
和![]() 的混合溶液中加入
的混合溶液中加入![]() 產生黑色沉淀,證明
產生黑色沉淀,證明![]()
D.侯式制堿法的化學方程式為![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】向濃度相等、體積均為100 mL的A、B兩份NaOH溶液中,分別通入一定量的CO2后,逐滴加入0.1 mol/L的鹽酸,產生CO2的體積(標準狀況)與所加鹽酸的體積關系如圖所示。

(1)A曲線表明,原溶液通入CO2 ________mL(標準狀況)。
(2)B曲線表明,原溶液通入CO2后,所得溶液中溶質的物質的量之比為__________。
(3)原NaOH溶液的物質的量濃度為__________。
查看答案和解析>>
科目: 來源: 題型:
【題目】化合物F是一種食品保鮮劑,可按如下途徑合成:

已知:RCHO+CH3CHO![]() RCH(OH)CH2CHO。
RCH(OH)CH2CHO。
試回答:
(1)A的結構簡式是_________,E→F的反應類型是_________。
(2)B→C反應的化學方程式為_____________。
(3)C→D所用試劑和反應條件分別是_________。E中官能團的名稱是________________。
(4)檢驗F中碳碳雙鍵的方法是_________________________。
(5)連在雙鍵碳上的羥基不穩定,會轉化為羰基,則D的同分異構體中,只有一個環的芳香族化合物有______種(除D外)。其中苯環上只有一個取代基,核磁共振氫譜有4個峰,峰面積比為3∶2∶2∶1的同分異構體的結構簡式為____________。
查看答案和解析>>
科目: 來源: 題型:
【題目】關于水溶液中的離子平衡,下列說法正確的是
A.往![]() 稀溶液中加入NaOH固體,溶液中
稀溶液中加入NaOH固體,溶液中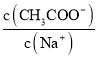 變大
變大
B.等物質的量濃度的![]() 、
、![]() 、
、![]() 三種溶液中,
三種溶液中,![]() 的大小順序為:
的大小順序為:![]()
C.常溫下![]() 的
的![]() 溶液和
溶液和![]() 的NaOH溶液等體積混合,溶液中離子濃度大小順序為:
的NaOH溶液等體積混合,溶液中離子濃度大小順序為:![]()
D.![]() 的
的![]() 溶液中:
溶液中:![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】把0.6mol X氣體和0.4mol Y氣體混合于2L容器中,發生反應:3X(g)+Y(g)== nZ(g)+2W(g),5min末已生成0.2mol W,若測知以Z濃度變化來表示的平均速率為0.03mol·L﹣1·min﹣1,計算:
(1)n的值為____;
(2)前5min內用X表示的反應速率_____;
(3)5min末Y的濃度_______。
查看答案和解析>>
科目: 來源: 題型:
【題目】常溫下,將![]() 緩慢通入100mL水中至飽和,然后向所得飽和氯水中逐滴加人
緩慢通入100mL水中至飽和,然后向所得飽和氯水中逐滴加人![]() 溶液,整個過程中pH的變化如圖所示,下列有關敘述正確的是( )
溶液,整個過程中pH的變化如圖所示,下列有關敘述正確的是( )

A.曲線③④段有離子反應:![]()
B.可依據②處數據計算所溶解的![]()
C.③處表示氯氣與氫氧化鈉溶液恰好反應完全
D.①處![]() 約為
約為![]() 處
處![]() 的兩倍
的兩倍
查看答案和解析>>
科目: 來源: 題型:
【題目】三氯氧磷(POCl3)是重要的基礎化工原料,廣泛用于制藥、染化、塑膠助劑等行業。某興趣小組模擬PCl3直接氧化法制備POCl3,實驗裝置設計如下:
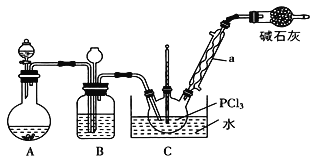
有關物質的部分性質如下表:
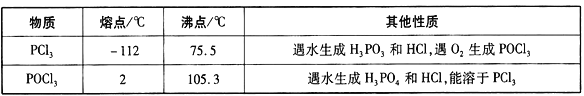
回答下列問題:
(1)儀器a的名稱是_____________。裝置A中發生反應的化學方程式為_______。
(2)裝置C中制備POCl3的化學方程式為________________________________。
(3)C裝置控制反應在60~65℃進行,其主要目的是_______________________。
(4)通過佛爾哈德法可以測定三氯氧磷產品中Cl元素含量,實驗步驟如下:
I.取xg產品于錐形瓶中,加入足量NaOH溶液,待完全反應后加稀硝酸至溶液顯酸性;
II.向錐形瓶中加入0.1000 mol·L-1的AgNO3溶液40.00 mL,使Cl-完全沉淀;
III.向其中加入2 mL硝基苯,用力搖動,使沉淀表面被有機物覆蓋;
IV.加入指示劑,用c mol·L-1 NH4SCN溶液滴定過量Ag+至終點,記下所用體積為VmL。
已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12
①滴定選用的指示劑是(填序號)________,滴定終點的現象為_____________。
a.酚酞 b.NH4Fe(SO4)2 c.淀粉 d.甲基橙
②Cl元素的質量分數為(列出算式)________________。
③若取消步驟III,會使步驟IV中增加一個化學反應,該反應的離子方程式為________;該反應使測定結果________(填“偏大”“偏小”或“不變”)。
查看答案和解析>>
科目: 來源: 題型:
【題目】下表是元素周期表的一部分:(不得用a~h字母回答)元素周期表有7個橫行,每一個橫行稱為“周期”,周期序數=電子層數;元素周期表共有18列,每一列稱為 “族”,下表中的7列為主族元素,分別用羅馬數字Ⅰ、Ⅱ、……表明族序數,族序數=最外層電子數。
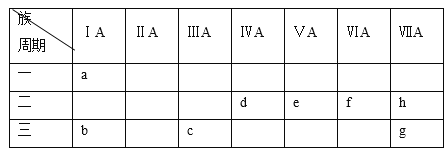
根據a~h各元素的性質,選擇相應的化學符號、化學式或化學方程式填空:
(1)單質氧化性最強的是__________,酸性最強的含氧酸是_____________。
(2)寫出e的堿性氣態氫化物的電子式_____,將它和化合物df 2通入飽和食鹽水發生反應的化學方程式是_____。
(3)最高價氧化物對應的水化物中,堿性最強的是___________。
(4)在b、c、g、h中,常見離子半徑最大的是__________。
查看答案和解析>>
科目: 來源: 題型:
【題目】下列關系圖中,A 是一種正鹽,B 是氣態氫化物,C 是單質,F 是強酸。當 X 無論是強酸還是強堿時都有如下轉化關系(其他反應產物及反應所需條件均已略去),當 X 是強堿時,過量的 B 跟 Cl2 反應除生成 C 外,另一產物是鹽酸鹽。
下列說法中不正確的是( )
![]()
A.當 X 是強酸時,A、B、C、D、E、F中均含同一種元素,F 可能是 H2SO4
B.當 X 是強堿時,A、B、C、D、E、F中均含同一種元素,F 是 HNO3
C.用 O2 代替 Cl2, 也能與 B 反應生成 C 物質
D.當 X 是強酸時,C 在常溫下是一種易溶于酒精的固體
查看答案和解析>>
科目: 來源: 題型:
【題目】Fe2(SO4)3溶液可除去煤中以黃鐵礦(FeS2)形式存在的硫元素,反應如下:
______FeS2 + ______Fe2(SO4)3 +______H2O →______FeSO4 + ______H2SO4
(1)試配平反應的化學方程式,并用單線橋標出電子轉移方向及數目_____;還原劑是_______,還原產物是_________,被還原的元素是__________。
(2)Fe2(SO4)3溶液呈_____性,用離子方程式解釋其原因________。
(3)檢驗上述反應中Fe2(SO4)3是否消耗完的實驗方案:_________________________。
(4)該方法的優點之一是Fe2(SO4)3易再生。向反應后的溶液中通入__________,就能達到使Fe2(SO4)3再生的目的,方便且價廉。
(5)實驗室.配制一定量FeSO4溶液時,需加入少量_____和_______其目的是_______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com