
科目: 來源: 題型:
【題目】A、B、C、D、E、F六種元素均位于周期表的前四周期,且原子序數依次增大。元素A是原子半徑最小的元素;B元素基態原子的核外電子分占四個原子軌道;D元素原子的已成對電子總數是未成對電子總數的3倍;E與D處于同一主族;F位于ds區,且原子的最外層只有2個電子。
(1)F2+離子的電子排布式是_______________。
(2)B、C、D三種元素的電負性由大到小的順序為___________________________
(3)B、C元素的某些氫化物的分子中均含有18個電子, B、C的這些氫化物的沸點相差較大的主要原因是________________________________________________。
(4)D、E可形成ED32-,則該離子的立體構型為____________;A、B、D可形成A2B2D4分子,1mol該物質能與2molNaHCO3反應,則1 mol該分子中含有π鍵的數目為________。
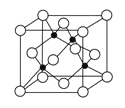
(5)如圖表示F與E形成的化合物晶胞(黑球是F、白球是E),該化合物的化學式為________;該晶胞邊長為540.0 pm,該晶體密度為____________g·cm-3
查看答案和解析>>
科目: 來源: 題型:
【題目】鎢是高熔點金屬,工業上用主要成分為FeWO4和MnWO4的黑鎢鐵礦與純堿共熔冶煉鎢的流程如下,下列說法不正確的是( )
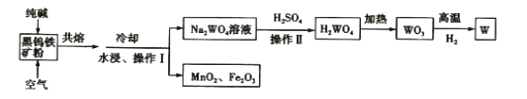
A.將黑鎢鐵礦粉碎的目的是增大反應的速率
B.共熔過程中空氣的作用是氧化Fe(II)和Mn(II)
C.操作II是過濾、洗滌、干燥,H2WO4難溶于水且不穩定
D.在高溫下WO3被氧化成W
查看答案和解析>>
科目: 來源: 題型:
【題目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色)+H2O![]() 2CrO42-(黃色)+2H+。用K2Cr2O7溶液進行下列實驗:( )
2CrO42-(黃色)+2H+。用K2Cr2O7溶液進行下列實驗:( )
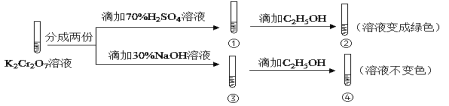
結合實驗,下列說法不正確的是( )
A.若向④中加入70%H2SO4溶液至過量,溶液變為橙色
B.①中溶液橙色加深,③中溶液變黃
C.對比②和④可知K2Cr2O7酸性溶液氧化性強
D.②中Cr2O72-被C2H5OH還原
查看答案和解析>>
科目: 來源: 題型:
【題目】下列圖示與對應的敘述相符的是

A.圖I表示某吸熱反應分別在有、無催化劑的情況下反應過程中的能量變化
B.圖Ⅱ表示常溫下,0.100 mol/L NaOH溶液滴定20.00 mL、0.100 mol/L HC1溶液所得到的滴定曲線。
C.圖Ⅲ表示一定質量的冰醋酸加水稀釋過程中,醋酸溶液電離程度:c<a<b
D.圖Ⅳ表示反應4CO(g)+2NO2(g)![]() N2(g)+4CO2(g),在其他條件不變的情況下改變起始物CO的物質的量,平衡時N2的體積分數變化情況,由圖可知的轉化率c>b>a
N2(g)+4CO2(g),在其他條件不變的情況下改變起始物CO的物質的量,平衡時N2的體積分數變化情況,由圖可知的轉化率c>b>a
查看答案和解析>>
科目: 來源: 題型:
【題目】硫和釩的相關化合物,在藥物化學及催化化學等領域應用廣泛。回答下列問題:
(1)基態釩原子的外圍電子排布式為_________________。釩有+2、+3、+4、+5等多種化合價,其中最穩定的化合價是______________,VO43-的立體構型為__________。
(2)2-巰基煙酸氧釩配合物(圖1)是副作用較小的有效調節血糖的新型藥物。
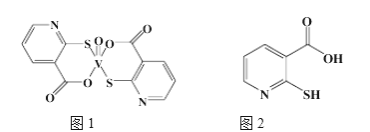
①該藥物中N原子的雜化方式是____________,其所含第二周期元素第一電離能按由大到小順序的排列是__________________。
②2-巰基煙酸(圖2)水溶性優于2-疏基煙酸氧釩配合物的原因是_________________________________。
(3)多原子分子中各原子若在同一平面,且有相互平行的p軌道,則p電子可在多個原子間運動,形成“離域π鍵”,下列物質中存在“離域π鍵”的是________。
A.SO2 B.SO42- C.H2S D.CS2
(4)某六方硫釩化合物晶體的晶胞如圖3所示,圖4為該晶胞的俯視圖,該晶胞的密度為________________ g·cm-3(列出計算式即可)。
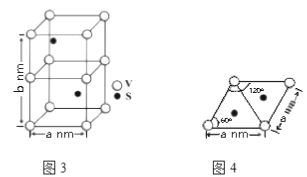
查看答案和解析>>
科目: 來源: 題型:
【題目】常溫下,下列各組離子一定能在指定溶液中大量共存的是( )
A. 使酚酞變紅色的溶液中:Na+、Al3+、SO42-、Cl-
B. ![]() =1×10-13mol·L-1的溶液中:NH4+、Ca2+、Cl-、NO3-
=1×10-13mol·L-1的溶液中:NH4+、Ca2+、Cl-、NO3-
C. 與Al反應能放出H2的溶液中:Fe2+、K+、NO3-、SO42-
D. 水電離的c(H+)=1×10-13mol·L-1的溶液中:K+、Na+、AlO2-、CO32-
查看答案和解析>>
科目: 來源: 題型:
【題目】水的電離平衡曲線如圖所示,下列說法不正確的是

A. 圖中五點Kw間的關系:B>C>A=D=E
B. 若從A點到D點,可采用在水中加入少量酸的方法
C. 若從A點到C點,在溫度不變時向水中加入適量NH4Cl固體
D. 若處在B點時,將pH=2的硫酸與pH=10的KOH溶液等體積混合后,溶液顯中性
查看答案和解析>>
科目: 來源: 題型:
【題目】用NA代表阿伏加德羅常數的值。下列說法正確的是
A.1 L0.5 mol/L Na2SO3溶液中含氧原子數為1.5NA
B.1 mol Na2O2中陰陽離子總數為3NA
C.4.6 g NO2和N2O4混合氣體中含氧原子數為0.3NA
D.11.2 L NH3所含的分子數為0.5NA
查看答案和解析>>
科目: 來源: 題型:
【題目】下列指定反應的離子方程式書寫正確的是
A.硝酸鋁溶液中滴加過量氨水:Al3++4NH3·H2O=AlO2-+4NH4+↑+2H2O
B.用鋁粉和NaOH溶液反應制取大量H2:Al+2OH-=AlO2-+H2↑
C.實驗室制取Cl2:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
D.氯氣溶于水,與水的反應:Cl2+H2O=2H++Cl-+ClO-
查看答案和解析>>
科目: 來源: 題型:
【題目】下列實驗、現象及相關結論均正確的是
A | B | C | D | |
實驗 |
|
|
|
|
現象 | 品紅褪色 | 最后試管有淺黃色沉淀 | 最后一滴溶液使酚酞由無色變為粉紅色,且30s不復原 | 出現白色沉淀 |
結論 | SO2 有強強氧化性 | 有機物中含有溴原子 | 滴定達終點 | Ksp(AgCl)>Ksp(AgI) |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com