
科目: 來源: 題型:
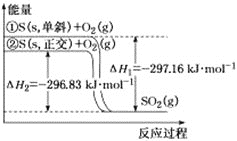
【題目】單斜硫和正交硫轉化為二氧化硫的能量變化如圖所示,下列說法正確的是![]()
![]()
A.![]() ,單斜
,單斜![]() ,正交
,正交![]()
B.等質量的單斜硫和正交硫分別完全燃燒,前者放出的熱量更多
C.相同物質的量的正交硫比單斜硫所含有的能量高,正交硫比單斜硫穩定
D.![]() 表示斷裂
表示斷裂![]() 中的共價鍵所吸收的能量比形成
中的共價鍵所吸收的能量比形成![]() 中的共價鍵所放出的能量少
中的共價鍵所放出的能量少 ![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】a-Fe(III)晶面鐵原子簇是合成氨工業的一種新型高效催化劑,N2和H2在其表面首先變為活化分子,反應機理為①H2 (g)=2H(g) △H1,②N2(g)+2H(g)2(NH)(g) △H2, ③(NH)(g)+H(g)![]() (NH2)(g) △H3, ④(NH2)(g)+H(g)
(NH2)(g) △H3, ④(NH2)(g)+H(g) ![]() NH3 (g) △H4,總反應為N2 (g)+3H2(g)
NH3 (g) △H4,總反應為N2 (g)+3H2(g)![]() 2NH3 (g) △H。下列說法正確的是
2NH3 (g) △H。下列說法正確的是
A. 催化劑能夠有效降低反應的活化能和改變反應的焓變
B. 增大壓強和使用高效催化劑均有利于提高總反應的平衡轉化率
C. 反應①和總反應均為放熱反應
D. △H=3△H1+△H2+2△H3+2△H4
查看答案和解析>>
科目: 來源: 題型:
【題目】MgCO3和CaCO3的能量關系如圖所示(M=Ca、Mg):
M2+(g)+CO32-(g) ![]() M2+(g)+O2(g)+CO2(g)
M2+(g)+O2(g)+CO2(g)
![]()
![]()
![]()
已知:離子電荷相同時,半徑越小,離子鍵越強。下列說法不正確的是
A. ΔH1(MgCO3)>ΔH1(CaCO3)>0
B. ΔH2(MgCO3)=ΔH2(CaCO3)>0
C. ΔH1(CaCO3)-ΔH1(MgCO3)=ΔH3(CaO)-ΔH3(MgO)
D. 對于MgCO3和CaCO3,ΔH1+ΔH2>ΔH3
查看答案和解析>>
科目: 來源: 題型:
【題目】向某密閉容器中加入0.15 mol·L-1 A、0.05 mol·L-1 C和一定量的B三種氣體。一定條件下發生反應,各物質濃度隨時間變化如圖中甲圖所示[t0~t1時c(B)未畫出,t1時c(B)增大到0.05 mol·L-1]。乙圖為t2時刻后改變反應條件,平衡體系中正、逆反應速率隨時間變化的情況。
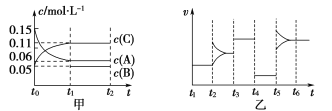
(1)若t4時改變的條件為減小壓強,則B的起始物質的量濃度為___mol·L-1。
(2)若t5時改變的條件是升溫,此時v(正)>v(逆),若A的物質的量減少0.03 mol時,容器與外界的熱交換總量為a kJ,寫出反應的熱化學方程式:___________________________________。
(3)t3時改變的某一反應條件可能是________(填字母)。
a.使用催化劑 b.增大壓強 c.增大反應物濃度
(4)在恒溫恒壓下通入惰性氣體,v(正)________v(逆)(填“>”“=”或“<”)。
查看答案和解析>>
科目: 來源: 題型:
【題目】在25℃、101kPa時,C(s)、H2(g)、CH3COOH(l)的燃燒熱分別為393.5kJ/mol、285.8kJ/mol、870.3kJ/mol,則2C(s)+2H2(g)+O2(g)= CH3COOH(l)的焓變為( )
A.-488.3kJ/molB.+488.3kJ/molC.+191kJ/molD.-191kJ/mol
查看答案和解析>>
科目: 來源: 題型:
【題目】下列情況中說明2HI(g)H2(g)+I2(g)已達平衡狀態的是__________
①單位時間內生成nmolH2的同時,生成nmolHI;
②1個H﹣H鍵斷裂的同時有2個H﹣I鍵斷裂;
③混合氣中百分組成為HI%=I2%;
④反應速率v(H2)=v(I2)=![]() v(HI)時;
v(HI)時;
⑤混合氣體中c(HI):c(H2):c(I2)=2:1:1時;
⑥溫度和體積一定時,某一生成物濃度不再變化;
⑦溫度和體積一定時,容器內壓強不再變化;
⑧條件一定,混合氣體的平均分子質量不再變化;
⑨溫度和體積一定時,混合氣體的顏色不再變化;
⑩溫度和壓強一定時,混合氣體的密度不再變化;
上述⑥~⑩的說法中能說明2NO2N2O4達到平衡狀態的是___________。
查看答案和解析>>
科目: 來源: 題型:
【題目】隨原子序數的遞增,八種短周期元素(用字母X表示)原子半徑的相對大小、最高正價或最低負價的變化如下圖所示。
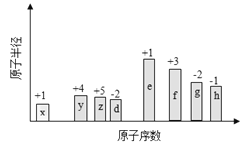
根據判斷出的元素回答問題:
(1)f在元素周期表的位置是__________。
(2)比較d、e常見離子的半徑的小(用化學式表示,下同)_______>__________;比較g、h的最高價氧化物對應的水化物的酸性強弱是:_______>__________。
(3)任選上述元素組成一種四原子共價化合物,寫出其電子式__________。
(4)已知1mole的單質在足量d2中燃燒,恢復至室溫,放出255.5kJ熱量,寫出該反應的熱化學方程式:___________________。
(5)上述元素可組成鹽R:zx4f(gd4)2,向盛有10mL1mol·L-1R溶液的燒杯中滴加1mol·L-1NaOH溶液,沉淀物質的量隨NaOH溶液體積變化示意圖如下:
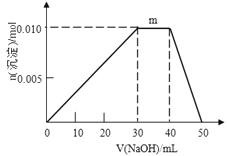
①R離子濃度由大到小的順序是:__________。
②寫出m點反應的離子方程式_________________。
③若R溶液改加20mL1.2 mol·L-1Ba(OH)2溶液,充分反應后,溶液中產生沉淀的物質的量為______mol。
查看答案和解析>>
科目: 來源: 題型:
【題目】新冠疫情下,西方各國防護服原材料價格飛漲,以PE復合膜透氣材料為代表的中國制造因物美價廉、供應充足贏得了世界贊譽。PE是由乙烯為原料合成的高分子材料的簡稱,乙烯的相關反應關系如下圖所示:
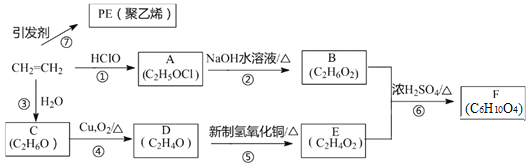
回答下列問題:
(1)C的結構簡式為___________,⑦的反應類型為____________。
(2)D、E分子中含有的官能團分別為__________,_____________。
(3)寫出能發生水解反應的E的同分異構體結構簡式________________。
(4)寫出下列反應的化學方程式:
①CH2=CH2→A__________________。
②A→B_________________。
(5)F的結構簡式為_________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】實驗室欲探究CO還原CuO,設計如圖所示裝置(夾持裝置略去)。下列說法正確的是
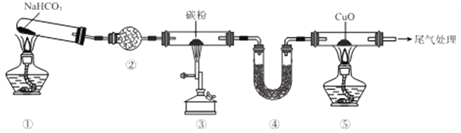
A. ②、④中均可盛裝堿石灰
B. 加熱的順序為③、①、⑤
C. ①、③、⑤中均發生氧化還原反應
D. 可將尾氣用導管通入到⑤的酒精燈處灼燒
查看答案和解析>>
科目: 來源: 題型:
【題目】甲烷是一種重要的基礎化工原料,不僅可制備多種重要有機產品,還可用于環境保護。請回答下列問題:
(1)用甲烷催化還原氮的氧化物可消除氮氧化物的污染。已知:

反應過程(2)是__反應(填“放熱”或“吸熱”),甲烷還原NO2生成H2O(g)、N2和CO2時的熱化學方程式是__。
(2)工廠利用甲烷與氯氣的反應原理制取氯甲烷,為妥善處理氯甲烷生產企業的副產物CCl4,以減少其對臭氧層的破壞。化學家研究在催化條件下,通過下列反應:CCl4(g)+H2(g)![]() CHCl3(g)+HCl(g),使CCl4轉化為重要的化工原料氯仿(CHCl3)(不考慮副反應)。在固定容積為2L的密閉容器中,該反應達到平衡后,測得如下數據:
CHCl3(g)+HCl(g),使CCl4轉化為重要的化工原料氯仿(CHCl3)(不考慮副反應)。在固定容積為2L的密閉容器中,該反應達到平衡后,測得如下數據:
實驗 序號 | 溫度℃ | 初始n(CCl4)( mol) | 初始n(H2)( mol) | 平衡時n(CHCl3)( mol) |
1 | 110 | 0.8 | 1.2 | |
2 | 110 | 2 | 2 | 1 |
3 | 100 | 1 | 1 | 0.6 |
①此反應在110℃時平衡常數為___。
②實驗l中,CCl4的轉化率為__。
③判斷該反應的正反應是__(填“放熱”或“吸熱”),理由是__。
④為提高實驗3中CCl4的轉化率,可采取的措施是__。
a.使用高效催化劑
b.向容器中再投入1molCCl4和1molH2
c.溫度升高到200℃
d.向容器中再投入1molHCl
e.向容器中再投入1molH2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com