
科目: 來源: 題型:
【題目】Ⅰ、某溫度時,在一個 10L 的恒容容器中,X、Y、Z 均為氣體,三種物質的物 質的量隨時間的變化曲線如圖所示.根據圖中數據填空:
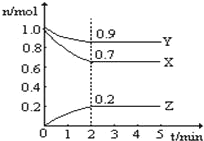
(1)該反應的化學方程式為______;
(2)反應開始至 2min,以氣體 Z 表示的平均反應速率為______;
(3)平衡時容器內混合氣體密度比起始時______(填“變大”,“變小”或“不變” 下同),混合氣體的平均相對分子質量比起始時__________;
(4)將 a mol X 與 b mol Y 的混合氣體發生上述反應,反應到某時刻各物質的量恰好滿足: n(X)=n(Y)=2n(Z),則原混合氣體中 a:b=______。
Ⅱ、在恒溫恒容的密閉容器中,當下列物理量不再發生變化時:①混合氣體的壓強,②混合 氣體的密度,③混合氣體的總物質的量,④混合氣體的平均相對分子質量,⑤混合氣體的顏 色,⑥各反應物或生成物的反應速率之比等于化學計量數之比
(1)一定能證明 2SO2(g)+O2(g)![]() 2SO3(g)達到平衡狀態的是_____(填序號,下同)。
2SO3(g)達到平衡狀態的是_____(填序號,下同)。
(2)一定能證明 I2(g)+H2(g)![]() 2HI(g)達到平衡狀態的是 ______。
2HI(g)達到平衡狀態的是 ______。
(3)一定能證明 A(s)+2B(g)![]() C(g)+D(g)達到平衡狀態的是______。(B C D 均無色)
C(g)+D(g)達到平衡狀態的是______。(B C D 均無色)
III 、某化學反應 2A![]() B+D 在四種條件下進行,B、D 起始濃度為 0,反應物 A 的濃度(mol/L)隨反應時間(min)的變化情況如表:
B+D 在四種條件下進行,B、D 起始濃度為 0,反應物 A 的濃度(mol/L)隨反應時間(min)的變化情況如表:
實驗序號 | 時間 濃度 溫度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
2 | 800 | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
3 | 800 | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
4 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
比較實驗 4 和實驗 1 可推測該正反應是_____反應(填“吸熱”或“放熱”)。 理由_________
查看答案和解析>>
科目: 來源: 題型:
【題目】某興趣小組進行鐵礦石中含鐵量的測定,實驗過程如圖:
![]()
下列說法正確的是( )
A.加熱煮沸的主要目的是除去溶液中溶解的氧氣
B.稀釋過程中用到的玻璃儀器主要有燒杯、玻璃棒、膠頭滴管
C.滴定過程中可用淀粉溶液作指示劑
D.鐵礦石中鐵的質量分數為70%
查看答案和解析>>
科目: 來源: 題型:
【題目】I.草酸與高錳酸鉀在酸性條件下能夠發生如反應:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,用 4mL 0.001mol/L KMnO4 溶液與2mL 0.01mol/L H2C2O4 溶液,研究不同條件對化學反應速率的影響.改變的條件如下:
組別 | 10%硫酸體積/mL | 溫度/℃ | 其他物質 |
Ⅰ | 2mL | 20 | |
Ⅱ | 2mL | 20 | 10 滴飽和 MnSO4 溶液 |
Ⅲ | 2mL | 30 | |
Ⅳ | 1mL | 20 | 1mL 蒸餾水 |
(1)該反應中氧化劑和還原劑的物質的量之比為_____
(2)如果研究催化劑對化學反應速率的影響,使用實驗_________和_____(用Ⅰ~Ⅳ表示,下同); 如果研究溫度對化學反應速率的影響,使用實驗_____和_________.
(3)對比實驗Ⅰ和Ⅳ,可以研究_____對化學反應速率的影響,實驗Ⅳ中加入 1mL蒸餾水的目的是_______
II、利用如圖裝置采用適當試劑可完成某探究實驗,并得出相應實驗結論.請根據相關信息回答:

(1)為了證明元素的非金屬性強弱是 S>C>Si.你認為各物質應該是: 甲為______;乙為______;丙為______.(已知乙中有氣泡產生,丙中 有白色沉淀)
(2)如果甲為水,乙為 Na2O2 粉末,丙為 H2S 的飽和水溶液.實驗中觀察到丙中生成淡黃色沉淀。說明元素O、S得電子能力強弱為 ______。
(3)將該裝置連接好后,在加入藥品開始實驗前還需進行氣密性檢查,請你簡述該操作_____。
查看答案和解析>>
科目: 來源: 題型:
【題目】下列變化不可能通過一步反應直接完成的是
A. Al(OH)3 → Al2O3 B. Al2O3 → Al(OH)3
C. Al → AlO2- D. Al3+ → Al(OH)3
查看答案和解析>>
科目: 來源: 題型:
【題目】電化學氣敏傳感器可用于監測環境中NH3的含量,其工作原理示意圖如下。下列說法不正確的是( )

A. O2在電極b上發生還原反應
B. 溶液中OH-向電極a移動
C. 反應消耗的NH3與O2的物質的量之比為4∶5
D. 負極的電極反應式為2NH3-6e-+6OH-===N2+6H2O
查看答案和解析>>
科目: 來源: 題型:
【題目】下列說法正確的是( )
A.測定HCl和NaOH中和反應的反應熱時,單次實驗均應測量3個溫度,即鹽酸起始溫度、NaOH溶液起始溫度和反應終止溫度
B.2C(s)+O2(g)=2CO(g) 若△H=-221.0kJ/mol,則碳的燃燒熱為110.5kJ/mol
C.需要加熱的反應一定是吸熱反應,常溫下能發生的反應一定是放熱反應
D.已知Ⅰ:反應H2(g)+Cl2(g)=2HCl(g) △H=-akJ/mol;Ⅱ:![]() ,
,![]() 且a、b、c均大于零,則斷開1molH-Cl鍵所需的能量為2(a-b-c)kJ/mol
且a、b、c均大于零,則斷開1molH-Cl鍵所需的能量為2(a-b-c)kJ/mol
查看答案和解析>>
科目: 來源: 題型:
【題目】mA(g)+nB(g)![]() pC(g)的速率和平衡的影響圖像如下,下列判斷正確的是
pC(g)的速率和平衡的影響圖像如下,下列判斷正確的是
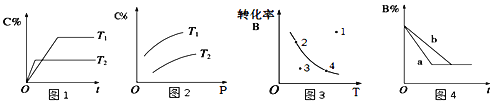
A.由圖1可知,T1<T2,該反應正反應為吸熱反應
B.由圖2可知,該反應m+n﹤p
C.圖3中,表示反應速率v正>v逆的是點3
D.圖4中,若m+n=p,則a曲線一定使用了催化劑
查看答案和解析>>
科目: 來源: 題型:
【題目】(1)金剛烷的結構如圖1所示,它可看作是由四個等同的六元環組成的空間構型。
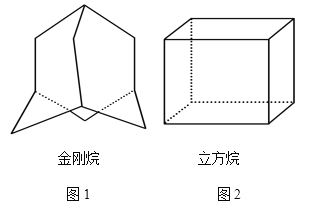
①金剛烷的分子式為________;
②根據中學學過的同分異構體判斷規則,判斷由溴原子取代分子中的氫原子形成的一溴代物有_____種。
(2)“立方烷”是一種新合成的烴,其分子為正方體結構,其碳架結構如圖2所示。
①立方烷的分子式為______________________;
②該立方烷的二氯代物具有同分異構體的數目是_____________;
③將a g立方烷溶于b mL苯中,然后通入c L乙炔(標準狀況下),所得混合物中碳的百分含量為_______________。
查看答案和解析>>
科目: 來源: 題型:
【題目】甲、乙、丙、丁、戊是中學化學常見的無機物,其中甲、乙均為單質,它們的轉化關系如圖所示(某些條件和部分產物已略去)。下列說法不正確的是
( )。
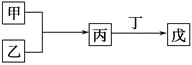
A. 若組成甲、乙的元素位于同一周期,則戊可能是一種弱酸
B. 若組成甲、乙的元素位于同一主族,則戊可能是一種弱酸
C. 若甲為短周期中原子半徑最大的主族元素形成的單質,且戊為堿,則丙只能為Na2O2
D. 若丙、丁混合生成白煙,且丙為18電子分子,丁為10電子分子,則乙的水溶液可能具有漂白作用
查看答案和解析>>
科目: 來源: 題型:
【題目】斷裂1 mol化學鍵所需的能量如下:
化學鍵 | N—N | O=O | N≡N | N—H |
鍵能(kJ) | 154 | 500 | 942 | a |
火箭燃料肼(H2N—NH2)的有關化學反應的能量變化如圖所示,則下列說法錯誤的是

A.N2比O2穩定
B.N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-534 kJ·mol-1
C.表中的a=194
D.圖中的ΔH3=+2218 kJ·mol-1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com