
科目: 來源: 題型:
【題目】將 4 molA 和 2 molB 在 2 L 的容器中混合并在一定條件下發生如下反應 2A(g)+B(s)=2C(g),若經2s后測得 C 的濃度為 0.6 mol/L,現有下列幾種說法:
①用物質 A 表示的反應的平均速率為 0.3 mol/(L·s)
②用物質 B 表示的反應的平均速率為 0.6 mol/(L·s)
③增大 B 的濃度可加快反應速率
④2 s 時物質 A 的濃度為 1.4 mol/L
其中正確的是
A.①③B.①④C.②③D.③④
查看答案和解析>>
科目: 來源: 題型:
【題目】氯化銨具有廣泛用途,可用于選礦、醫藥等。
(1)實驗室用氯化銨與熟石灰反應制取氨氣的化學方程式為____,收集氨氣時,可選用下圖中的裝置____(填字母)。
A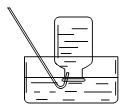 B
B C
C![]()
(2)工業上為提高氯化銨產品的經濟利用價值,常利用氫氧化鎂和氯化銨共熱制得氨氣、堿式氯化鎂[Mg(OH)Cl](520℃發生分解)。實驗室模擬該工藝的裝置圖如下:

①冷凝管進水口是_____(填“a”或“b”)。
②實驗中持續通入氮氣的目的是_____。
③共熱時,溫度不宜過高的原因是_____。
④共熱時,若氯化銨用量過大會導致Mg(OH)Cl中混有較多的雜質為_____(寫化學式)。
(3)已知氧化鈣與氯化銨溶液反應制備氯化鈣的適宜溫度為80℃。補充完整由氧化鈣(含少量SiO2)、氯化銨溶液制備醫用CaCl2·2H2O晶體的實驗步驟:將氯化銨溶液、氧化鈣粉末按照一定配比加入反應器中,_____,得到CaCl2溶液,_____、趁熱過濾、洗滌、干燥。(實驗中須使用的試劑:稀硫酸)
查看答案和解析>>
科目: 來源: 題型:
【題目】下列物質中,既能因發生化學反應而使溴水褪色,又能使高錳酸鉀酸性溶液褪色的是( )
①CH3CH2CH2CH3 ②CH3CH2CH===CH2

A.①②③④ B.②③④
C.②④ D.只有②
查看答案和解析>>
科目: 來源: 題型:
【題目】研究和深度開發CO、CO2的應用對構建生態文明社會具有重要的意義。
(1)CO可用于煉鐵,已知:Fe2O3(s)+ 3C(s)=2Fe(s)+ 3CO(g) ΔH 1=+489.0 kJ·mol-1
C(s) +CO2(g)=2CO(g) ΔH 2 =+172.5 kJ·mol-1。則CO還原Fe2O3(s)的熱化學方程式為_________________________________________________。
(2)分離高爐煤氣得到的CO與空氣可設計成燃料電池(以KOH溶液為電解液)。寫出該電池的負極反應式:__________________________________________________。
(3)①CO2和H2充入一定體積的密閉容器中,在兩種溫度下發生反應:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),測得CH3OH的物質的量隨時間的變化如圖。①曲線I、Ⅱ對應的平衡常數大小關系為KⅠ___________________KⅡ(填“>”或“=”或“<”)。
CH3OH(g)+H2O(g),測得CH3OH的物質的量隨時間的變化如圖。①曲線I、Ⅱ對應的平衡常數大小關系為KⅠ___________________KⅡ(填“>”或“=”或“<”)。
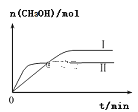
②一定溫度下,在容積相同且固定的兩個密閉容器中,按如下方式加入反應物,一段時間后達到平衡。
容 器 | 甲 | 乙 |
反應物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
若甲中平衡后氣體的壓強為開始的0.8倍,要使平衡后乙與甲中相同組分的體積分數相等,且起始時維持化學反應向逆反應方向進行,則c的取值范圍為______________________。
③一定溫度下,此反應在恒壓容器中進行,能判斷該反應達到化學平衡狀態的依據是______________。
a.容器中壓強不變 b.H2的體積分數不變 c.c(H2)=3c(CH3OH)
d.容器中密度不變 e.2個C=O斷裂的同時有3個H-H斷裂
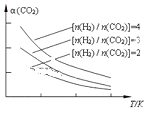
(4)將燃煤廢氣中的CO2轉化為二甲醚的反應原理為:2CO2(g) + 6H2(g)![]() CH3OCH3(g) + 3H2O(g)。已知一定條件下,該反應中CO2的平衡轉化率隨溫度、投料比[n(H2) / n(CO2)]的變化曲線如圖,若溫度不變,提高投料比n(H2)/n(CO2),則K將__________;該反應△H_________0(填“>”、“<”或“=”)。
CH3OCH3(g) + 3H2O(g)。已知一定條件下,該反應中CO2的平衡轉化率隨溫度、投料比[n(H2) / n(CO2)]的變化曲線如圖,若溫度不變,提高投料比n(H2)/n(CO2),則K將__________;該反應△H_________0(填“>”、“<”或“=”)。
查看答案和解析>>
科目: 來源: 題型:
【題目】下表是元素周期表的一部分,表中所列的字母分別代表一種元素。
A | |||||||||||||||||
B | C | D | E | F | T | ||||||||||||
G | H | I | J | K | L | ||||||||||||
M | N | O | |||||||||||||||
試回答下列問題(注意:每問中的字母代號為上表中的字母代號,并非為元素符號)
(1)N的單質和水蒸氣反應能生成固體X,則I的單質與X反應的化學方程式_______。
(2)D的氣態氫化物的VSEPR模型的名稱為_______。
(3)由A、C、D形成的ACD分子中,σ鍵和π鍵個數比= _______________。
(4)要證明太陽上是否含有R 元素,可采用的方法是__________________________。
(5)元素M的化合物(ME2L2)在有機合成中可作氧化劑或氯化劑,能與許多有機物反應。回答問題:
①ME2L2常溫下為深紅色液體,能與CCl4、CS2等互溶,據此可判斷ME2L2是_________(填“極性”或“非極性”)分子。
②將N和O的單質用導線連接后插入D的最高價氧化物對應的水化物濃溶液中,可制成原電池,則組成負極材料的元素的外圍電子軌道表示式為______________________。
(6)往O2+溶液中加入氨水,形成藍色沉淀,繼續加入氨水,難溶物溶解變成藍色透明溶液,寫出沉淀溶解的離子方程式_____。
(7)若F 、K兩種元素形成的化合物中中心原子的價電子全部參與成鍵,則該化合物的空間構型的名稱為___。
(8)如圖四條折線分別表示ⅣA族、ⅤA族、ⅥA族、ⅦA族元素氣態氫化物沸點變化,則E的氫化物所在的折線是__(填m、n、x或y)。

(9)1183 K以下純N晶體的基本結構單元如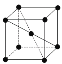 所示,1183 K以上轉變為
所示,1183 K以上轉變為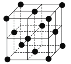 所示結構的基本結構單元。在1183 K以下的晶體中,空間利用率為____;在1183 K以上的晶體中,與N原子等距離且最近的N原子數為____,晶體堆積方式的名稱為_____。
所示結構的基本結構單元。在1183 K以下的晶體中,空間利用率為____;在1183 K以上的晶體中,與N原子等距離且最近的N原子數為____,晶體堆積方式的名稱為_____。
查看答案和解析>>
科目: 來源: 題型:
【題目】25℃時,向0.1molL-1NaA溶液中逐滴滴加鹽酸,測得混合溶液的pH與p![]() 變化關系如圖所示[p
變化關系如圖所示[p![]() =-lg
=-lg![]() ]。下列說法正確的是( )
]。下列說法正確的是( )
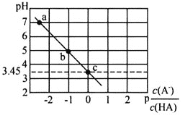
A.a點溶液中c(Na+)=c(A-)
B.電離常數K(HA)的數量級為10-4
C.滴加過程中![]() 不斷減小
不斷減小
D.b點溶液中c(HA)>c(Na+)>c(A-)>c(OH-)
查看答案和解析>>
科目: 來源: 題型:
【題目】自然界中氯化鈉是由1123Na 與1735Cl 和1735Cl所構成的。已知氯元素的相對原子質量是35.5,則 11.7g 氯化鈉中,含1735Cl 的質量為
A.1.75gB.1.85gC.5.25gD.5.55g
查看答案和解析>>
科目: 來源: 題型:
【題目】在元素周期表中,除稀有氣體外幾乎所有元素都能與氫形成氫化物。
(1)氨氣屬于共價型氫化物,工業常用氨氣和醋酸二氨合銅[Cu(NH3)2]Ac的混合液來吸收CO(醋酸根離子簡寫為Ac-)。反應方程式為:[Cu(NH3)2]Ac+CO+NH3=[Cu(NH3)3CO]Ac
①氨水溶液中各元素原子的第一電離能從大到小排列順序為___________。
②醋酸分子(CH3COOH)中的兩個碳原子的雜化方式分別是_________________。
③生成物[Cu(NH3)3CO]Ac中所含化學鍵類型有_________(填序號)。
A.離子鍵b.金屬鍵c.共價鍵d.配位鍵
(2)某離子化合物XY2,晶胞結構如圖所示,其中6個Y原子用數字1~6標注。
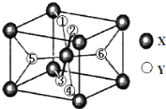
已知1、2、3、4號Y原子在晶胞上、下面上,則5、6號Y原子均在晶胞_________(填“側面”或“內部”)。
②根據以上信息可以推知,XY2晶體的熔沸點______(填“>”、“=”或“<”)固態氨的熔沸點。
③若該晶胞的邊長為anm,密度為ρg/cm3,XY2的摩爾質量為Mg/mol,則阿伏加德羅常數為____。
查看答案和解析>>
科目: 來源: 題型:
【題目】已知A、B、C、D、E、F都是周期表中前四周期的元素,它們的核電荷數A<B<C<D<E<F。其中A原子核外有三個未成對電子;化合物B2E為離子晶體,E原子核外的M層中只有兩對成對電子;C元素是地殼中含量最高的金屬元素;D單質的晶體類型在同周期的單質中沒有相同的;F原子最外層電子數與B的相同,其余各層均充滿電子。請根據以上信息,回答下列問題(答題時,A、B、C、D、E、F用所對應的元素符號表示):
(1)A、B、C、D四種元素原子半徑由小到大的順序為_______________________。
(2)A、F形成某種化合物的晶胞結構如下圖(其中A顯-3價),則其化學式為___(每個球均表示1個原子)。
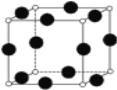
(3)A、C形成的化合物具有高沸點和高硬度,是一種新型無機非金屬材料,則其化學式為________,其晶體類型為_______,晶體中1個A原子周圍最近距離且等距離的C原子數為_______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com