
科目: 來源: 題型:
【題目】化合物AX3和單質X2在一定條件下反應可生成化合物AX5。回答下列問題:反應AX3(g)+X2(g)![]() AX5(g)在容積為10 L的密閉容器中進行。起始時AX3和X2均為0.2 mol。反應在不同條件下進行,反應體系總壓強隨時間的變化如圖所示。
AX5(g)在容積為10 L的密閉容器中進行。起始時AX3和X2均為0.2 mol。反應在不同條件下進行,反應體系總壓強隨時間的變化如圖所示。
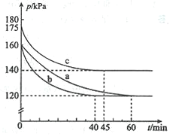
(1)列式計算實驗a從反應開始至達到平衡時的反應速率 v(AX5)=________________。
(2)圖中3組實驗從反應開始至達到平衡時的反應速率v(AX5)由大到小的次序為_______________(填實驗序號);與實驗a相比,其他兩組改變的實驗條件是:b_________________、c____________________________________。
(3)用p0表示開始時總壓強,p表示平衡時總壓強,α表示AX3的平衡轉化率,則α的表達式為_________________;實驗a和c的平衡轉化率:αa為___________、αc為_______________。
查看答案和解析>>
科目: 來源: 題型:
【題目】堿式碳酸鋁鎂[MgaAlb(OH)c(CO3)d·x H2O]常用作塑料阻燃劑。
(1)堿式碳酸鋁鎂具有阻燃作用,是由于其受熱分解需吸收大量熱量和_________。
(2)MgaAlb(OH)c(CO3)d·x H2O中a、b、c、d的代數(shù)關系式為_________________。
(3)為確定堿式碳酸鋁鎂的組成,進行如下實驗:
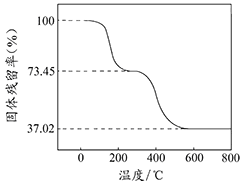
①準確稱取3.390g樣品與足量稀鹽酸充分反應,生成CO20.560L(已換算成標準狀況下)。②另取一定量樣品在空氣中加熱,樣品的固體殘留率(固體樣品的剩余質量/固體樣品的起始質量×100%)隨溫度的變化如右圖所示(樣品在2700C時已完全失去結晶水,6000C以上殘留固體為金屬氧化物的混合物)。
根據(jù)以上實驗數(shù)據(jù)計算堿式碳酸鋁鎂樣品中的n(OH-): n(CO32-)(寫出計算過程)________。
查看答案和解析>>
科目: 來源: 題型:
【題目】某種礦石中鐵元素以氧化物FemOn形式存在,現(xiàn)進行如下實驗:將少量鐵礦石樣品粉碎,稱取25.0 g樣品于燒杯中,加入稀硫酸充分溶解,并不斷加熱、攪拌,濾去不溶物。向所得濾液中加入10.0 g銅粉充分反應后過濾、洗滌、干燥得剩余固體3.6 g。剩下濾液用濃度為2 mol·L-1的酸性KMnO4滴定,至終點時消耗KMnO4溶液體積為25.0 mL。(提示:2Fe3++Cu=2Fe2++Cu2+,8H++MnO4-+5Fe2+=Mn2++5Fe3++4H2O。)
(1)計算該鐵礦石中鐵元素的質量分數(shù)。_____
(2)計算氧化物FemOn的化學式(m、n為正整數(shù))。_______
查看答案和解析>>
科目: 來源: 題型:
【題目】H2S是一種劇毒氣體,如圖為質子膜H2S燃料電池的示意圖,可對H2S廢氣資源化利用。下列敘述不正確的是( )
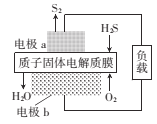
A.電池工作時,化學能轉化為電能和熱能
B.電極b上發(fā)生的電極反應式為O2+ 4e+4H+=2H2O
C.a是負極,電池工作時,電子的流動方向是:電極a→負載→電極b→質子膜→電極a
D.當電路中通過4mol電子時,有4molH+經(jīng)質子膜進入正極區(qū)
查看答案和解析>>
科目: 來源: 題型:
【題目】為提升電池循環(huán)效率和穩(wěn)定性,科學家近期利用三維多孔海綿狀Zn(3DZn)可以高效沉積ZnO的特點,設計了采用強堿性電解質的3DZn—NiOOH二次電池,結構如圖所示。電池反應為Zn+2NiOOH+H2O ![]() ZnO+2Ni(OH)2。下列說法錯誤的是
ZnO+2Ni(OH)2。下列說法錯誤的是

A.放電過程中OH通過隔膜從負極區(qū)移向正極區(qū)
B.充電時陽極反應為Ni(OH)2+OHe=NiOOH+H2O
C.放電時負極反應為Zn+2OH2e=ZnO+H2O
D.三維多孔海綿狀Zn具有較高的表面積,所沉積的ZnO分散度高
查看答案和解析>>
科目: 來源: 題型:
【題目】下列關于有機化合物的敘述正確的是( )
A.糖類、油脂、蛋白質都是有機高分子化合物
B.有機物![]() 可以發(fā)生消去反應和催化氧化
可以發(fā)生消去反應和催化氧化
C.乙醇可以和金屬鈉反應很緩慢地放出氫氣,說明乙醇的酸性很弱
D.福爾馬林可用作食品防腐劑
查看答案和解析>>
科目: 來源: 題型:
【題目】CCl3CHO可通過“CH3CH2OH+4Cl2→CCl3CHO+5HCl”進行制備。
⑴實驗室常用KMnO4、MnO2或NaClO與濃鹽酸反應制取Cl2。質量分數(shù)為36.5%,密度為1.18 g·cm-3鹽酸,其物質的量濃度為______mol·L1。等物質的量的KMnO4、MnO2或NaClO與足量濃鹽酸反應,理論上生成的Cl2的質量之比為______。
⑵可用如下方法測定所制CCl3CHO粗品的純度(雜質不參與反應):稱取該實驗制備的產品5.00 g,配成100.00 mL溶液,取其中10.00 mL,加入一定量的NaOH后,加入30.00 mL 0.100 mol·L1的碘標準液,用0.100 mol·L1的Na2S2O3溶液滴定,重復上述3次操作,消耗Na2S2O3溶液平均體積為20.00 mL。實驗中所發(fā)生反應如下:CCl3CHO+NaOH=CHCl3+HCOONa,HCOONa+I2=HI+NaI+CO2↑, I2+2Na2S2O3=2NaI+Na2S4O6,計算粗品中所含CCl3CHO的質量分數(shù)(寫出計算過程)。_____________
查看答案和解析>>
科目: 來源: 題型:
【題目】回答下列問題:
(1)Mn、Fe均為第四周期過渡金屬元素,兩元素的部分電離能數(shù)據(jù)列于下表:
元素 | Mn | Fe | |
電離能/( | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
錳元素位于第四周期第ⅦB族。請寫出基態(tài)Mn2+的價電子軌道排布圖:_________________,比較兩元素的I2、I3可知,氣態(tài)Mn2+再失去1個電子比氣態(tài)Fe2+再失去1個電子難,對此你的解釋是________________________________________________________
(2)下表是第三周期部分元素的電離能[單位:[![]() (電子伏特)]數(shù)據(jù)。
(電子伏特)]數(shù)據(jù)。
元素 |
|
|
|
甲 | 5.7 | 47.4 | 71.8 |
乙 | 7.7 | 15.1 | 80.3 |
丙 | 13.0 | 23.9 | 40.0 |
丁 | 15.7 | 27.6 | 40.7 |
下列說法正確的是___________(填序號)。
A.甲的金屬性比乙強 B.乙有![]() 價
價
C.丙不可能為非金屬元素 D.丁一定為金屬元素
查看答案和解析>>
科目: 來源: 題型:
【題目】短周期主族元素X、Y、Z、W原子序數(shù)依次增大,Y的原子半徑是短周期主族元素原子中最大的,X與Z屬于同一主族,Z的最外層電子數(shù)為最內層電子數(shù)的3倍。下列說法正確的是
A.原子半徑: r(Y)>r(W)>r(Z)>r(X)
B.由X、Y組成的化合物中均不含共價鍵
C.W的氧化物對應水化物的酸性比Z的強
D.X的簡單氣態(tài)氫化物的熱穩(wěn)定性比Z的強
查看答案和解析>>
科目: 來源: 題型:
【題目】下列指定反應的離子方程式正確的是
A.Fe3O4溶于足量稀HNO3:Fe3O4+8H+=Fe2++2Fe3++4H2O
B.向KClO3溶液中滴加稀鹽酸:ClO3-+Cl-+6H+=Cl2↑+3H2O
C.向Al2(SO4)3溶液中滴加過量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+
D.NaHSO4溶液與Ba(OH)2溶液反應至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com