
科目: 來源: 題型:
【題目】高錳酸鉀是錳的重要化合物和常用的氧化劑。以下是工業上用軟錳礦制備高錳酸鉀的一種工藝流程:
![]() 時溶解度
時溶解度![]() 克
克![]() 克水
克水![]() ,
,![]() :111,
:111,![]() :
:![]()
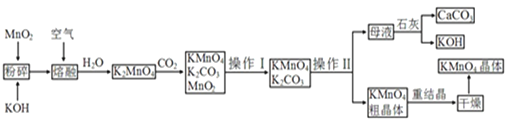
![]() 稀溶液是一種常用的消毒劑,其消毒原理與下列____物質相似。
稀溶液是一種常用的消毒劑,其消毒原理與下列____物質相似。
A ![]() 酒精
酒精 ![]() 雙氧水
雙氧水 ![]() 苯酚
苯酚 ![]() “84”消毒液
“84”消毒液![]() 溶液
溶液![]()
![]() 操作Ⅰ的名稱是____;操作Ⅱ是根據
操作Ⅰ的名稱是____;操作Ⅱ是根據![]() 和
和![]() 兩物質在____
兩物質在____![]() 填性質
填性質![]() 上差異,采用____
上差異,采用____![]() 填操作步驟
填操作步驟![]() 、趁熱過濾得到
、趁熱過濾得到![]() 粗晶體的。
粗晶體的。
![]() 上述流程中可以循環使用的物質有石灰、
上述流程中可以循環使用的物質有石灰、![]() 、____和____
、____和____![]() 寫化學式
寫化學式![]() 。
。
![]() 向
向![]() 溶液中通入
溶液中通入![]() 以制備
以制備![]() ,該反應中的還原劑是_________。
,該反應中的還原劑是_________。
![]() 鉍酸鈉
鉍酸鈉![]() ,不溶于水
,不溶于水![]() 用于定性檢驗酸性溶液中
用于定性檢驗酸性溶液中![]() 的存在
的存在![]() 鉍元素的還原產物為
鉍元素的還原產物為![]() ,Mn的氧化產物為
,Mn的氧化產物為![]() 價
價![]() ,寫出反應的離子方程式_________。
,寫出反應的離子方程式_________。
![]() 寫出
寫出![]() 、KOH的熔融混合物中通入空氣時發生的主要反應的化學方程式___________。
、KOH的熔融混合物中通入空氣時發生的主要反應的化學方程式___________。
![]() 若不考慮物質循環與制備過程中的損失,則
若不考慮物質循環與制備過程中的損失,則![]() 可制得____
可制得____![]() 。
。
查看答案和解析>>
科目: 來源: 題型:
【題目】下列說法正確的是
A.1 mol O2的體積是22.4 L
B.1.7 g NH3中含有的質子數約為6.02×1023
C.8 g S在足量O2中完全燃燒轉移的電子數約為3.01×1023
D.0.5 mol·L1NaCl溶液中含有Cl的物質的量為0.5 mol
查看答案和解析>>
科目: 來源: 題型:
【題目】人體血液里存在重要的酸堿平衡:![]() ,使人體血液pH保持在7.35~7.45,否則就會發生酸中毒或堿中毒。其pH隨
,使人體血液pH保持在7.35~7.45,否則就會發生酸中毒或堿中毒。其pH隨![]() 變化關系如下表:
變化關系如下表:
| 1.0 | 17.8 | 20.0 | 22.4 |
pH | 6.10 | 7.35 | 7.40 | 7.45 |
下列說法不正確的是
A. 正常人體血液中, ![]() 的水解程度大于電離程度
的水解程度大于電離程度
B. 人體血液酸中毒時,可注射![]() 溶液緩解
溶液緩解
C. ![]() 的血液中,
的血液中, ![]()
D. pH=7.40的血液中, ![]() 的水解程度一定大于
的水解程度一定大于![]() 的電離程度
的電離程度
查看答案和解析>>
科目: 來源: 題型:
【題目】二氯烯丹是一種播前除草劑,其合成路線如下:
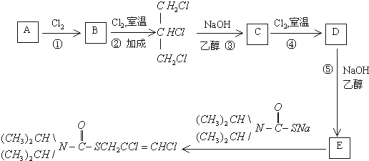
已知:D在反應![]() 中能生成的E,其結構只有一種可能.
中能生成的E,其結構只有一種可能.
![]() 寫出下列反應的類型:
寫出下列反應的類型:
反應![]() 是 ______ ,反應
是 ______ ,反應![]() 是 ______ .
是 ______ .
![]() 寫出下列物質的結構簡式:C ______
寫出下列物質的結構簡式:C ______
![]() 的系統命名為 ______ ,E中官能團的結構式 ______
的系統命名為 ______ ,E中官能團的結構式 ______
![]() 與NaOH水溶液反應的化學方程式 ______
與NaOH水溶液反應的化學方程式 ______
![]() 寫出C的同分異構體
寫出C的同分異構體![]() 核磁共振氫譜只有一種峰
核磁共振氫譜只有一種峰![]() ______
______
![]() 下列敘述正確的是 ______
下列敘述正確的是 ______
![]() 到B的反應條件為加熱
到B的反應條件為加熱 ![]() 到二氯烯丹的反應為加成
到二氯烯丹的反應為加成
![]() 堿性水解的產物之一分子式為
堿性水解的產物之一分子式為![]()
![]() 二氯烯丹酸性水解可生成
二氯烯丹酸性水解可生成![]() .
.
查看答案和解析>>
科目: 來源: 題型:
【題目】“低碳生活”是指減少能源消耗、節約資源,從而減少二氧化碳排放的生活方式。下列不符合“低碳生活”的做法是( )
A.用籃子代替塑料袋 B.經常開車上班
B.經常開車上班
C.使用節能燈泡 D.節約每一滴水
D.節約每一滴水
查看答案和解析>>
科目: 來源: 題型:
【題目】二氧化氯(ClO2)廣泛應用于紙漿漂白、殺菌消毒和水凈化處理等領域。工業上利用甲醇還原NaClO3的方法制備ClO2,工藝流程如下:
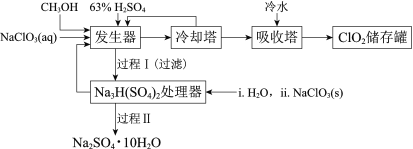
已知:a.發生器中制備ClO2的反應:12NaClO3+8H2SO4+3CH3OH= 12ClO2↑+3HCOOH+4Na3H(SO4)2↓+9H2O
b.相關物質的熔沸點:
物質 | CH3OH | HCOOH | ClO2 |
熔點/℃ | -97 | 9 | -59 |
沸點/℃ | 65 | 101 | 11 |
(1)ClO2可用于紙漿漂白、殺菌消毒是因其具有______性。
(2)冷卻塔用于分離ClO2并回收CH3OH,應控制的最佳溫度為______(填字母)。
A.0~10℃ B.20~30℃ C.60~70℃
(3)經過程Ⅰ和過程Ⅱ可以獲得芒硝(Na2SO4·10H2O)并使部分原料循環利用。
已知:Na2SO4·10H2O和Na2SO4的溶解度曲線如下圖:
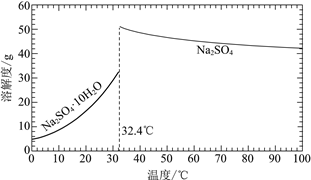
①Na3H(SO4)2處理器中獲得芒硝時需加入NaClO3固體,從芒硝溶解平衡的角度解釋其原因:______。
②結合Na2SO4·10H2O和Na2SO4的溶解度曲線,過程Ⅱ的操作是:在32.4℃恒溫蒸發,______。
③Na3H(SO4)2處理器的濾液中可以循環利用的原料是NaClO3和______。
查看答案和解析>>
科目: 來源: 題型:
【題目】青蒿素是一種有效的抗瘧藥。常溫下,青蒿素為無色針狀晶體,難溶于水,易溶于有機溶劑,熔點為156~157℃。提取青蒿素的方法之一是乙醚浸取法,提取流程如下:

請回答下列問題:
(l)對青蒿進行破碎的目的是__________________。
(2)操作I用到的玻璃儀器是__________,操作Ⅱ的名稱是_______。
(3)用下列實驗裝置測定青蒿素的化學式,將28.2g青蒿素放在燃燒管C中充分燃燒:

① 儀器各接口的連接順序從左到右依次為_______(每個裝置限用一次)。A裝置中發生的化學反應方程式為_________________。
② 裝置C中CuO的作用是_________________。
③ 裝置D中的試劑為_________________。
④ 已知青蒿素是烴的含氧衍生物,用合理連接后的裝置進行實驗.測量數據如下表:
裝置質量 | 實驗前/g | 實驗后/g |
B | 22.6 | 42.4 |
E(不含干燥管) | 80.2 | 146.2 |
則青蒿素的最簡式為__________。
(4)某學生對青蒿素的性質進行探究。將青蒿素加入含有NaOH 、酚酞的水溶液中,青蒿素的溶解度較小,加熱并攪拌,青蒿素的溶解度增大,且溶液紅色變淺,與青蒿素化學性質相似的物質是______(填字母代號)。
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖
查看答案和解析>>
科目: 來源: 題型:
【題目】寫出下列物質在水溶液中的水解離子方程式及沉淀溶解平衡方程式:
(1)NaClO水解離子方程式___________________________
(2)NH4Cl水解離子方程式____________________________
(3)KAl(SO4)2·12H2O水解離子方程式__________________________
(4)CaCO3沉淀溶解平衡方程式__________________________
(5)Fe(OH)3沉淀溶解平衡方程式__________________________
查看答案和解析>>
科目: 來源: 題型:
【題目】藥物Z可用于治療哮喘、系統性紅斑狼瘡等,可由X(咖啡酸)和Y(1,4
-環己二酮單乙二醇縮酮)為原料合成(如下圖)。
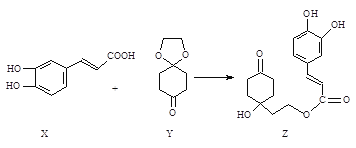
試填空:
(1)X的分子式為_______;該分子中最多共面的碳原子數為________。
(2)Y中是否含有手性碳原子_____(填“是”或“否”)。
(3)Z能發生_______反應。(填序號)
A.取代反應 B.消去反應 C.加成反應
(4)1 mol Z與足量的氫氧化鈉溶液充分反應,需要消耗氫氧化鈉________mol;
1 mol Z在一定條件下與足量H2充分反應,需要消耗H2 ________mol。
查看答案和解析>>
科目: 來源: 題型:
【題目】I.某學生用0.100molL-1的KOH標準溶液滴定未知濃度的鹽酸,其操作可分解為如下幾步:
A.用標準溶液潤洗滴定管2~3次;
B.取標準KOH溶液注入堿式滴定管至刻度“0”以上2~3cm 處;
C.把盛有標準溶液的堿式滴定管固定好,調節滴定管使尖嘴處充滿溶液;
D.調節液面至“0”或“0”以下刻度,記下讀數;
E.移取20mL待測鹽酸溶液注入潔凈的錐形瓶中,并加入2~3滴酚酞;
F.把錐形瓶放在滴定管的下面,用標準KOH溶液滴定至終點并記下滴定管液面的刻度。
實驗編號 | KOH溶液的濃度(mol/L) | 滴定完成時,KOH溶液滴入的體積(mL) | 待測鹽酸溶液的體積(mL) |
1 | 0.10 | 22.62 | 20.00 |
2 | 0.10 | 22.72 | 20.00 |
3 | 0.10 | 22.80 | 20.00 |
就此實驗完成填空:根據上述數據,可計算出該鹽酸的濃度約為__________(保留兩位有效數字)
II.亞硫酸鹽是一種常見食品添加劑。為檢驗某食品中亞硫酸鹽含量(通常以1kg樣品中含SO2的質量計),某研究小組用“碘氧化還原滴定法”進行測定,實驗流程如下:

(1)碘標準液應選用____(填“酸式”或“堿式”)滴定管盛裝,加注標準液之前必須對滴定管進行_____、洗滌、____。
(2)錐形瓶內的指示劑為_____,判斷達到滴定終點的現象是______________________。
(3)下列操作會使測定結果偏大的有_______
A.起始讀數時平視,終點讀數時俯視
B.未用標準液潤洗滴定管
C.步驟①中用稀鹽酸代替稀硫酸
(4)若取樣品w g,按乙方案測得消耗0.01000mol·L-1 I2溶液VmL,則1kg樣品中含SO2的質量是____g(用含w、V的代數式表示)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com